8 月 27 日,科伦药业发布半年报,营收 89.22 亿元,同比增长 14.50%;归母净利润 7.28 亿元,同比下降 5.91%;研发支出 6.66 亿元,同比增长 32.51%。
虽然净利润有所下降,但是销售收入保持良好的增长势头。2019 年上半年,科伦药业输液板块保持持续稳定增长。报告期内,公司抗生素中间体实现了稳产满产,销售收入较去年同期增长 10.10%,实现净利润 2.78 亿元。通过研发体系的建设和多元化的技术创新,公司新产品陆续获批上市。
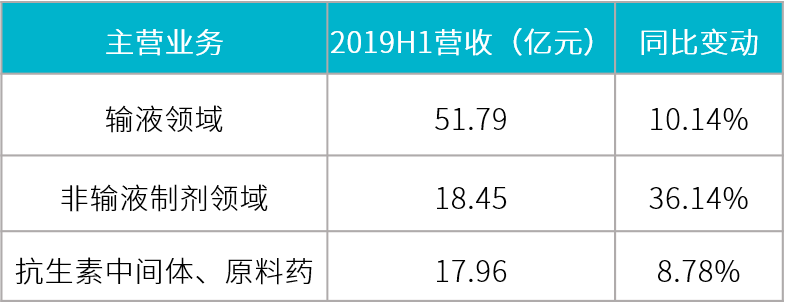
科伦药业 2019 H1 主要领域营收情况
报告期内,子公司伊犁川宁持续满产,实现销售收入 18.11 亿元,同比增长 10.10%,净利润 2.78 亿元,同比下降 20.60%。主要原因系部分产品竞争降价及所得税减免政策到期。广西科伦、邛崃项目技改稳步推进,工艺攻关持续进行。
4+7 品种销量增长显著
仿制药销量达预期
2019 年上半年,公司仿制药市场推广迅速,销量符合预期,4+7 中选品种销量增长显著,并且下一轮全国集采仍将受益。
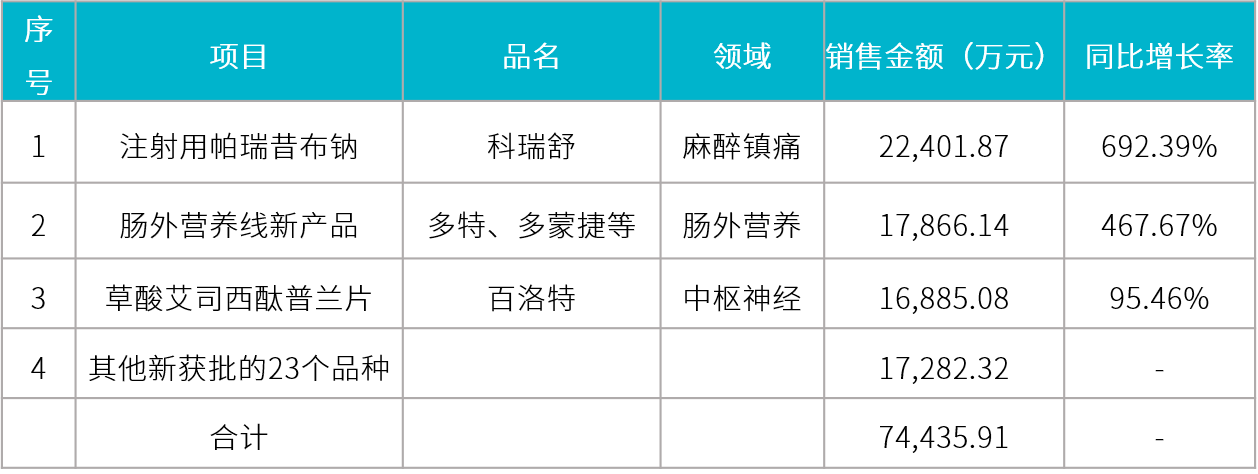
2019 H1 公司科瑞舒(注射用帕瑞昔布钠)销售额约 2.24 亿元,较去年同期增长 692.39%(2018 H1:2827 万元)。
百洛特(草酸艾司西酞普兰片)在 4+7 带量采购中标后,迅速覆盖了 11 个重点城市的 200 多家三级医院,对整体销售增长促进明显,上半年销售额约 1.69 亿元,较去年同期增 95.46%(2018 H1:8638 万)。同时,随着福建、河北等省份联动 4+7 中标结果和带量采购政策的进一步推进,科伦的市场份额还将进一步提升。
多特、多蒙捷等肠外营养品种销售额约 1.79 亿元(2018 H1:多特 2297 万元;多蒙捷 1990 万元)。
报告期间,公司主要新药销售额如下:
研发投入同增 32.5%
2 个 ADC 药物获 FDA 批临床
2019 年上半年,公司研发投入约为 6.66 亿元,同比增长 32.51%。
5 个仿制药获批上市
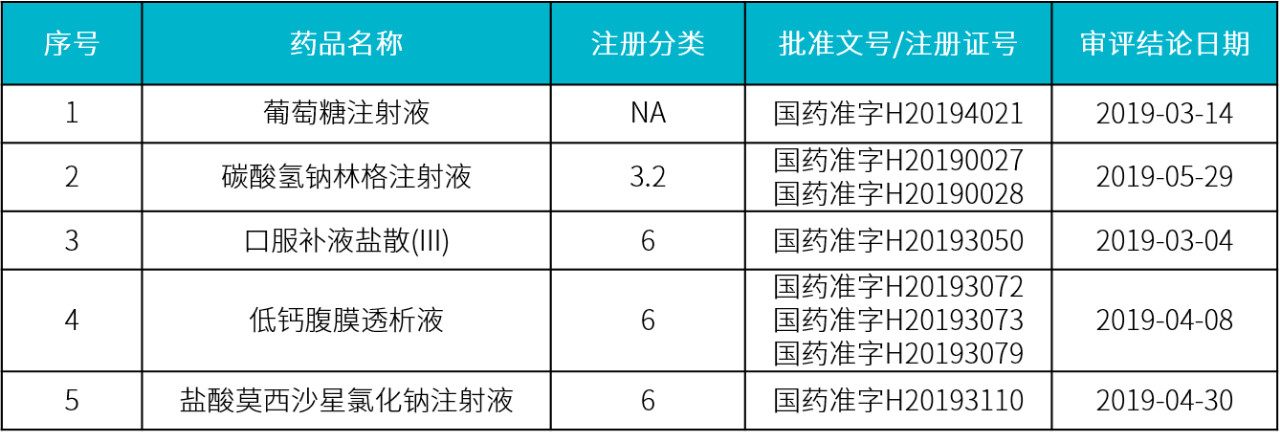
科伦 2019 年上半年获批 5 个仿制药品种,分别为碳酸氢钠林格注射液、葡萄糖注射液、口服补液盐散 (III)、低钙腹膜透析液、盐酸莫西沙星氯化钠注射液,大部分为 6 类仿制药;其中碳酸氢钠林格注射液为元 3.2 类,为国内第 2 家获批。
1 类乙肝新药获批临床
报告期内,公司 1 类创新药 KL060332 胶囊获批临床。KL060332 胶囊是一款科伦药业开发的具有自主知识产权的乙肝病毒核衣壳组装调节剂,有 5 mg,25 mg,50 mg, 200 mg 几种规格。目前全球尚无相同作用机制药物获批上市。
此外,棕榈酸帕利哌酮注射液仿制药的上市申请获批临床。
6 个在研生物药,2 个 ADC 药物获 FDA 批临床
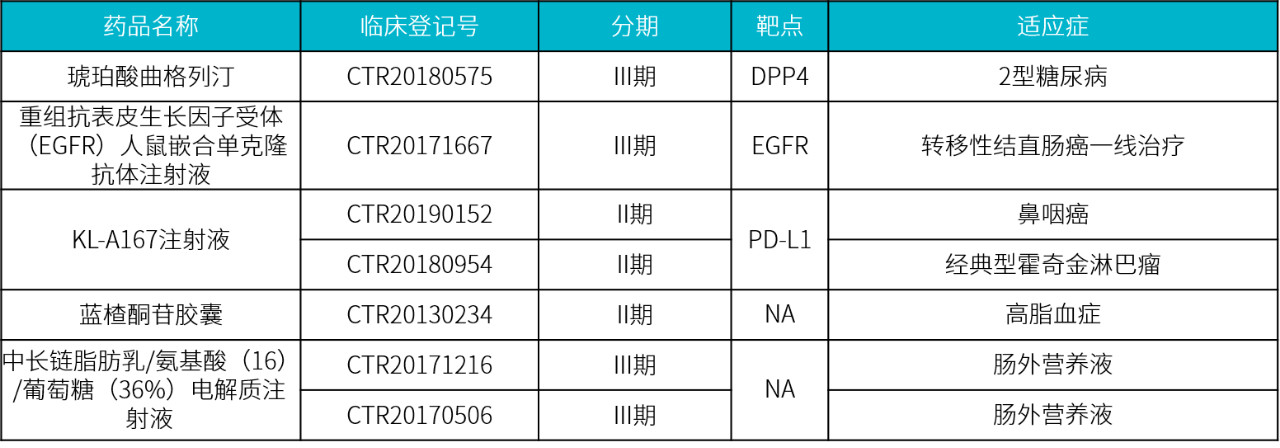
据 Insight 数据库统计,科伦药业国内在研的生物药有 6 个, 其中进展最快的是西妥昔单抗生物类似药,目前处于 3 期临床,用于转移性结直肠癌一线治疗。
其中,注射用 A166 是全球首个通过赖氨酸定点定量偶联、具有创新连接子和高活性毒素小分子的第三代抗 HER2 ADC,拟用于 HER2 阳性乳腺癌、胃癌等恶性肿瘤的治疗;该新药已经在 2018 年 5 月份获 FDA 批准临床。
同时,在 8 月 23 日,科伦药业控股子公司 KLUS PHARMA INC 收到 FDA 签发的书面通知,允许其「注射用 SKB264」抗体偶联药物(ADC)在美国开展临床试验。成为继注射用 A166(HER-2 ADC)后,又一个获得 FDA 批准开展临床试验的创新 ADC 药物。
KL-A167 注射液是科伦研发的抗 PD-L1 单克隆抗体,目前共有 5 个临床实验进行中,适应症涉及鼻咽癌、淋巴瘤、晚期实体瘤等。此外 KL-A167 注射液新适应症已经申请临床,目前已完成审评。
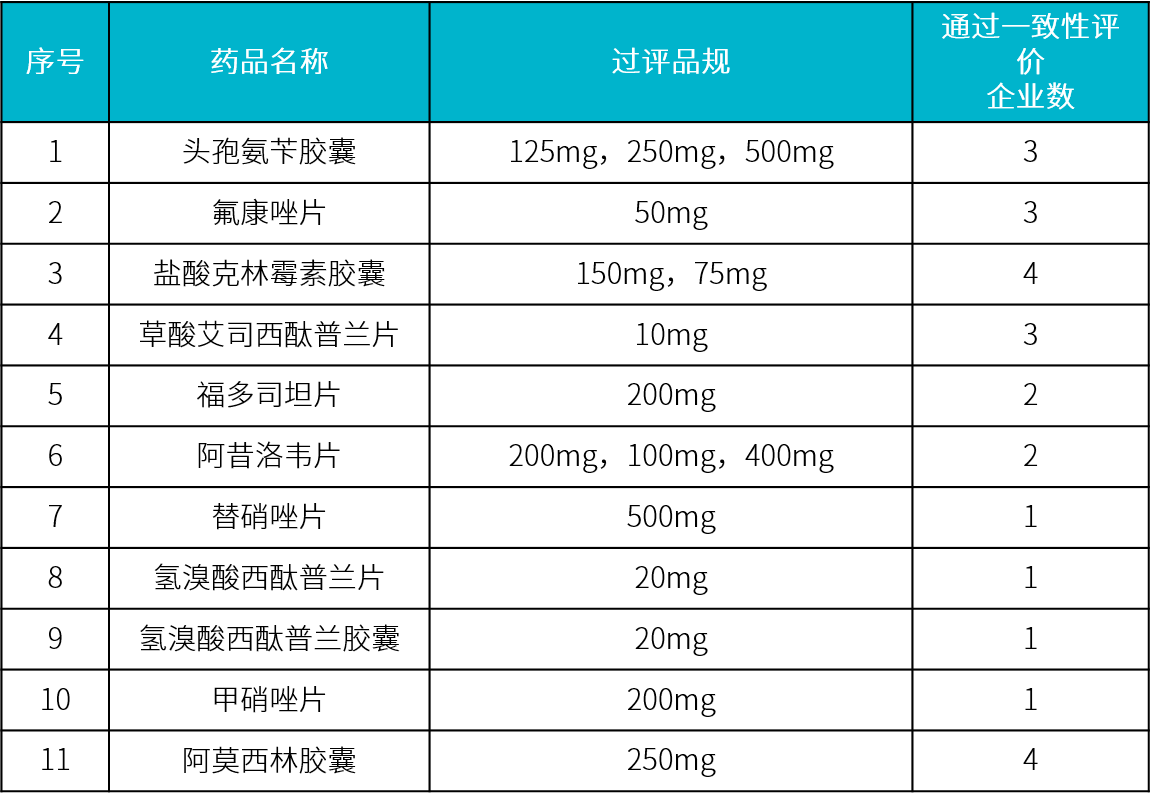
一致性评价通过 11 个
4 个暂为独家通过
据 Insight 数据库显示,科伦药业目前共有 11 个品种通过/视同通过一致性评价;其中,替硝唑片、氢溴酸西酞普兰片、氢溴酸西酞普兰胶囊、甲硝唑片目前为独家过评。
积极拓展国际业务
2019 年,公司继续推动国际化战略实施,积极开展海外市场拓展,实现海外销售收入 50,356 万元,同比增长 83.29%。其中,输液制剂出口 7,329 万元;抗生素中间体出口 39,725 万元,同比增长 107.53%。
报告期内,共开展日本等 9 个国家/地区共计 35 个项目的注册工作,产品涉及普通输液、治疗性输液和营养型输液,部分创新药物已向国外药监部门递交资料。新规格剂型输液产品通过日本 PMDA 认证,未来将实现对发达国家产品出口多元化。
目前哈萨克斯坦科伦生产供不应求,上半年销量显著提升,同比增长 91.7%。其中,俄罗斯销售数量占比为 53.47%,同比增长 219.94%。俄罗斯市场在销售数量和销售质量上均得到明显提升,推动哈萨克斯坦科伦盈利能力提升。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57