APOE基因E4变异是最主要的老年痴呆症风险变异,携带一条E4变异的人群,罹患老年痴呆症的风险增加3-4倍,而携带二条E4变异,得病风险增加12-15倍。E4变异很常见,大约20-30%的人群携带E4变异。携带E4变异的患者症状出现得更年轻,病程发展更快,脑中的淀粉样蛋白斑块也更多更大更结实。本文通过解析已知的实验证据,探讨E4变异对apoE蛋白质结构和功能的影响,以及这些变化如何导致淀粉样蛋白斑块的沉积,最终诱发老年痴呆症的症状。同时,也试图解释为什么以清除淀粉样蛋白为治疗机制的药物开发,临床实验结果都以失败告终。
第一部分:APOE基因E4突变是迄今发现的最大老年痴呆症风险
1. 老年痴呆症与APOE基因变异
阿尔茨海默病(Alzheimer’s Disease, AD),俗称老年痴呆症可能是最后一个完全无药可治的大病种,也是全球各药企最大的念想。过去30年针对老年痴呆症的新药开发都以失败告终,大把白花花的银子打了水漂,更让人失望的是黑夜漫漫兮不知路在何方。很多人开始纷纷抛弃淀粉样蛋白假说(amyloid beta hypothesis), 取而代之的是更时髦但机理尚且模糊的新概念。然而,在进军任何新靶点之前,很有必要仔细审核一下老年痴呆症的最大遗传风险因子,APOE 基因和它的E4变异是通过什么样的分子机制促使淀粉样蛋白堆积并最终诱发老年痴呆症的。
记忆和认知能力的逐渐丢失是老年痴呆症的症状,这些症状是源于大脑神经细胞的进行性死亡。老年痴呆症患者的大脑中有大量淀粉样蛋白沉积,并且随着脑细胞死亡,大脑严重萎缩。淀粉样蛋白假说曾经是主流公认的老年痴呆症致病机制。这一假说认为,淀粉样蛋白在神经细胞外沉积,是造成神经细胞死亡的前奏和诱因,因此,抑制淀粉样蛋白产生或清除淀粉样蛋白沉积,可能可以治疗或减缓老年痴呆症。然而, 迄今为止据于这一假设的药物设计在临床实验中都以失败告终。
老年痴呆症分为家族性早发型(familial early-onset Alzheimer’s disease) 和散发性晚发型(sporadic late-onset Alzheimer’s disease)。前者人数很少,约占老年痴呆症病人总数的5%,一般在65岁以前发病。这些早发型老年痴呆症是单基因疾病,主要涉及三个基因,APP, PSEN1和PSEN2。APP基因编码直接生产淀粉样蛋白的前体蛋白,而PSEN1和PSEN2基因编码参与切割淀粉样蛋白前体的酶。这三个基因上的某些突变会导致淀粉样蛋白过量产生。以上三个基因的致病机理为淀粉样蛋白假说提供了坚实依据。然而,大部分(95%以上)老年痴呆症是散发性晚发型,属于多基因复杂疾病(polygenic complex disease)。也就是说单个基因突变不能决定是否会得病,而是多个遗传因素互相加和或消减,同时又受性别年龄,饮食结构和生活习惯等多重环境因素影响。发病越早的老年痴呆症,基因的因素越大,而发病越晚的病人,则基因的因素越小,而更多受环境因素影响。虽然我们都认为老年痴呆症是一种无药可治的可怕疾病,但事实上,只那些没有早早死于癌症,心脏病,脑中风和其他致命疾病的幸运者,才有机会经历这种病。你越长寿,患上老年痴呆症的可能性就越大了。
APOE基因的E4变异是迄今为止发现的老年痴呆症最大风险因子。在75岁以前诊断为老年痴呆症的病人中,高达67%的患者携带E4变异。而在80岁以后才被诊断的患者中,E4的携带率只有13%, 这个比例和80岁以后脑子仍然健康人群一致。对白种人而言,携带一条E4变异,得老年痴呆的风险增加3-4倍,而携带二条E4变异,得病风险会增加到13-15倍。不同的种族对E4变异的敏感性也不一样,生活在非洲的黑人敏感性最低,携带一条E4变异并不增加老年痴呆症风险,而携带二条E4只稍微增加风险。而日本人敏感性最高,携带一条E4变异增加5-7倍风险,二条E4变异增加风险到33倍。然而,携带E4变异既不是罹患老年痴呆症的充分条件,也不是必要条;有大约一半携带E4变异的人群活到80岁还未被诊断患老年痴呆症,而相反在80岁以前就被诊断的患者中,约40%并不携带E4变异。而在80岁以后才被诊断的患者中,87%不携带E4变异。携带E4变异的老年痴呆症患者不仅发病时间较早,症情恶化得也更快,而且病理观察还发现,有E4变异的病人比没有E4变异的病人脑中的淀粉样蛋白斑块更多更大。
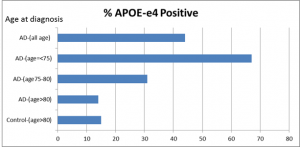
APOE基因E4变异在不同年龄段被诊断的老年痴呆症患者中的分布。
有100多个基因被报道与散发性晚发型老年痴呆症相关连,其中至少二十几个基因有很肯定的分子生物学机制。有的变异会减弱APOE基因E4的致病风险,例如CASP7基因的失活变异和ABCA1基因的增活变异;而有的则会加重E4的致病风险。
2. APOE基因与胆固醇代谢
APOE基因编码一个称为apoE的脂蛋白元(apolipoprotein), 主要在肝 脏和大脑中表达。通常脂蛋白元与油脂类分子相互嵌合形成脂蛋白微粒,协助油脂类分子在水相运输,并通过与细胞表面的受体相结合将油脂分子转运进入目标组织。血液中主要有五种脂蛋白微粒,包括乳糜微粒(chylomicron), 非常低密度脂蛋白(VLDL), 中密度脂蛋白(IDL), 低密度脂蛋白(LDL)和高密度脂蛋白(HDL)。通过脂蛋白微粒运输的油脂类分子包括甘油三脂,胆固醇,磷脂和各种脂溶性维生素等。apoE主要存在于三种脂蛋白微粒上,包括乳糜微粒,VLDL和HDL,其主要功能是参与胆固醇的吸收,合成和分配。
apoE与饮食中的胆固醇吸收和利用非常相关。 在大脑之外,apoE主要由肝细胞合成并分泌到血液中,高胆固醇饮食会诱导apoE合成。食物中的油脂分子经由肠道吸收并合成乳糜微粒。乳糜微粒是一种巨大的脂蛋白微粒,主要含有来自食物的甘油三脂,也有少量的胆固醇,磷脂和油溶性维生素(包括维生素A,D, K及红萝卜素等)。乳糜微粒经肠道分泌,通过淋巴管进入血液,在餐后浓度达到最高。乳糜微粒随着血液在身体中循环,经过肌肉,肝 脏和脂肪等组织时,相嵌在这些组织细胞表面的脂蛋白脂酶(lipoprotein lipase, LPL)就会将乳糜微粒上的甘油三脂“收割“下来,并吸收进入组织细胞。随着甘油三脂被“收割“,微粒越变越小,最后主要剩下胆固醇分子,称乳糜微粒残体。这时apoE与富含胆固醇的残体相嵌合,负责将残体及其所携带的胆因醇转运进入肝 脏和其他需要胆固醇的目标组织。可见,APOE是一个与饮食非常相关的基因。
身体中的胆固醇有两个来源,一个来源于食物,一个来源于肝 脏的自主合成(de novo biosynthesis)。富含胆固醇的食物包括禽蛋类,奶制品,鱼虾海鲜和动物内脏。当从食物中摄取的胆固醇不足时,就没有足够的胆固醇转运进入肝细胞,肝 脏就会启动自主合成来补充身体所需。肝 脏合成的胆固醇包装在VLDL脂蛋白微粒里进入血液。VLDL是我们通常说的“坏胆固醇”LDL的前体。apoE通过与VLDL嵌合参与肝 脏胆固醇的合成和分泌。此外,apoE还会与一类HDL脂蛋白微粒结合,参与从外围组织回收多余的及损坏的胆固醇分子,并逆向转运进入肝细胞进行再利用或消毁。APOE基因的E4变异也会增加心血管病的风险,但远没有增加老年痴呆症风险那么厉害。
肝 脏,生殖腺和肾上腺等组织有大量apoE受体表达。apoE依靠受体介导的内饮机制(receptor-mediated endocytosis)将胆固醇等油脂分子转运进入目标组织。表达apoE受体的组织是那些需要”进口”胆固醇为原料合成甾体激素的组织,例如生殖腺细胞用胆固醇为前体合成性激素;肾上腺细胞用之合成“紧张激素”可的松;甲状腺细胞用之合成甲状腺素,皮肤细胞用之合成维生素D等。肝 脏作为身体中胆固醇的”仓库”和”加工厂”,具有最多的受体,用于调度和平衡胆固醇的”进货“和”出货”。apoE受体主要包括LDLR(LDL receptor)和LRP(LDL receptor related receptor family) 受体家族。这些受体的共同特点是都具有一个或多个带负电荷胺基酸的脂蛋白结合区域,正好可以与脂蛋白上带正电荷胺基酸的受体结合区域相亲合。这些受体不是专一接收apoE的,其中LDLR更主要是在肝细胞上接收含apoB的脂蛋白微粒LDL。LDL就是我们通常说的”坏胆固醇”。apoB上也有一个与apoE相似的带正电荷胺基酸区域用于与受体结合。LDLR基因缺陷和APOB受体结合区域变异都会导致家族性高胆固醇症(familial hypercholesterolemia)。而APOE受体结合区域变异会导致家族性三型高血脂症(familial type III hyperlipidemia)。
在大脑中,apoE主要由星型胶质细胞(astrocytes)合成,并与胆固醇和磷脂嵌合而形成类似于血液中高密度脂蛋白的微粒(HDL-like lipoprotein particles)。不同于外周血液系统有五种脂蛋白微粒,大脑中只有两种脂蛋白微粒,均由星型胶质细胞合成, 一种含有apoE,另一种含有apoJ。apoE和apoJ都是脂蛋白元,其作用都是与油性分子嵌合形成脂蛋白微粒而协助油性分子在细胞间转运。大脑中,apoE是最主要的脂蛋白微粒,含脂量较高并且以胆固醇为主。apoJ含脂量低,主要含磷脂。apoE在大脑中的主要生理功能可能是运输胆固醇和磷脂到神经细胞,用于神经细胞的维护俢复和扩充。很有趣的是编码apoJ的基因CLU也与老年痴呆症风险相关,不过没有APOE基因的E4变异那么厉害。更有趣的是,apoE在大脑中的受体LRP1, LRP2和SORL1, 都是老年痴呆症风险基因。另外,星型胶质细胞上负责将胆固醇泵出到HDL-like 微粒上的ABCA1基因也是重要的老年痴呆症风险基因。这些观察指向,大脑中参与胆固醇转运的相关通道与老年痴呆症的发病机制严重相关。
星型胶质细胞有如大脑中的肝 脏,负责神经细胞的营养供应,其中一项重要功能就是自主合成胆固醇。大脑是人体胆固醇最富集的器官,神经细胞膜上的胆固醇含量大约是其他细胞膜的3-7倍。大脑中的胆固醇基本上完全由大脑自主中合成,饮食摄入及肝 脏合成的胆固醇均不能进入大脑。可见胆固醇对大脑神经系统的重要性,大脑根本不敢”相信”我们能控制好我们的饮食和 肝 脏, 以保障胆固醇的供运,而要完全自主掌控胆固醇的合成。星型胶质细胞合成的胆固醇与apoE嵌合, 形成HDL-like脂蛋白微粒,与神经细胞上的apoE受体结合, 从而将胆固醇等营养物质转运进入神经细胞。当神经细胞受损需要修复时,对胆固醇的需求就会增加。如果沒有得到足够的供运,就会启动神经细胞内部的胆固醇自主合成,这一过程会伴随产生更多的淀粉样蛋白。有实验观察显示,表达E4变异的星型胶质细胞分泌到细胞外的胆固醇较少,对神经细胞的胆固醇供应可能不足。同时,带有E4变异的神经细胞,在有压力的情况下,会生产更多易聚合的AB短肽。
参考文献:
http://www.alz.org/facts/ accessed on 10/22/2019
Ayers KL, Mirshahi UL, Chen RJ, et al. A loss of function variant in CASP7 protects against Alzheimer's disease in homozygous APOE ε4 allele carriers. BMC Genomics. 2016 Jun 23;17 Suppl 2:445. PMID: 27358062
Bertram L, McQueen MB, Mullin K, et al. Systematic meta-analyses of Alzheimer disease genetic association studies: the AlzGene database. Nat Genet. 2007 Jan; 39(1):17-23. PMID: 17192785
Engelman CD, Koscik RL, Sager MA, et al. Interaction between two cholesterol metabolism genes influences memory: findings from the Wisconsin Registry for Alzheimer's Prevention. J Alzheimers Dis. 2013;36(4):749-57. PMID: 23669301.
Gong JS, Kobayashi M, Michikawa M,et al. Apolipoprotein E (ApoE) isoform-dependent lipid release from astrocytes prepared from human ApoE3 and ApoE4 knock-in mice. J Biol Chem. 2002 Aug 16;277(33):29919-26. PMID:12042316.
Guerreiro RJ, Beck J, Gibbs JR, et al. Genetic variability in CLU and its association with Alzheimer's disease. PLoS One. 2010 Mar 3;5(3):e9510. PMID: 20209083.
Katzov H1, Chalmers K, Prince JA, et al. Genetic variants of ABCA1 modify Alzheimer disease risk and quantitative traits related to beta-amyloid metabolism. Hum Mutat. 2004 Apr;23(4):358-67. PMID: 15024730.
Long JM, Holtzman DM. Alzheimer Disease: An Update on Pathobiology and Treatment Strategies. Cell. 2019 Oct 3;179(2):312-339. PMID: 31564456.
Ma Y, Jun GR, Zhang X, Chung J, et al. Analysis of Whole-Exome Sequencing Data for Alzheimer Disease Stratified by APOE Genotype. JAMA Neurol. 2019 Jun 10.
Naj AC, Schellenberg GD; Alzheimer's Disease Genetics Consortium (ADGC). Genomic variants, genes, and pathways of Alzheimer's disease: An overview. Am J Med Genet B Neuropsychiatr Genet. 2017 Jan;174(1):5-26.



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57