罗氏拥有丰富的研发管线储备,截止2019年10月16日,有多达131个研发管线项目正在进行中,至少处于III期临床的有50个,其中新分子实体有14个,新适应症项目36个。我们今天就来综合临床研究项目数量、创新性、市场前景等方面盘点一下罗氏10个最具潜力的新药。
10。Gantenerumab
Gantenerumab是一种完全人源化IgG1单克隆抗体,可与大脑中的β-淀粉样蛋白特异性结合,用于治疗老年性痴呆症。科学家们通过30多年的研究认为β-淀粉样蛋白与老年性痴呆存在着紧密的关系,但是近年来的多个临床药物大部分可以减少β-淀粉样蛋白,却并不能缓解老年性痴呆的疾病进程。2014年罗氏也搁置了Gantenerumab的研究,直到2015年,Biogen的Aducanumab在1b期临床结果显示,Aducanumab能够降低前驱期或轻微阿尔茨海默病患者的淀粉样蛋白斑,同时可以延缓认知功能的下降,此研究结果佐证了目前科学家关于β淀粉样蛋白导致阿尔兹海默症的假说,给包括Gantenerumab在内的多个临床研究药物带来了希望,同时后续的生物标志物和疗效信号分析表明,在疾病进展最快的患者中,高剂量的Gantenerumab表现出一定疗效,这些促使罗氏又重新启动Gantenerumab的阿尔兹海默症临床III期试验,目前有4个临床III期项目正在进行中。
9。RG6042
RG6042是一种用于治疗亨廷顿病(HD)的第二代修饰反义寡核苷酸。 HD是一种罕见的遗传性、进行性疾病,HD的病因是编码亨廷顿蛋白(huntington protein,HTT)的基因出现三核苷酸序列CAG重复超过36次,从而编码结构异常的HTT,在功能上显现出能够杀死神经元细胞的**,严重影响患者的行动和思维能力,估计全球约有50万HD患者。
RG6042通过靶向人HTT mRNA来降低突变型HTT(mHTT)蛋白的表达水平,从而减缓或阻止HD患者的疾病进展。 RG6042原名为IONIS-HTTRx,是罗氏2017年12月与反义RNA领域的行业领导者Ionis达成协议共同开发。 该药已经获得美国FDA和欧盟EMA已授予的治疗HD的孤儿药资格,并获EMA授予治疗HD的优先药物资格(PRIME)。 2019年1月罗氏宣布该药进入临床III期研究阶段,目前已经开启了两项共包括接近2000名患者的III期临床研究。 预计该药2022年左右获批上市。
8。Idasanutlin
Gantenerumab是一种完全人源化IgG1单克隆抗体,可与大脑中的β-淀粉样蛋白特异性结合,用于治疗老年性痴呆症。科学家们通过30多年的研究认为β-淀粉样蛋白与老年性痴呆存在着紧密的关系,但是近年来的多个临床药物大部分可以减少β-淀粉样蛋白,却并不能缓解老年性痴呆的疾病进程。2014年罗氏也搁置了Gantenerumab的研究,直到2015年,Biogen的Aducanumab在1b期临床结果显示,Aducanumab能够降低前驱期或轻微阿尔茨海默病患者的淀粉样蛋白斑,同时可以延缓认知功能的下降,此研究结果佐证了目前科学家关于β淀粉样蛋白导致阿尔兹海默症的假说,给包括Gantenerumab在内的多个临床研究药物带来了希望,同时后续的生物标志物和疗效信号分析表明,在疾病进展最快的患者中,高剂量的Gantenerumab表现出一定疗效,这些促使罗氏又重新启动Gantenerumab的阿尔兹海默症临床III期试验,目前有4个临床III期项目正在进行中。
7。Entrectinib
Entrectinib是一种口服、选择性、具有中枢神经系统活性的酪氨酸激酶抑制剂,靶向治疗携带神经营养性原肌球蛋白受体激酶(NTRK1/2/3)或ROS1基因融合突变的局部晚期或转移性实体瘤。 Entrectinib能够穿过血脑屏障,阻断TRKA/B/C和ROS1蛋白的激酶活性,从而导致携带ROS1或NTRK基因融合突变的癌细胞死亡。
Entrectinib是由专注于肿瘤精准医疗的美国生物技术公司Ignyta研制,罗氏在2017年12月耗资17亿美元现金将其收购,在此之前此药已经分别被美国FDA和欧盟授予突破性药物资格和优先药物资格。 2019年8月FDA批准Entrectinib治疗ROS阳性的非小细胞肺癌和NTRK阳性的局部晚期实体瘤,值得注意的是,在此对于NTRK阳性的治疗是不限肿瘤类别的,这在药物审批历史上具有里程碑意义,这两种适应症预计也将在年内被欧盟批准。 目前罗氏还有多个临床项目研究Entrectinib联合PD1疗法治疗肿瘤的效果。
6。Xofluza
Xofluza是一种内切核酸酶抑制剂,通过抑制流感病毒中的CAP帽子结构依赖性内切核酸酶来抑制流感病毒的复制,这是一种全新的抗流感机制,主要用于抑制A型和B型流感病毒,包括对其他药物耐药的流感株和禽流感株。
Xofluza由日本药企盐野义发现,由罗氏和盐野义进行全球共同开发。Xofluza于2018年10月率先获得美国FDA批准,用于12岁及以上健康人群治疗症状不超过48小时的急性、非复杂性流感,它是FDA近20年来批准的首个新型的治疗流感的抗病毒 药物,2019年10月FDA又批准Xofuza用于流感相关并发症的高危人群。目前罗氏还有多达6项III期临床研究,用来全面探索Xofuza在预防以及治疗流感病毒中的作用。
5。Etrolizumab
Etrolizumab是一种靶向于整合素α4β7 和αEβ7 的β7 亚基的人源化单克隆抗体,处于治疗溃疡性结肠炎以及克罗恩病的III其临床研究中,这两种疾病都属于严重的自身免疫性疾病。
目前治疗自身免疫疾病的主流药物是TNF-a抑制剂,如修美乐、恩利、类克等,整合素抑制剂将是非常重要的后备军,当病人对TNF-a抑制剂治疗无反应时,整合素抑制剂可能会带来惊喜。
Etrolizumab治疗溃疡性结肠炎的适应症预计2020年左后获批上市,在此领域已经有武田的Vedolizumab被批准上市,此药物的靶点比Etrolizumab少一个,仅为α4β7,但销售额相当不错,2018年销售额接近10亿美元,有理由相信Etrolizumab的销售额只会高于Vedolizumab。
4。Polatuzumabvedotin
这款抗体偶联药物(ADC)由3部分组成: 靶向于B细胞表面抗原CD79b的重组人源化抗体polatuzumab、一个链接子以及小分子药物MMAE(单甲基奥瑞他汀E)。
CD79b是B细胞受体的一部分,在超过90%的非霍奇金淋巴瘤的B细胞上都有表达,它与抗原结合后可以迅速被内吞并被传递到溶酶体中,这一特点使得它成为ADC开发的一个热门靶点。 ADC作用于细胞分裂的重要环节: 或遗传物质的复制,或微管蛋白的组装等,Polatuzumab vedotin的链接子在细胞外部不会断裂,因此具有强**的MMAE就不会被随意释放,只有识别CD79b并被内吞到肿瘤细胞内的溶酶体后才发挥其**作用。
该药于2019年6月被FDA批准上市,用于联合治疗复发性或难治性弥漫性大B细胞淋巴瘤。 目前罗氏还有多个临床项目正在进行,研究Polatuzumab vedotin一线治疗弥漫性大B细胞淋巴瘤以及治疗复发性或难治性滤泡性淋巴瘤的效果,预计这两个适
3。Ipatasertib
Ipatasertib是一种高选择性的pan-Akt抑制剂,可阻断PI3K / AKT信号传导途径,此信号途径在包括乳腺癌、前列腺癌等多种癌症细胞中被激活,因此Ipatasertib的潜在适应症包括多种实体瘤,其中最令人关注的就是三阴性乳腺癌(TNBC)的临床研究,三阴乳腺癌一直是临床治疗的难点,因为它不像雌孕激素受体阳性乳腺癌可以用内分泌疗法,也不像HER2阳性的乳腺癌有比较成熟的靶向治疗药物。
在已经完成的名为LOTUS的II期临床试验中,Ipatasertib联合化疗药物可以将TNBC的疾病进展和死亡风险降低56%(HR = 0.44),目前该药已经推进到III期临床研究阶段,评估其联合化疗药物紫杉醇治疗晚期三阴性乳腺癌和HR+/HER2-乳腺癌的疗效和安全性,该研究于2018年1月启动,预计将在2021年12月完成; 同时在进行还有治疗非转移性去势抵抗性前列腺癌(CRPC) 的III期临床研究; 另外还有多个研究Ipatasertib对其他实体瘤治疗效果的临床研究正在进行中。
2。Faricimab
Faricimab是一种靶向血管生成素-2(Ang-2)和血管内皮生长因子A(VEGF-A)的双特异性抗体,用于治疗包括糖尿病黄斑水肿(DME)以及新生血管(湿性)年龄相关性黄斑变性(nAMD)在内的多种眼科疾病。
Ang-2信号传导通路与血管不稳定性和微血管炎症有关,而VEGF-A可以促进新生血管生成,因此Faricimab可以增强相关眼科疾病患者的血管稳定性、减少新生血管的形成、减轻炎性渗出等,理论上可起到更好的治疗效果。而罗氏最近公布的临床研究结果也支持了这一点:Faricimab治疗nAMD的II期临床研究STAIRWAY的数据显示,在治疗第52周时,与每4周一次的雷珠单抗治疗组相比,每16周一次Faricimab治疗组和每12周一次Faricimab治疗组显示出相当的持续视力结果。
罗氏已经将该药推进到治疗DME以及nAMD的III期临床研究中,预计前者将在2021年获批,后者最快2022年。 目前眼科疾病的市场高达数百亿美元,其中大部分被VEGF靶向药物占据,仅阿柏西普和雷珠单抗的年销售额就接近100亿美元,Faricimab上市后将是它们强有力的竞争者。
1。Atezolizumab
Atezolizumab(Tecentriq ? )是罗氏旗下基因泰克开发的一种PD-L1单克隆抗体。2016年5月美国FDA批准Tecentriq ? 作为二线药物用于治疗晚期膀胱癌,使它成为全球首款获批上市的PD-L1单抗。截止到2019年11月Tecentriq ? 已经在非小细胞肺癌、三阴乳腺癌、尿路上皮癌等多个适应症上获批,而更多的适应症已经处于在审,或者III期临床研究阶段;尤其最近一段时间好消息不断:Tecentriq ? +含铂化疗一线治疗膀胱癌III期临床成功、Tecentriq ? +Avastin组合治疗肝癌III期临床显著延长总生存期和无进展生存期、Tecentriq ? 单药一线治疗PD-L1高表达患者III期临床提前获得成功……而这还远不是全部,罗氏发布的研发管线报告显示,Tecentriq ? 还有多达数十个临床研究正在进行中,包括单药或联合其他药物,适应症几乎包括所有常见的实体瘤,Tecentriq ? 在PDL-1领域已经占据绝对的优势,2019年前三季度销售额超过13亿美元,预测其峰值年销售额不低于50亿美元。
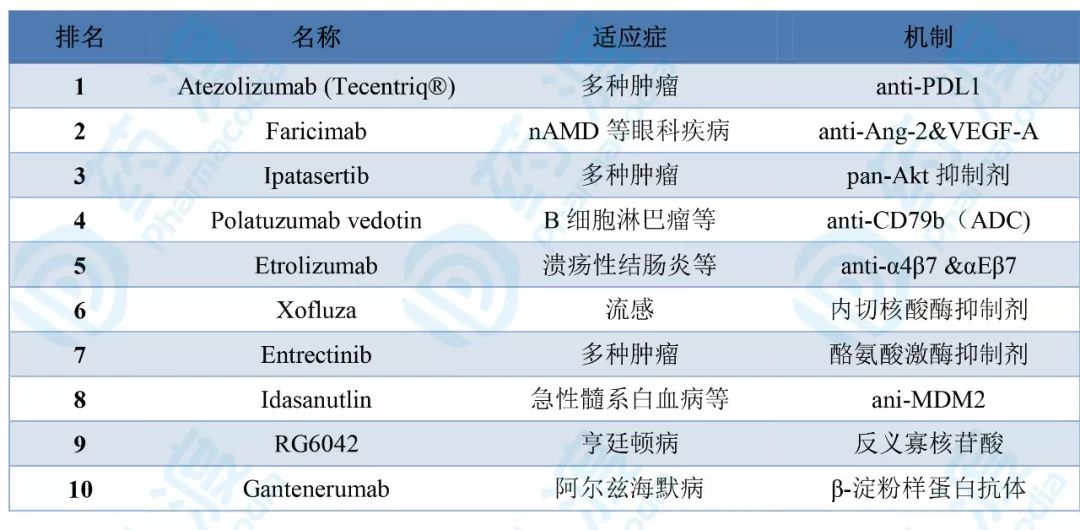
罗氏10大潜力药物



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57