精彩内容
日前,奥赛康以仿制4类申报的甲磺酸仑伐替尼胶囊上市申请及注射用替加环素一致性评价补充申请获得CDE承办受理。作为国内PPIs注射剂龙头企业,奥赛康业绩稳步提升,同时持续加大研发投入。目前公司已提交11个注射剂一致性评价补充申请,拿下DPP4抑制剂沙格列汀首仿后,还有8大品种抢首仿,此外肺癌1类新药即将报产。
糖尿病领域实现零突破,8大品种抢首仿
2019年1月9日,奥赛康按仿制4类申报的沙格列汀片获国家药监局批准上市,适应症为2型糖尿病。奥赛康不仅收获该产品国内首仿,同时也是首家过评,此外还实现了公司在糖尿病领域零的突破。
2020年3月28日,奥赛康以仿制4类申报的甲磺酸仑伐替尼胶囊上市申请获得CDE承办受理。仑伐替尼是一种口服多靶点激酶抑制剂(TKI),由日本卫材研发,2019年前三季度全球销售额为805亿日元,同比去年同期增长186%;2018年3月,卫材与默沙东就仑伐替尼全球联合开发及商业化的战略合作达成协议,据默沙东披露的财报数据,2019年仑伐替尼全球销售额为4.04亿美元。
表1:奥赛康申报上市仿制药中未有首仿上市的品种
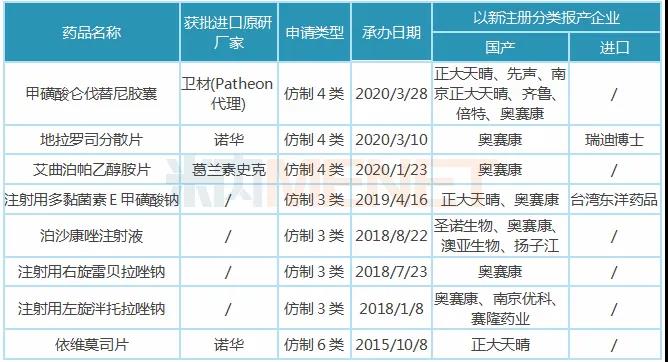
数据显示,含仑伐替尼在内,目前奥赛康申报上市的仿制药中有8个还未有首仿获批上市,其中地拉罗司分散片、艾曲泊帕乙醇胺片、泊沙康唑注射液、注射用右旋雷贝拉唑钠、注射用左旋泮托拉唑钠5个品种由奥赛康独家报产或审评进展最快,有望以首仿获批上市。
注射用多黏菌素E甲磺酸钠、泊沙康唑注射液、注射用右旋雷贝拉唑钠、注射用左旋泮托拉唑钠4个品种在国内市场暂时处于空白状态。右雷贝拉唑钠、左泮托拉唑钠分别是雷贝拉唑钠、泮托拉唑钠的优势构型,2018年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)终端,注射用雷贝拉唑钠、注射用泮托拉唑钠的销售额分别为16.26亿元、79.13亿元。
地拉罗司分散片、泊沙康唑注射液2个品种列入国家首批鼓励仿制药品清单。由诺华研发的地拉罗司分散片是目前治疗铁过载唯一有效药物,2019年全球销售额9.75亿美元,奥赛康是国内首家完成BE试验并申报上市的公司。
默沙东研发的泊沙康唑为新一代三唑类抗真菌药,2019年全球销售额6.62亿美元。目前国内市场无泊沙康唑相关仿制药上市销售,原研厂家的泊沙康唑口服混悬液、泊沙康唑肠溶片分别于2013年、2018年获批进口。奥赛康与上海宣泰签署协议,获得泊沙康唑肠溶片在中国大陆地区的独家推广权,上海宣泰以仿制4类提交的泊沙康唑肠溶片上市申请于2019年2月19日获得CDE承办受理,并于同年9月纳入优先审评,预计2020年能以首仿获批上市;泊沙康唑注射液还未获批进口,奥赛康的产品以“专利到期前1年的药品生产申请”为由获纳入优先审评,预计2020年首仿上市。
11个品种在审,跻身注射剂一致性评价申报数TOP10
2020年3月27日,奥赛康提交的注射用替加环素一致性评价补充申请获得CDE承办受理,成为公司第11个申报一致性评价的注射剂。
图1:注射剂一致性评价申报品种数超过10个的企业
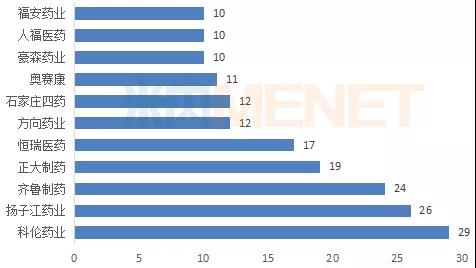
注:申报品种数相同排名并列
数据显示,目前150个注射剂有企业提交一致性评价补充申请,涉及108家企业(以集团计),申报品种数TOP10企业中,科伦药业以29个品种领跑,而奥赛康以11个品种位列第七。
表2:奥赛康提交一致性评价补充申请的注射剂
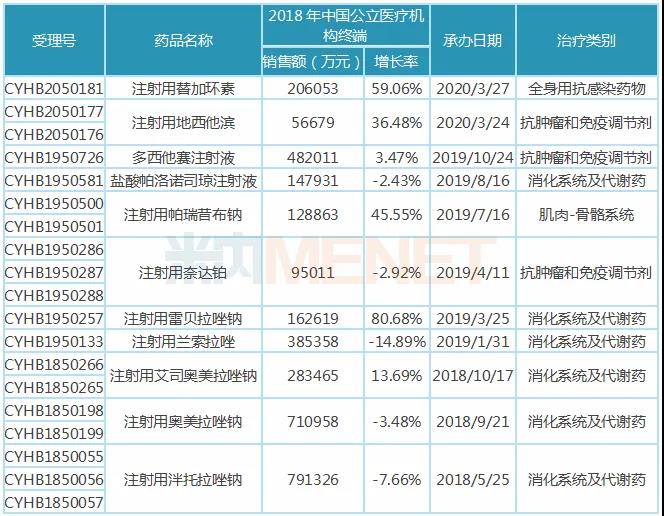
奥赛康申报一致性评价的注射剂均为临床畅销药,数据显示,除注射用奈达铂、注射用地西他滨外,其余9个注射剂在2018年中国公立医疗机构终端销售额均超过10亿元,其中注射用奥美拉唑钠、注射用泮托拉唑钠年销均超70亿元。
奥赛康主要产品涉及消化道溃疡、肿瘤、耐药菌感染、糖尿病等4个治疗领域。在审的11个注射剂中有6个为消化系统及代谢药,其中有5个为质子泵抑制剂(PPIs)注射剂,未来若顺利过评,将进一步夯实公司在消化性溃疡领域的市场竞争力;有3个抗肿瘤药,多西他赛注射液在2018年中国公立医疗机构终端抗肿瘤化药竞争格局中,以6.06%的市场份额排位第一。
表3:11个注射剂一致性评价申报情况
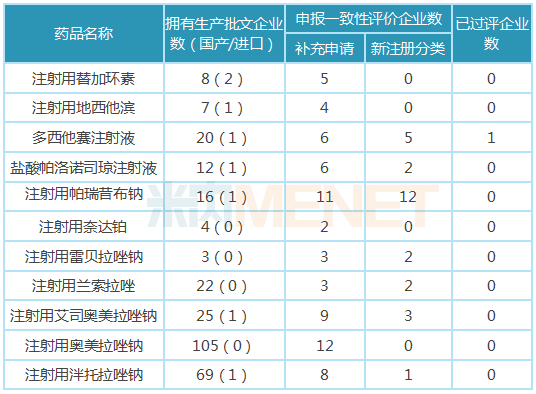
除了多西他赛注射液,其余10个注射剂均未有企业过评,其中注射用泮托拉唑钠、注射用奥美拉唑钠、注射用雷贝拉唑钠、注射用奈达铂4个品种为奥赛康首家提交一致性评价补充申请。
注射用帕瑞昔布钠、注射用艾司奥美拉唑钠、注射用奥美拉唑钠、多西他赛注射液4个品种竞争激烈,申报一致性评价企业数(含补充申请及新注册分类申报上市)均超过10家。
研发创新不止步,肺癌1类新药即将报产
奥赛康是国内治疗与胃酸分泌相关疾病药物的领军企业,是目前最大的PPIs注射剂生产企业之一,涵盖国内已上市6款PPIs注射剂中的5个。依托PPIs及抗肿瘤药优势产品组群,奥赛康近几年来业绩稳步增长。
2月27日发布的业绩快报显示,2019年奥赛康实现营业收入45.19亿元,同比增长14.93%;利润总额9.1亿元,同比增长20.60%;归母净利润7.93亿元,同比增长18.41%。
业绩稳步提升的同时,奥赛康也持续加大研发投入,2019年上半年研发投入1.45亿元,同比去年同期增长13.31%,占同期营业收入的比例为6.3%。除了定位临床亟需及国内首仿药,公司还瞄准了创新药板块。
奥赛康首个1类创新药ASK120067临床进展顺利,目前已获得一线用药的III期临床伦理批件。2019年5月,ASK120067获得CDE认可,完成临床II期研究后可有条件批准上市,预计2020年申报生产。
ASK120067是靶向作用于T790M的三代EGFR抑制剂,用于治疗非小细胞肺癌。全球首款三代EGFR抑制剂为阿斯利康的奥希替尼,2019年全球销售额31.89亿美元。虽然首款国产三代EGFR抑制剂已被豪森药业拿下,但由于市场空间巨大,上市的同类品种不多,ASK120067若获批上市仍有潜力成为重磅单品。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57