FGFRs
FGFRs是一类典型的受体酪氨酸激酶(receptor tyrosine kinases,RTKs), 其家族包括FGFR1、FGFR2、FGFR3和FGFR4四种受体,它们均由胞外区、跨膜区和胞内酪氨酸激酶区三个部分组成。FGFR的高表达、突变等导致其信号通路异常激活,与多种疾病的发生发展密切相关,包括肺癌、胃癌、乳腺癌、结直肠癌、慢性粒细胞白血病、胆管癌、脑胶质母细胞瘤、软骨肉瘤、脂肪瘤病、膀胱癌等。
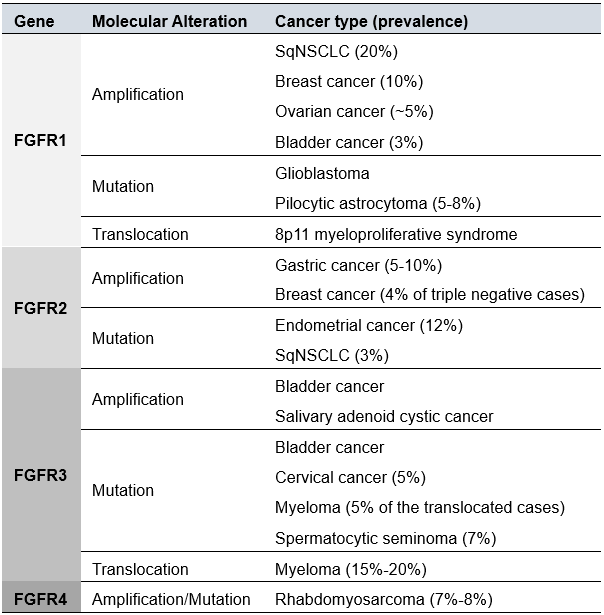
表一 FGFRs靶点在不同肿瘤中的分布
已上市的FGFRs靶点抑制药物
对FGFRs小分子抑制剂的研究始于上世纪90年代,晚于其他类似靶标如血管内皮生长因子受体(VEGFR)和表皮生长因子受体(EGFR)家族的研究。根据抑制剂与FGFR的蛋白结合位点的不同,可将其分为两种类型,第一类是通过靶向膜内酪氨酸激酶域,抑制FGFR的催化活性或酪氨酸自磷酸化,该类抑制剂均为小分子化合物。另一类是靶向FGFR膜外免疫球蛋白域,与FGFs 竞争性结合FGFR膜外区,阻断FGF-FGFR结合和通路激活。
虽然已上市的多靶点酪氨酸激酶抑制剂(TKIs)可用于治疗存在FGFRs突变的肿瘤,但是FGFR不是其主要靶点(表二)。如治疗白血病的ponatinib,其主要靶点为Abl、PDGFRα、VEGFR2、FGFR1。目前,能够实现选择性抑制FGFRs靶点的已上市药物只有厄达替尼Balversa (erdafitinib)。另外,近日FDA正式宣布加速批准Incyte公司开发的FGFR2抑制剂pemigatinib上市,用于治疗FGFR2基因融合或其它重排类型的经治晚期胆管癌患者。
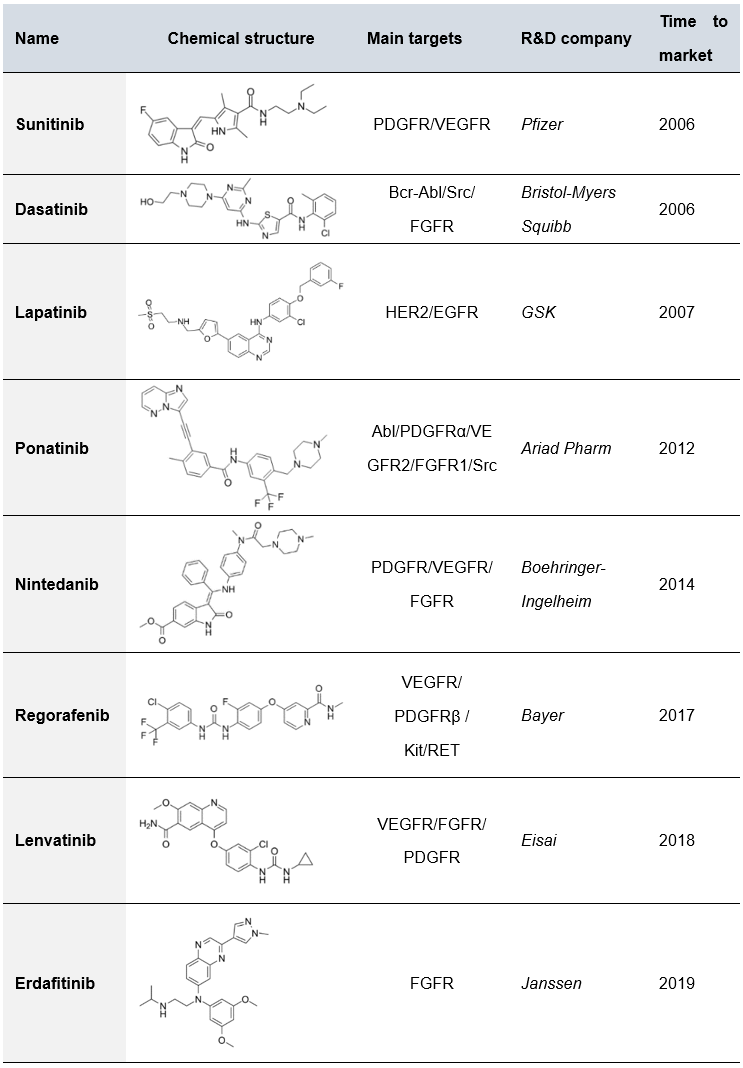
表二 可用于FGFR靶点抑制的已上市酪氨酸激酶抑制剂TKIs
FGFRs靶点在研药物
目前,有多款FGFRs抑制剂正处于临床研究阶段,下面进行简单的介绍。
Pemigatinib
Pemigatinib是胆管癌的首个靶向新药。该药是针对FGFR亚型1/2/3的强效选择性口服抑制剂,在既往临床研究中已证实该药物对FGFR基因突变的肿瘤细胞具有选择性的药理学活性。此药二线治疗胆管癌患者的有效率ORR达35.5%,疾病控制率DCR为82%。近期,美国FDA正式宣布加速批准Incyte公司开发的FGFR2抑制剂pemigatinib上市,治疗FGFR2基因融合或其它重排类型的经治晚期胆管癌患者,标志着胆管癌唯化疗的时代的终结。
除了二线治疗胆管癌患者,Pemigatinib在一线也展开了一项名为FIGHT 302III期研究,该研究是头对头比较,Pemigatinib与吉西他滨联合顺铂化疗一线治疗不可手术切除或转移性的伴FGFR2重排晚期胆管癌患者的疗效。
不久前,信达生物宣布中国第一例患者已完成pemigatinib首次给药。该项研究的目的是评估pemigatinib在既往至少接受过一线系统治疗、成纤维细胞生长因子受体2(FGFR2)基因融合或重排的中国晚期胆管癌患者中的有效性和安全性,本研究结果将用于pemigatinib在中国的新药上市申请(NDA)。
Infigratinib (BGJ398)
2018年1月,BridgeBio公司宣布从诺华(Novartis)公司获得了抗癌在研新药infigratinib(BGJ398)的授权,并由其子公司QED Therapeutics负责推动这种强效选择性酪氨酸激酶受体FGFR抑制剂的开发。Infigratinib是一种经口服给药的,ATP竞争性FGFR1-3酪氨酸激酶抑制剂,用于治疗FGFR驱动的疾病,包括胆管癌,尿路上皮癌(膀胱癌)和儿童软骨发育不全。2020年1月初被FDA授予快速通道资格。
目前,一项针对Infigratinib用于胆管癌(CCA)一线治疗的临床三期实验PROOF Trial (NCT03773302)正在进行当中。本研究的目的是比较口服Infigratinib与标准护理化疗(吉西他滨联合顺铂)一线治疗FGFR2基因融合/易位的无法切除的局部晚期或转移性胆管癌患者的疗效和安全性。受试者随机2:1接受Infigratinib或吉西他滨联合顺铂治疗。另一项三期临床实验PROOF 302 (NCT03773302)目前也在进行当中。这是一项多中心,双盲,随机,安慰剂对照研究,旨在评估在患有浸润性尿路上皮癌和FGFR3基因改变(突变,基因融合或重排)的成年患者手术后给予口服Infigratinib作为辅助治疗的疗效。
Rogaratinib (BAY1163877)
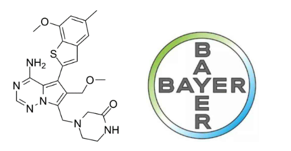
Rogaratinib (BAY 1163877)是由拜耳公司开发一种具有口服活性的高效、选择性的小分子pan-FGFR(FGFR1-4)抑制剂。Rogaratinib目前正作为单一疗法(NCT03762122, NCT03410693)以及联合免疫检查点抑制剂(NCT03473756)或靶向治疗(NCT03517956, NCT03088059)等进行多个临床试验。其中,NCT03410693 已进入临床三期研究,在FGFR阳性、局部晚期或转移性尿路上皮癌患者中评价rogaratinib疗效和安全性,证明rogaratinib对于总生存期的延长优于化疗。
2019年ASCO摘要中收录了rogaratinib的数据(J Clin Oncol 37:15s, 2019,suppl; abstr e20661)。研究纳入了40例FGFR在mRNA中阳性的晚期NSCLC患者。ORR为5.6%(1例反应持续了16个月以上),DCR为64%。药物安全性方面,Rogaratinib的耐受性尚可,大部分为轻中度AE。
Futibatinib (TAS-120)

Futibatinib (TAS-120) 是由日本Taiho公司开发的一种口服生物可利用地,高选择性的,不可逆的 FGFR抑制剂。Futibatinib (TAS-120) 与 FGFR 的 ATP 口袋中高度保守的 P 环半胱氨酸残基共价结合,对野生型 FGFR1/2/3/4 以及某些 FGFR2 激酶结构域突变表现高特异性效力,属于第二代FGFR抑制剂。
2019年8月,Cancer Discovery 杂志(Cancer Discovery 2019, 9, 1064.)报道了TAS-120在抗耐药方面的新进展。4名接受一代药BGJ398治疗起效但是后来有耐药的胆管癌患者,接受了TAS-120治疗,2名患者出现客观缓解,另外2名患者疾病稳定,控制率100%。其中2位有效患者的PFS超过一年,显示出良好的前景。
目前,Futibatinib的III期FOENIX-CCA3(NCT04093362)研究正在评估Futibatinib一线治疗具有FGFR 2基因重排的晚期胆管癌(CCA)患者的有效性和安全性。此外,Futibatinib的II期Basket研究(NCT04189445)正在评估Futibatinib治疗具有FGFR基因异常的晚期实体瘤的有效性和安全性。
AZD4547
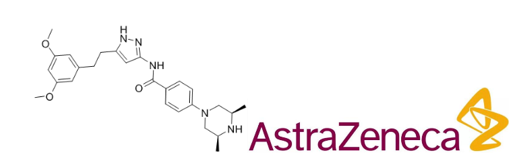
AZD4547是一种选择性FGFR抑制剂,作用于FGFR1/2/3的IC50值为0.2nM/2.5 nM/1.8nM,对FGFR4、VEGFR2 (KDR)的活性较弱,对IGFR、CDK2和p38几乎没有活性。
AZD4547主要在进行肺鳞癌和胃癌的临床试验。15名FGFR1基因扩增的肺鳞癌患者接受了AZD4547治疗,1名患者客观缓解,2名患者疾病稳定超过3个月;另外一项入组了43名晚期肺鳞癌患者的小规模临床试验,2名患者客观缓解,中位总生存时间为7.5个月。
2018 ASCO年会公布了AZD4547在FGFR突变/扩增/融合实体瘤中的治疗效果,研究结果显示总体ORR 9.5%,SD 47.6%,中位PFS 3.8个月。
目前,恶性胸膜间皮瘤(MPM)患者经一线化疗后复发,尚无有效治疗方法。2020年2月,Lung Cancer杂志刊登了一项AZD4547的单中心,开放标签,单臂II期研究结果,以评估 AZD4547作为二线或三线治疗恶性胸膜间皮瘤的疗效(Lung Cancer 2020, 140, 87-92.)。主要终点是6个月无进展生存期(PFS6)。实验结果显示,24名患者中有3名(12%)在6个月时无进展,说明 AZD4547对一线铂类化学疗法治疗后进展的MPM患者未显示疗效,实验终止。
2019年11月,上海和誉医药宣布与阿斯利康(AstraZeneca)就创新药AZD4547的开发和商业化达成全球性独家授权协议。根据协议,和誉医药获得AZD4547全球独家开发、生产以及商业化的许可。阿斯利康将获得相应的首付款、里程碑及销售提成。
另外一些处于临床开发阶段的FGFRs抑制剂见表三。
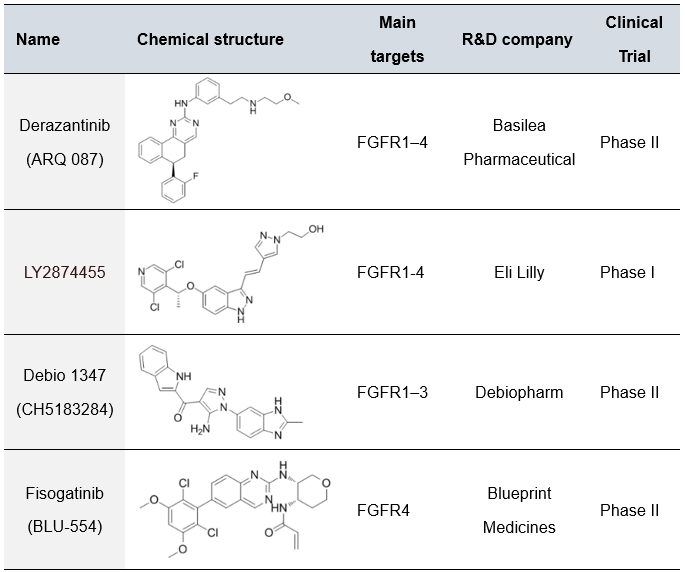
表三 处于临床阶段的FGFR抑制剂
结语
FGFR抑制剂的发展为FGFRs驱动的肿瘤患者带来了靶向治疗的希望。如Pemigatinib的开发与上市,是胆管癌靶向治疗里程碑式的成果。但是,FGFR抑制剂的研究也面临着许多的挑战。如耐药性的产生,抑制剂类药物**所导致的的剂量限制性等等。这也是未来FGFR抑制剂类药物研发所要解决的重点问题。如TAS-120对FGFR的不可逆结合,克服了部分耐药性的问题。目前,众多医药研发公司对FGFRs抑制剂赛道均有布局,相信FGFR抑制剂类药物能为肿瘤患者带来更多的希望。
参考文献
1.Cells 2019, 8, 614.
2.Clin Cancer Res 2020,26,764.
3.Eur J Med Chem 2020, 186, 111884.
4.https://clinicaltrials.gov/
点击下图进行CPhI & P-MEC China 2020观众预登记!立省100元门票



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57