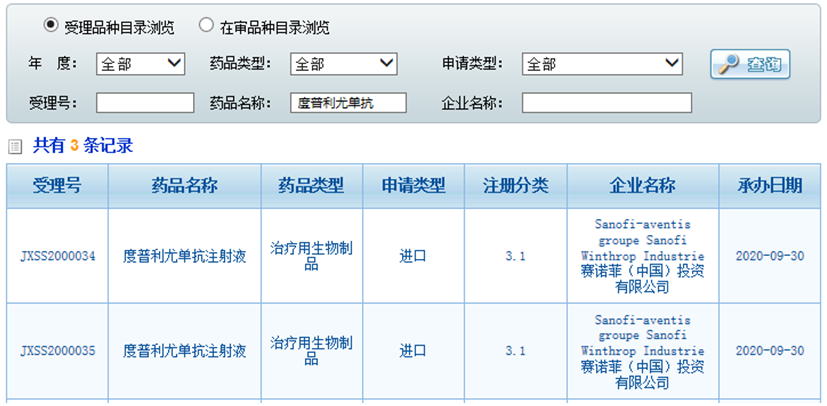
9月30日,赛诺菲「普利尤单抗注射液」在华递交的第二个上市申请被CDE受理,这距该药首次在国内获批仅三个月左右。
度普利尤单抗(Dupilumab)是利用再生元开创性的Veloclmmune技术开发一款全人源单克隆抗体,由赛诺菲和再生元共同负责。该药通过靶向结合IL-4和IL-13共有受体IL-4Rα亚单位,阻断IL-4和IL-13下游信号转导,缓解由Th2细胞介导为主的疾病,包括特应性皮炎、哮喘、过敏性鼻炎以及食物过敏等。
2017年3月,Dupilumab被FDA批准用于局部治疗药物控制病情不佳的成人中重度特应性皮炎患者,商品名为Dupixent,这使其成为FDA批准的首个治疗特应性皮炎的生物制品。2018年10月,该药又被FDA批准作为一种附加维持疗法,用于治疗年龄在12岁及以上的中度至重度哮喘青少年及成人患者。2019年6月,再次被FDA批准联合其他药物,用于治疗病情控制不足的伴鼻息肉的慢性鼻-鼻窦炎(CRSwNP)成人患者。
此外,Dupilumab还被开发用治疗由2型炎症驱动的其他多种炎症性疾病,比如儿童哮喘(III期临床)、儿童特应性皮炎(III期临床)、青少年特应性皮炎(III期)、嗜酸性粒细胞性食管炎(III期)和慢性阻塞性肺病(III期)。
截止目前,Dupilumab已在包括美国、日本、欧盟约40个国家和地区获得监管机构批准并上市。自上市后,Dupilumab的销售额一路飙升,2017年-2019年销售额分别为2.51亿美元、 9.24 亿美元和 23.13 亿美元。业界非常看好该产品的市场前景,医药市场调研机构EvaluatePharma在2018年6月发文预测,Dupilumab有望在2024年成为继艾伯维修美乐之后的全球第二大畅销抗炎药,销售额达到80.58亿美元。
在国内,度普利尤单抗于2019年5月被纳入《第二批临床急需境外新药名单》,2019年12月上市申请被CDE受理,2020年6月被NMPA批准用于治疗外用处方药控制不佳或不建议使用外用处方药的成人中重度特应性皮炎患者,商品名为达必妥。
9月28日,CDE官网显示度普利尤单抗注射液被纳入优先审评范围,拟定适应症为12岁及以上青少年和成人中重度特应性皮炎。鉴于未公示受理号,笔者猜测此次申报的适应症是12岁以上特应性皮炎患者,不过具体情况有待公司官网披露。

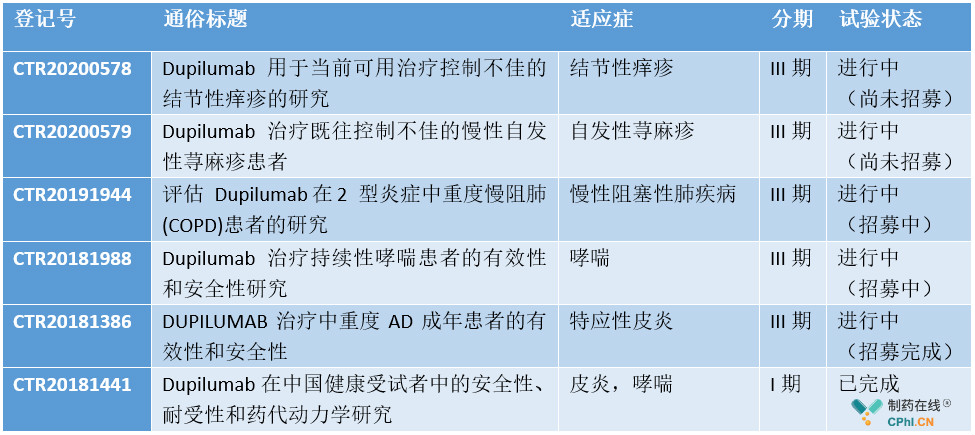
此外,在国内度普利尤单抗还被开发用于治疗其他疾病。据insight数据库,截止目前度普利尤单抗共登记6项临床试验,适应症包括哮喘、慢性阻塞性肺疾病、自发性荨麻疹和结节性痒疹,预计未来该药还将不断有新适应症在国内申报、获批。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57