引言
近日,Lorlatinib 临床Ⅲ期CROWN研究中期分析结果在2020年欧洲肿瘤内科学会(ESMO)虚拟年会上发布。数据显示,相比克唑替尼,第三代间变性淋巴瘤激酶(ALK)酪氨酸激酶抑制剂(TKI)Lorlatinib一线治疗ALK阳性NSCLC能够降低疾病进展或死亡风险达72%(HR=0.28,单侧P<0.001)。
Lorlatinib
Lorlatinib(商品名:LORBRENA®)是一种口服的具有抗ALK和ROS1体外活性的酪氨酸激酶抑制剂(TKI),对ALK、ROS1,以及TYK1、FER、FPS、TRKA、TRKB、TRKC、FAK、FAK2和ACK具有体外抑制活性。
辉瑞先后研发了第一代ALK抑制剂克唑替尼(crizotinib)、第二代ALK抑制剂阿来替尼(alectinib)、塞瑞替尼(ceritinib)、Brigatinib。但是,以上ALK抑制剂对具有获得性耐药突变的患者束手无策。作为第三代ALK抑制剂,lorlatinib能够克服获得性耐药,并且具有较强的穿透血脑屏障的能力,用于晚期ALK阳性NSCLC患者(包括先前ALK TKIs治疗失败的患者)的临床治疗。
2018年11月2日,美国食品药品监督管理局(FDA)批准lorlatinib用于治疗在接受克唑替尼(以及至少其它一种ALK抑制剂)后病情仍进展,或在接受阿来替尼或塞瑞替尼作为第一个ALK抑制剂治疗后病情仍进展的ALK阳性转移性非小细胞肺癌(NSCLC)患者。
CROWN研究

Ⅲ期CROWN研究头对头比较了Lorlatinib和克唑替尼用于未经治疗的ALK阳性NSCLC一线治疗的疗效和安全性。入组患者按1∶1比例随机分配接受Lorlatinib(100mg,QD)或克唑替尼(250mg,BID)治疗。两组患者在疾病进展后不允许交叉治疗。研究的主要终点为盲化独立评审委员会(BICR)评估的PFS。次要终点包括研究者评估的PFS、BICR和研究评估的客观缓解率(ORR)、BICR评估的颅内ORR(IC-ORR)、总生存期(OS)、安全性、生活质量等。
从2017年5月至2019年2月,CROWN研究共纳入296例患者:Lorlatinib组149例,克唑替尼组147例。对BICR评估PFS,Lorlatinib组尚未达到(发生28%的PFS事件),而克唑替尼组为9.3个月(发生59%的PFS事件),Lorlatinib降低疾病进展或死亡风险代72%(HR=0.28,95%CI:0.19~0.41,单侧P<0.001)。亚组分析结果显示,各亚组人群均能够从Lorlatinib治疗中取得PFS的获益。
研究者评估的PFS与BICR评估的PFS数据保持一致,Lorlatinib组和克唑替尼组的中位PFS分别为未达到和9.1个月。在其他次要终点上,BICR评估的ORR,Lorlatinib组和克唑替尼组分别为76%和58%,中位缓解持续时间(DOR),两组分别为未达到和11.0个月。此外,BICR评估显示,相比克唑替尼,Lorlatinib显示出优异的颅内疗效。
整体而言,研究的结果支持Lorlatinib作为一种有效的一线治疗方案用于晚期ALK阳性NSCLC。
Lorlatinib合成工艺一览
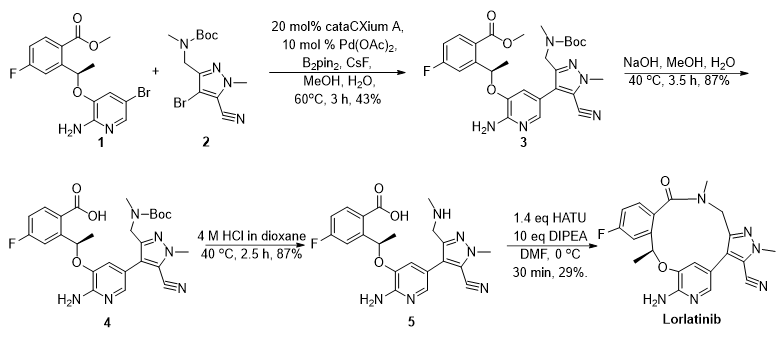
图一:Lorlatinib初始合成路线
如图一所示,初始合成路线能够在实验室内制备5克规模API原料。该路线以溴吡啶1与溴吡唑2为起始原料,经一锅法Suzuki-Miyaura偶联反应,合成中间体3。而后经甲酯水解得到羧酸中间体4,随后Boc基团的脱保护得到中间体5。最终,经HATU大环内酰胺化反应得到目标产物Lorlatinib。为应对紧迫的原料药交付计划,研究人员选择对该路线进行优化。
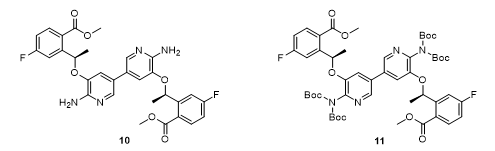
经讨论,初步确定该路线需要解决的五个关键问题:(1)第一步中,形成大量(30%)的化合物1自偶联副产物10;(2)第二步中,在甲酯水解过程中通过腈基的竞争性水解形成酰胺杂质;(3)终产物之前缺乏可用于质量控制的结晶中间体;(4)在大环酰胺化步骤中使用HATU,而在辉瑞内部的安全性评估中不支持规模扩大设施中使用HATU(5)需要进行三次硅胶柱层析色谱纯化。
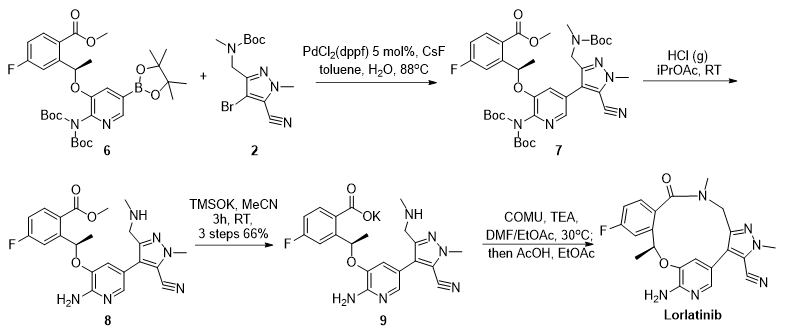
图二:Lorlatinib扩大化生产合成路线
金属钯与起始原料1中的2-氨基吡啶部分具有较强的亲和力,这不仅会影响Suzuki-Miyaura偶联的效率,而且也将给API中重金属残留物的清除带来挑战,因此研究者们选择制备Boc保护后的产物6作为起始原料进行路线优化。这一改变能够将钯催化剂载量减少到3-5mol%,得到boc保护中间体7。但是,在该条件下仍观察到了化合物6自身偶联的副产物11。研究者首先将含有PdCl2(dppf)2和CsF的甲苯/水反应混合物在反应釜中搅拌回流,然后在15小时内将化合物2和6的甲苯溶液缓慢滴加至反应釜中参与反应,从而成功抑制了自身偶联产物11的产生,在大规模生产期间副产物11的形成控制在3%(UPLC面积)以下。为了规避硅胶柱层析色谱法纯化副产物10、11,将中间体7的粗产物在iPrOAc中用HCl(g)进行Boc脱保护,并利用副产物10与中间体8的pKa差异,在不同pH条件下通过水萃取的方法较为方便地清除副产物10。在完成Boc脱保护后,将反应混合物的pH调节至4.5,将所需产物8带入水相,同时将杂质7排入有机相(iPrOAc)。而后将富含产物的水相pH值调节至9 - 10,然后进行萃取后处理,以完全清除10。经计算,上述提取操作中产物8的损失小于2%。随后,中间体8经甲酸酯水解得到中间体9。研究者仔细筛选后发现,三甲基硅酸钾(TMSOK)能够高度化学选择性水解酯基,而保留腈基。此外,产物9能够以钾盐的形式直接从反应混合物中结晶沉淀析出。但需要注意的是,研究者们发现商业化采购的TMSOK中往往含有一定量的KOH,这将导致氰基水解副产物的生成,因此TMSOK的质量控制十分重要。以上三步反应采用叠缩工艺,无需色谱分离,产率为66%。UPLC(210 nm)检测9的纯度大于98%。
对于大环内酰胺化反应,研究者选择使用更加安全高效的肽偶联试剂COMU替代HATU。在14小时内将9的DMF溶液添加到COMU的DMF / THF溶液中。将化合物9的浓度尽量稀释,以最大程度地减少竞争性分子间偶联。反应完成后,经硅胶柱除去COMU副产物N,N-二甲基吗啉-4-羧酰胺。接下来,目标产物从游离碱形式转化为乙酸盐形式,两步收率为46%。通过这些工艺改进,首次大规模交付临床前批次API(438 g)时,路线总收率由原来的10%增加到30%。
观察整条工艺路线,发现大环内酰胺环化步骤的收率较低,因此辉瑞的科学家们进一步筛选了酰胺缩合剂,并确定缩合剂反应速率依次为HATU> COMU> T3P> TPTU≈TSTU。显然,更快的反应速率有助于降低体系的底物浓度,从而降低分子间成酰胺的杂质。因此,有必要重新考虑在扩大化生产工艺中使用HATU的可能性。经Koenen UN 2,BAM Fallhammer UN 3等一系列安全性测试之后,研究者认为,可以选择HATU作为缩合剂进行放大生产。HATU替代COMU参与反应后,能够规避原路线中硅胶柱层析的步骤,将整条路线的收率由30%提升至37%。
CN 109651398 A
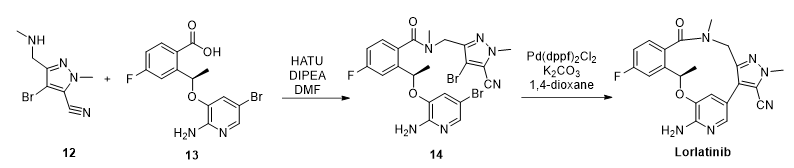
国内有研发公司通过专利CN109651398A报道了一种Lorlatinib的新合成路线。根据报道,该路线以溴吡唑化合物12为起始原料,与羧基中间体13经HATU缩合,得到中间体14。而后,在钯催化剂的作用下,中间体14发生分子内偶联反应,得到目标产物。该专利对最后一步的反应条件表述并不充分。
CN 109651397 A
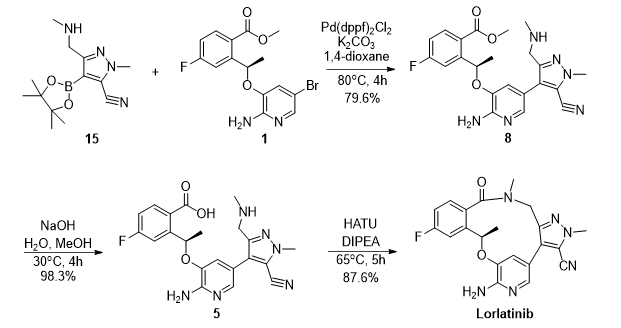
专利CN 109651397 A报道了一种Lorlatinib新的合成路线。该路线首先制备了吡唑硼酸酯15作为反应起始原料,而后经Suzuki偶联,甲酯水解,HATU酰胺缩合得到目标产物。值得注意的是,该专利所报道的分子内酰胺化反应收率远高于原研公司所报道收率,但反应条件并无明显不同。
CN 109232607 A
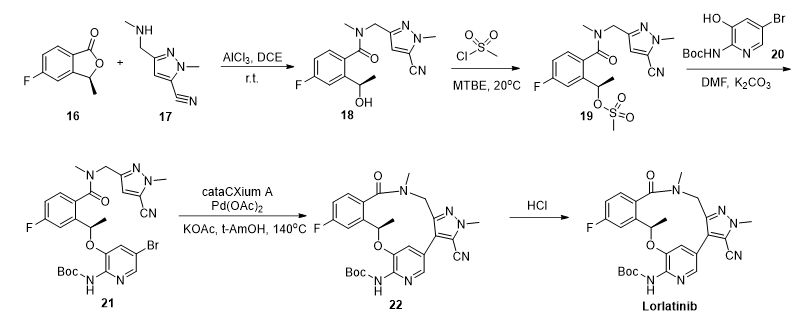
沈阳药科大学有研究团队报道了一条Lorlatinib合成路线。该路线以苯并呋喃酮16为起始原料,经胺解开环得到酰胺化合物18。而后,MsCl与羟基反应,得到中间体19,随后亲核取代得到化合物21。在钯催化剂与磷配体的催化下,经分子内偶联反应得到化合物22。最终,盐酸脱boc得到目标产物。该路线需要用到两个金属催化剂的参与,MsCl属于剧毒品,应用受到管制,且钯催化偶联步骤反应温度较高。因此,该路线仍有改进的空间。
参考文献:
1. Org. Process Res. Dev. 2018, 22, 9, 1289-1293.
2. CN 109651398 A
3. CN 109651397 A
4. CN 109232607 A



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57