2020年11 月 11 日,CDE 官网公示,西安杨森制药有限公司的「达雷妥尤单抗注射液(皮下注射)」(受理号:JXSS200050)新适应症(原发性轻链型淀粉样变)的上市申请拟纳入优先审评。
图1 来自CDE 官网
原发性轻链型淀粉样变(primary light chain amyloidosis ,pAL)是一种多系统受累的单克隆浆细胞病,其临床表现多样化,发病率较低,诊断和治疗都比较困难。pAL是一种由具有反向β折叠结构的单克隆免疫球蛋白轻链沉积在器官组织内,并造成相应器官组织功能异常的系统性疾病。造成肢体水肿和尿中泡沫增多,活动后气短、肢体水肿、腹水、晕厥等限制性心功能不全表现以及肝 脏、周围神经和自主神经、胃肠道、软组织、凝血功能异常等多脏器受累症状。
达雷妥尤单抗是一种靶向CD38的细胞溶解抗体,通过与MM细胞表面的CD38蛋白结合,直接杀死或让免疫系统识别并消灭MM细胞,如:通过补体依赖的细胞毒作用(CDC)、抗体依赖性细胞介导的细胞毒作用(ADCC)和抗体依赖性细胞吞噬作用(ADCP)、以及Fcγ受体等多种免疫相关机制诱导肿瘤细胞凋亡。由杨森开发,其静脉注射液于2015年11月获得FDA批准,商品名为Darzalex。
FDA批准的适应症如下:1、联合硼替佐米、沙利度胺、地塞米松:治疗适合行自体干细胞移植的新诊断的成人多发性骨髓瘤(MM)患者。2、联合来那度胺、地塞米松:①治疗不适合行自体干细胞移植的新诊断的多发性骨髓瘤患者;②经至少一种前线治疗后复发或难治性的MM患者。3、联合硼替佐米、美法仑、泼尼松:治疗不适合行自体干细胞移植的新诊断的MM患者。4、联合泊马度胺、地塞米松:治疗经至少2种前线治疗后疾病进展的MM患者。5、联合硼替佐米、地塞米松:治疗经至少一种前线疗法治疗后疾病进展的MM患者。6、单药:治疗经至少3种前线治疗后疾病的多发性骨髓瘤患者。
NMPA批准的适应症如下:单药治疗复发和难治性多发性骨髓瘤成年患者,包括既往接受过一种蛋白酶体抑制剂和一种免疫调节剂且最后一次治疗时出现疾病进展的患者。剂型/给药途径: 注射剂,静脉注射给药。2019年7月在中国获批进口。2020年5月,杨森开发的达雷妥尤单抗皮下剂型获得FDA批准,商品名为Darzalex Faspro,这是首个皮下注射的anti-CD38单抗,用于治疗多发性骨髓瘤。
达雷妥尤单抗从三/四线用药,到二线用药,到现在一线用药,已是强生肿瘤业务中一款核心产品。2018 年,Darzalex 全年销售收入 20.25 亿美元,同比大增+63%;2019 年,其销售额为 29.98 亿美元,同比增长+48%。
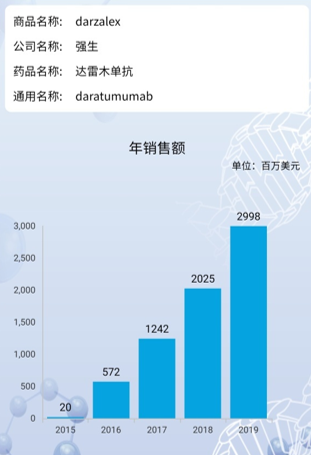
图2 MEDICINE数据库



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57