
ADC进入黄金期
一百年多前,德国免疫学家保罗·欧立希(Paul Ehrlich)最早提出单克隆抗体的"黄金子 弹"学说,即:利用单克隆抗体对抗原的特异性结合实现对癌变细胞的靶向治疗。随着基因工程抗体制备技术的成熟,以及新型化学连接技术的出现,抗体偶联药物的概念逐渐变为现实。2000年,第一个ADCs药物Mylotarg经FDA批准上市用于治疗急性髓系白血病。
2019年-2020年,ADC迎来了大爆发,FDA一连批准了5款药物上市,尤其是阿斯利康斥资69亿美元从第一三共引进的Her2-ADC药物Enhertu从递交上市申请到获批仅用了不到3个月的时间。至此,全球已有10款ADC药物获得FDA批准上市。
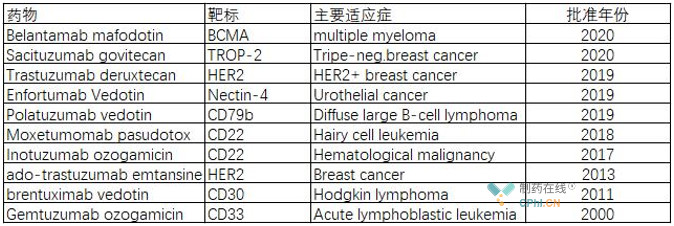
ADC的不俗表现
随着ADC药物的不断上市,ADC药物市场发展进入加速爆发期。Adecetris 是由 西雅图遗传学开发的 ADC 药物,治疗血液肿瘤开创了新的一线疗法是目前最成功的ADC药物之一,2011年上市以来到2020年药品累计销售额达到20亿美元。由罗氏/ImmunoGen共同开发的Kadcyla也表现不俗,2019年全球销售额高达14.25亿美元,成为名副其实的"重磅炸 弹"药物。中国也在2020年1月21日批准了Kadcyla,中国市场由此也迎来首个抗体偶联药物。
资本市场的强力追捧
ADC的高光表现引来了资本市场的强力追捧,各大跨国制药巨头纷纷入场布局。今年9月,两家药企完成了两项重磅交易,均涉及ADC药物领域。一项是吉利德以210亿美元收购以肿瘤学为重点的Immunomedics;另一项则是默沙东以45亿美元与Seattle Genetics达成两项战略合作。吉利德的此次收购,就是为了获得靶向Trop-2的ADC药物Trodelvy。加上去年阿斯利康69亿美元引进Enhertu,ADC近两年出尽了风头。
国内各个制药公司也纷纷入场,握有国内第一个进入临床的ADC药物的荣昌生物11月9日一上市便收到了资本的热烈追捧。其它公司也纷纷布局,10月29日,基石药业宣布以1000万美元预付款+3.535亿美元里程碑金额引进一款ROR1靶向的ADC药物。2019年4月,云顶新耀以8.35亿美元总金额引进Immunomedics的Trop2靶向ADC药物Trodelvy;2019年12月,君实生物以3000万元人民币预付款+2.7亿元人民币里程碑金额引进多禧生物的Trop2靶向ADC药物; 2020年10月,华东医药以4000万美元预付款+2.65亿美元里程碑金额引进ImmunoGen的FRα靶向ADC药物Mirvetuximab Soravtansine。
ADC的技术突破
目前在临床开发或临床应用中的许多ADC,都是基于一种完全内化的IgG形式,以极高过表达的抗原为靶点,并使用随机生物结合技术与微管蛋白聚合抑制剂偶联。已知可裂解连接体在胞浆循环过程中不稳定,而这种疏水性连接体具有较高的聚集倾向。然而,基于完整IgG的ADC在富含基质的肿瘤中可能会有肿瘤渗透的问题,并且被新生Fc受体(FcRn)回收,可能导致内皮和肝 脏中的不利分布,从而导致不良反应。此外, ADCs的有效性还取决于抗原在细胞表面的丰度,还有包括Kadcyla®在内的ADC通过多种机制诱导肿瘤耐药。
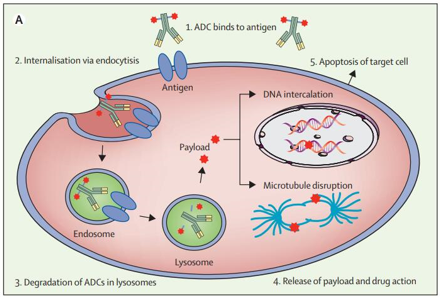
图片来源参考文献2
随着ADC技术的不断进步,人们开发出多种方法来克服前2代ADC的固有缺陷。首先区域特异性生物结合方法得到广泛发展,通过区域特异性生物偶联产生更均匀和更稳定的ADC;其次,新的细胞毒 药物已经被开发出来,以靶向低抗原表达或对auristatins或maytansinoids耐药的癌细胞;新的靶标和相关释放系统也被开发出来,在这种策略中,细胞外蛋白酶和细胞外基质的其他成分(如酸性介质或还原性谷胱甘肽)可用于有效的细胞外释放用于非内化ADC的细胞**;最后,更多的ADC形式有助于加强ADC对肿瘤的穿透和减少靶外**。
新兴的第三代ADC已崭露头角,Enhertu®和Trodelvy®是其中的典范。Sacituzumab-govitecan(IMMU-132)是一种抗TROP-2单抗,通过具有短聚乙二醇化单元的可裂解马来酰亚胺连接体与SN-38(伊立替康的活性代谢物)偶联。FDA于2020年4月批准,这一成就令人印象深刻,因为这种ADC用于难治或耐药的三阴性乳腺癌(TNBC),之前没有有效的治疗药物。这种ADC的另一个有趣的特点是:包括聚乙二醇化单元的连接结构的优化使得该ADC的DAR高达7.6,而不会影响其耐受性或效率。DAR=4长期以来被认为是最佳的,但这一说法现在只适用于已知认可的ADC,其有效载荷为DM1或MMAE的第二代接头。

图片来源参考文献1
同样,为了使伊立替康衍生物与精心设计的连接体结合,日本第一三共公司开发了DXd(exatecan或DX-8951)。DXd是一种比SN-38体外对癌细胞活性高10倍的细胞**剂。DXd具有更好的安全性和最佳的溶解度,能够引起旁观者杀伤效应杀死邻近的癌细胞,这在异质性肿瘤中是一个优势,但半衰期短,可避免靶外**。通过对蛋白水解敏感的马来酰亚胺连接体将DXd生物结合到抗HER2曲妥珠单抗半胱氨酸残基上,使得获得均匀DAR为7.7的共轭fam-trastuzumab-deruxtecan nxki(DS-8201a)。尽管DAR很高,但第一三共的DS-8201a在大鼠和猴子中的耐受性非常好,并且在血浆中非常稳定。
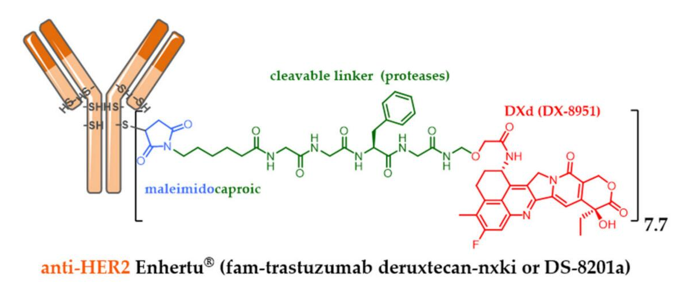
图片来源参考文献1
DS-8201a能够在体内有效地将DXd输送到异质性肿瘤中,并显示出很高的治疗效果。去年,在转移性HER2阳性乳腺癌的III期临床研究中,DS-8201a成功地与T-DM1进行了比较,并最终于2019年12月底获得FDA批准。
ADC研发进入快车道
技术的突破使ADC药物的研发进入了发展的快车道,更多的制药公司参与到了ADC的药物开发中。ADC药物主要聚焦肿瘤领域,临床I期之后的管线中,88.3%的项目集中在肿瘤领域,其次是免疫领域,占比 5.3%。截至 2020 年第一季度,全球处于活跃状态的 ADC 研发药物共 302 个。临床二期和三期的研发管线有33个。
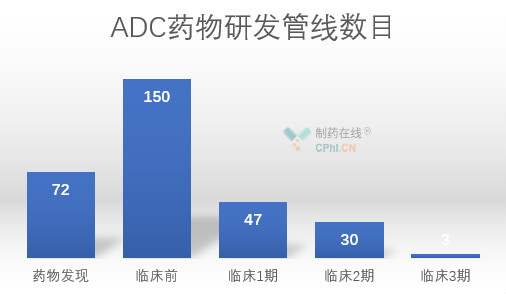
数据来源:Cortellis、财通证券研究所
国内临床开发进度最快的ADC是百奥泰的BAT8001项目(III期)、荣昌生物的RC48-ADC(II期)、科伦药业的A166(I/II期);恒瑞医药、东曜药业、浙江医药、特瑞斯等企业10余个项目正处于I期临床阶段。
展望
ADC药物从概念提出到第一款药物上市经历了一百多年的历程,随着ADC药物技术的进一步成熟,ADC历经风雨之后终于迎来了盛世华年。大批制药企业和资金蜂拥而入,可以预见,未来会有更多的ADC药物获批上市。另外,在中国政府鼓励创新和加快临床亟需药品进入中国的政策环境下,ADC药物在中国的可及性会明显增高,这些药物的到来,将为中国的癌症患者,尤其是晚期恶性肿瘤患者带来新的选择。
参考文献:
1. Antibody-Drug Conjugates: The Last Decade. Pharmaceuticals 2020, 13, 245.
2. Antibody-drug conjugates for cancer. Lancet. 2019 Aug 31;394(10200):793-804.
3. 财通证券-抗体偶联药物(ADC)专题报告
4. 各公司官网
作者简介:小药说药,本人姓药,本科学医,博士毕业于上海交通大学分子生物学专业,转而从事医药行业研发工作近10年,闲暇之余爱好写作,在微信公众号”小药说药“与大家一起分享医药行业前沿和知识,一起成长,共同进步!



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57