近期,恒瑞医药官方发布消息,氟唑帕利胶囊获得美国FDA国际多中心临床试验资格,批准开展《氟唑帕利胶囊联合醋酸阿比特龙片和泼尼松片(AA-P)对比安慰剂联合AA-P一线治疗转移性去势抵抗性前列腺癌患者的多中心、随机、双盲、安慰剂对照的III期临床研究》。目前,该临床试验已在中国、美国获批开展,后续计划在澳洲、欧洲、韩国、中国台湾等国家及地区申请开展国际多中心临床试验。
根据世界卫生组织国际癌症研究机构(IARC)近期发布的《2020全球癌症报告》数据显示,2020年全球前列腺癌新发病例数141万,成为全球第四大癌症;新增死亡病例数37万,位居全球恶性肿瘤死亡数第八位。根据国家癌症中心《2015年中国恶性肿瘤流行情况分析》显示,男性前列腺癌近年来的上升趋势明显,已位居男性发病第六位(全国发病人数达7.2万人),新增死亡病例数位居男性死亡第十位;分析还特别指出在未来的肿瘤防控中应当重点关注前列腺癌。
我国大多数前列腺癌患者在初诊时就已经出现转移,据不完全统计国内新诊断的前列腺癌患者中,54%的患者在诊断时已发生远处转移(包括骨和腹部器官转移)。发生远处转移的患者,5年相对生存率从未转移患者的80%降至30%,无进展生存时间是未转移患者的一半。前列腺癌细胞的生长具有雄激素依赖性,因此雄激素剥夺治疗(ADT)是前列腺癌的基础治疗手段。转移性激素敏感性前列腺癌(指对ADT有疗效应答的转移性前列腺癌)经过持续的ADT后依然会进展,最终转变为转移性去势抵抗性前列腺癌(mCRPC)。患者一旦进入mCRPC阶段,预后一般较差。

mCRPC系统治疗-NCCN指南
mCRPC的标准一线治疗方案包括醋酸阿比特龙片和泼尼松片(AA-P)、多西他赛以及二代新型抗雄药物恩扎卢胺。多西他赛是治疗前列腺癌的重要化疗药物,但由于前列腺癌患者多为老年患者,身体状态差以致难以承受多西他赛较大的化疗**,故临床上多做二线或三线使用。阿比特龙通过抑制17-α雄羟化酶/C17,20-裂解酶(CYP17)从而全面阻断睾丸、肾上腺和前列腺肿瘤组织的睾酮合成,具有显著的抗CRPC疗效;2015年自强生原研阿比特龙Zytiga获中国国家药监局(NMPA)批准上市进入中国市场,后续恒瑞医药、正大天晴、江西青峰及齐鲁制药的阿比特龙仿制药也相继获批上市,在医保谈判、国家集采的影响下,阿比特龙价格呈瀑布式下降,同时也迎来了市场大爆发,销量冲击8亿,占据前列腺癌的主要市场。二代新型抗雄药物恩扎卢胺于2019年11月获得NMPA批准,用于ADT失败后无症状或有轻微症状且未接受化疗的转移性去势抵抗性前列腺癌成年患者的治疗,由于上市时间短,在临床尚未被广泛使用。
多聚ADP-核糖聚合酶(PARP),最主要的功能是参与DNA单链断裂损伤修复过程。当DNA发生单链断裂损伤时,PARP及时感应到DNA断裂,自动识别并结合到断裂部位,同时催化NAD+(烟酰胺腺嘌呤二核苷酸)形成PARP-聚ADP核糖支链;随后吸引DNA修复蛋白结合到损伤部位进行DNA修复。PARP抑制剂可以竞争性结合到PARP酶上,直接抑制PARP酶参与的DNA单链损伤修复过程;同时当PARP抑制剂结合到PARP酶上之后,会导致与受损DNA结合的PARP-1和PARP-2被困在DNA链上(PARP抑制剂的"捕获"效应),直接造成其他的DNA修复蛋白也无法结合,从而DNA断裂不仅不能被修复,而且还从单链断裂变成双链断裂,双链断裂最终会导致细胞死亡。DNA双链断裂修复方式主要为同源重组修复(HRR),该修复方式具有高保真特性,参与蛋白非常之多例如BRCA、ATM、RAD51等等。如果肿瘤细胞本身存在DNA修复基因缺陷,尤其是同源重组修复相关基因缺陷,会使肿瘤细胞DNA损伤修复功能受到限制而无法修复因PARP抑制剂竞争性结合PARP酶而造成的DNA损伤,从而达到杀伤肿瘤细胞的作用,也被称为是PARP抑制剂的合成致死作用机制。
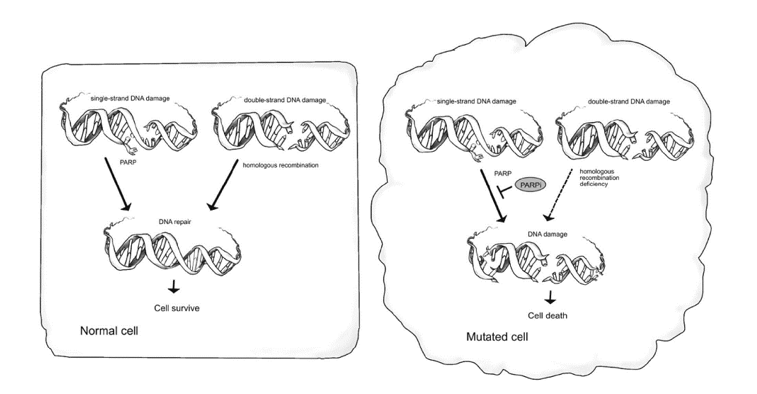
PAPR抑制剂合成致死作用机制
基于合成致死作用机制的显著疗效,PARP抑制剂已在多个癌种获批适应症。目前FDA已批准4款PARP抑制剂,包括奥拉帕利(Olaparib,阿斯利康,2014 FDA获批,2018国内获批),尼拉帕利(Niraparib,GSK,2017 FDA获批,2019国内获批),卢卡帕利(Rucaparib,ClovisOncology,2016 FDA获批),他拉唑帕利(Talazoparib,辉瑞,2018 FDA获批),主要适应症覆盖卵巢癌、乳腺癌、胰 腺癌、前列腺癌,目前针对肾细胞癌、胃癌、肺癌等多个癌种的临床研究也在进行中。2020年12月,国产首 个PARP抑制剂恒瑞医药的氟唑帕利胶囊(商品名:艾瑞颐)获批上市,用于既往经过二线及以上化疗的伴有胚系BRCA突变(gBRCAm)的铂敏感复发性卵巢癌、输卵管癌或原发性腹膜癌患者的治疗。该适应症的获批是基于一项由中国医学科学院肿瘤医院吴令英教授担任主要研究者,全国26家研究机构共同参与的氟唑帕利治疗BRCA1/2突变的复发性卵巢癌的单臂、多中心Ⅰb期临床研究,研究结果近期已于国际著名医学期刊《临床癌症研究》(Clin Cancer Res)上在线全文发表。该研究评估了氟唑帕利单药在BRCA1/2突变的复发性卵巢癌中的疗效和安全性,在113例疗效可评估的患者中,客观缓解率(ORR)高达69.9%,中位缓解时间(mDoR)长达10.2个月,中位无进展生存期(mPFS)长达12.0个月,疗效显著。同时,氟唑帕利也显示出良好的安全性,血液学**与同类产品相当,3级胃肠道反应较同类药发生率更低。
PARP抑制剂前列腺癌获批情况
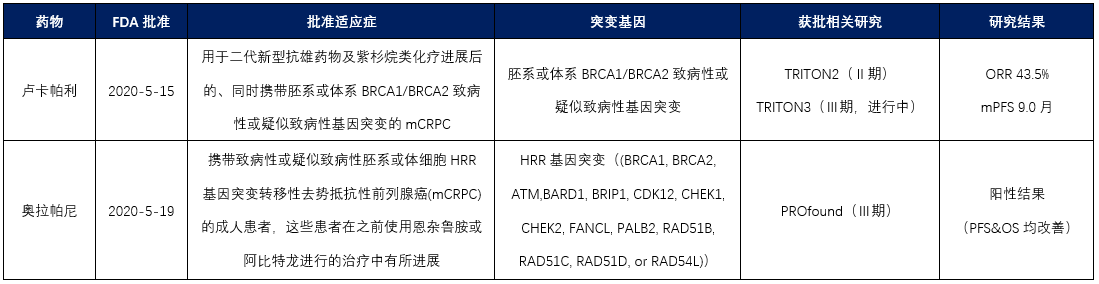
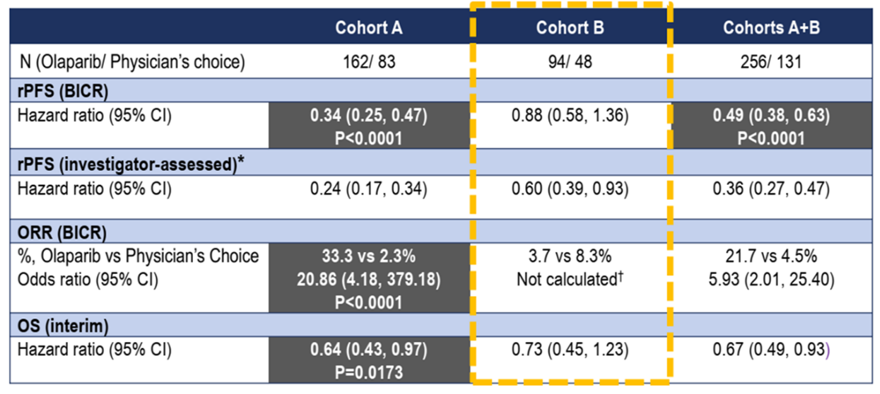
mCRPC患者中约20%~30%的患者发生同源重组修复(HRR)基因突变,最常见的突变基因为BRCA1/BRCA2和ATM,因此各药企也均在前列腺癌领域开展了多项PARP抑制剂研究。目前已有两款PARP抑制剂药物获得FDA批准用于前列腺癌治疗。2020年5月,FDA有条件快速批准(Accelerated Approval)卢卡帕利用于二代新型抗雄药物及紫杉烷类化疗进展后的、同时携带胚系或体系BRCA1/BRCA2致病性或疑似致病性基因突变的mCRPC。该适应症的获批是基于TRITON2(NCT02952534),一项开放、单臂的Ⅱ期临床研究,显著的ORR(43.5% ,95% CI, 31.0%-56.7%)及mPFS(9.0月,95% CI, 8.3月-13.5月)结果。该适应症的完全批准(Full Approval)将有赖于卢卡帕利TRITON3(NCT02975934)研究的结果。TRITON3是一项多中心、随机、开放Ⅲ期临床研究,旨在评价卢卡帕利单药对比研究者选择的治疗方案(阿比特龙、恩扎卢胺或多西他赛)治疗既往接受过新型抗雄药物但没接受过化疗、且同时携带胚系或体系BRCA1/ BRCA2或ATM基因突变的mCRPC的疗效与安全性,主要终点为PFS,该研究正在进行中尚未出结果。仅4天后,FDA再次宣布批准奥拉帕利用于恩扎卢胺或阿比特龙治疗进展后的、同时携带胚系或体系同源重组修复(HRR)致病性或疑似致病性基因突变的mCRPC。值得注意的是,该适应症将获批人群扩大至14种HRR基因突变类型,包括BRCA1, BRCA2, ATM, BARD1, BRIP1, CDK12, CHEK1, CHEK2, FANCL, PALB2, RAD51B, RAD51C, RAD51D, 或RAD54L。该适应症的获批是基于PROfound研究阳性试验结果。PROfound是一项多中心、开放、随机、对照Ⅲ期临床研究,旨在评价奥拉帕利单药对比研究者选择的治疗方案(阿比特龙或恩扎卢胺)治疗既往接受过新型抗雄药物且至多一线紫杉烷类化疗、且同时携带指定HRR基因突变mCRPC。该研究根据基因突变类型,将受试者分为队列A(BRCA1/2或ATM突变)和队列B(至少携带其他12个指定基因中的一个突变),主要研究终点为第三方独立影像中心(IRC)评估的队列A的mPFS。研究结果表明队列A中奥拉帕利单药mPFS显著优于对照组(7.4月vs 3.6月,HR, 0.34; 95% CI, 0.25-0.47; P <0.001),队列A+B中奥拉帕利单药mPFS也显著优于对照组(5.8月vs 3.5月,HR, 0.49; 95% CI, 0.38-0.63; P <0.001)。同时OS数据也显示出优势,队列A中奥拉帕利单药mOS优于对照组(19.1月vs 14.7月,HR, 0.69; 95%CI, 0.50-0.97; P =0.0175),队列A+B中奥拉帕利单药mOS也优于对照组(17.5月vs 14.3月,HR, 0.67)。
PROfound研究有效性数据汇总
笔者在中国药物临床试验登记与信息公示平台查询到关于氟唑帕利共有34条记录,覆盖卵巢癌、乳腺癌、胰 腺癌、前列腺癌、小细胞肺癌及胃癌领域,可以看出恒瑞医药对此产品的广泛布局和重视程度。其中正在进行的Ⅲ期临床研究共有5项,包括卵巢癌2项,乳腺癌1项,胰 腺癌1项,以及近期已获得美国及中国临床试验资格的前列腺癌1项(SHR3162-III-305)。根据已公开信息,笔者大致推断该研究设计:该研究旨在评价氟唑帕利联合AA-P对比安慰剂联合AA-P一线治疗mCRPC的疗效和安全性,样本量预计804例,研究将分为两个队列,队列1为不考虑DNA损伤修复缺陷状态(deoxyribonucleic acid DNA damage repair deficiencies,DRD),队列2为DRD阳性;主要研究终点包括评价队列1的PFS和队列2的PFS。笔者还观察到恒瑞医药同时在开展氟唑帕利联合醋酸阿比特龙在mCRPC中的药代动力学和安全性I期研究(NCT04108247,首次公示时间2020-02-12),笔者猜测此I期研究结果是申请该Ⅲ期研究最重要的支持依据。该Ⅲ3期研究通过将PARP抑制剂与一线抗雄药物阿比特龙联用,将目标人群扩展到不再考虑基因突变类型的mCRPC,结果非常值得期待。
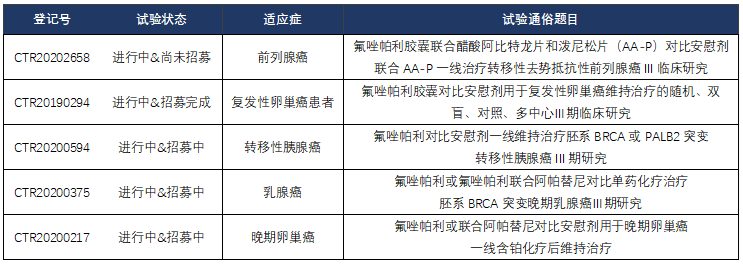
氟唑帕利正在进行中相关III期临床研究
已有临床前及临床研究表明同时靶向AR和DNA修复途径,可能增加协同作用并提高疗效。临床前研究表明,奥拉帕利与AR拮抗剂之间存在协同作用,而无需考虑HRR突变状态。正基于此协同作用发现,奥拉帕利开展了一项随机、双盲、安慰剂对照、多中心Ⅱ期临床研究(NCT01972217),旨在评价在不考虑HRR突变状态下,奥拉帕利联合阿比特龙对比安慰剂联合阿比特龙治疗既往多西他赛化疗失败的mCRPC的有效性与安全性,主要研究终点为mPFS。2018年6月研究公布结果,显示奥拉帕利联合阿比特龙的mPFS优于安慰剂联合阿比特龙(13.8月vs 8.2月,HR 0·65, 95% CI 0·44-0·97,p=0·034)。在安全性方面,奥拉帕利联合阿比特龙出现更多的药物不良反应事件,3级及以上AE为54% vs 28%,常见的包括贫血(21% vs 0%)、肺炎(6% vs 4%)、心肌梗塞(6% vs 0%),但总体安全性可耐受。该Ⅱ期临床研究结果进一步证实PARP抑制剂联合AR拮抗剂治疗mCRPC具有协同作用,同时显示该联合方案对不考虑HRR突变状态的所有患者均可带来临床获益。目前除了恒瑞医药此次批准的该项III期临床研究外,还有3项PARP抑制剂联合AR拮抗剂治疗mCRPC的III期临床研究正在开展。
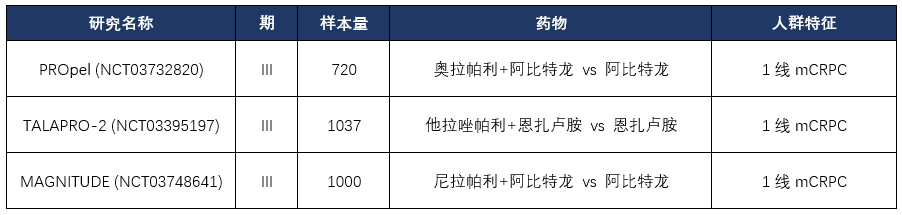
PARP抑制剂联合AR拮抗剂治疗mCRPC的III期临床研究
引文:
1. https://mp.weixin.qq.com/s/4hR0Qp1VqQcEZYhR_1-dqQ
2. 前列腺癌NCCN指南2020 V3版
3. FDA官网
4. PROfound III期研究ESMO结果
5. https://clinicaltrials.gov/
6. http://www.chinadrugtrials.org.cn/
7. PARP inhibitors as a new therapeutic option in metastatic prostate cancer: a systematic review
8. Olaparib combined with abiraterone in patients with metastatic castration-resistant prostate cancer: a randomised, double-blind, placebo-controlled, phase 2 trial



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57