
3月17日,Apellis Pharmaceuticals和Swedish Orphan Biovitrum AB(Sobi)宣布pegcetacoplan和eculizumab头对头治疗成人阵发性睡眠性血红蛋白尿症(PNH)的三期研究PEGASUS结果已在《新英格兰医学杂志》发表。结果显示,pegcetacoplan在改善血红白蛋水平和关键临床结果上优于eculizumab。
阵发性睡眠性血红蛋白尿症(PNH)是一种慢性、威胁生命的罕见血液疾病,由造血干细胞基因突变导致红细胞膜缺陷性而诱发的一种后天获得性溶血性疾病,临床表现为与睡眠有关、间歇发作的慢性血管内溶血、血红蛋白尿等。据统计,全球大约有15000名PNH患者,男性发病率高于女性,主要在20~40岁发病。
PNH患者若不接受有效治疗,五年病死率约达35%,中位生存时间仅为10-15年。此前,PNH的治疗以输血、大剂量糖皮质激素冲击、骨髓移植等非特异性治疗为主,直到2007年Alexion公补体C5单克隆抗体Eculizumab(Soliris)获批问世,PNH患者才迎来首 款特异性治疗药物。随着Soliris专利的到期,Alexion公司又于2018年推出了第2款补体C5单克隆抗体Ultomiris(Ravulizumab)。其实Ultomiris是Soliris的升级版产品,仅需每2月注射一次,而Soliris需每2周注射一次。此外,这两款药物目前获批的适应症也不完全相同,除了PNH,Soliris还被批准用于治疗非典型溶血性尿毒症综合征(aHUS),全身性重肌无力(gMG)以及成人视神经脊髓炎,而Ultomiris还批准用于治疗aHUS。
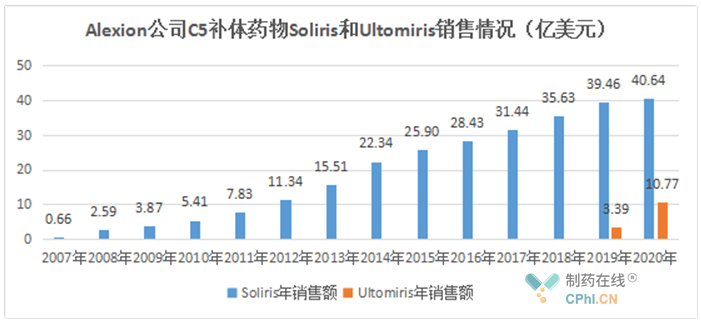
凭借先发优势,Soliris已成为Alexion公司的重磅产品,2020年销售额高达40.64亿美元。而Ultomiris凭借长效优势,上市第二年就成为销售额超过10亿美元的重磅产品。此外,值得一提的是,2020年12月阿斯利康以390亿美元的价格与Alexion达成收购协议,创2020年医药领域收购案交易金额之最。而此次收购案的背后,笔者认为阿斯利康如此大手笔,除了为补充其罕见病产品线,可能更是看中Alexion在补体生物学领域的领导地位。
Pegcetacoplan(APL-2)是Apellis公司开发的一款补体C3抑制剂,是与聚乙二醇聚合物偶联的合成环状肽,可以特异性结合C3和C3b旨在调节许多疾病中过度的补体激活(C3是C5的上游信号分子)。目前该药治疗PNH的NDA和MAA正在美国和欧盟进行审查,其中FDA指定的PDUF日期为2021年5月14日。2020年11月,Apellis与Sobi达成协议,共同开发该药的开发许可权。据协议,Sobi将向Apellis支付2.5亿美元预付款、8000万美元开发费用以及高达9.15亿美元的其它注册和商业里程碑付款。
Pegcetacoplan的NDA和MAA正是基于三期研究PEGASUS的积极结果。该研究旨在评估pegcetacoplan与Soliris(eculizumab)相比治疗成人PNH患者的疗效和安全性差异,共入组80例PNH患者,这些患者在入组前必须先经eculizumab治疗并达到病情稳定3个月以上,基线血红蛋白水平<10.5g/dL。
研究中,前4周导入期内,患者接受每周2次的pegcetacoplan 1080mg以和之前剂量的eculizumab。随后16周的随机、对照治疗期内,患者随机化分组,分别接受每周2次的pegcetacoplan 1080mg或之前剂量的eculizumab。
结果显示:与eculizumab相比,pegcetacoplan显著改善患者的平均血红蛋白水平,达到研究主要终点。治疗16周后,接受pegcetacoplan治疗患者的平均血红蛋白水平较eculizumab对照组中患者改善了3.8g/dL。关键次要终点上,治疗第16周,pegcetacoplan治疗组85%的患者无输血,而Soliris治疗组这一比例为15%,而且pegcetacoplan治疗组中患者在慢性疾病疗法功能评估(FACIT)-疲劳评估量表得分方面也有较好的表现。
安全性方面:pegcetacoplan与eculizumab两组发生严重不良事件(SAEs)的比例分别为17.1%和15.4%,不过未见脑膜炎和死亡病例报道。16周随机试验中最常见的不良事件包括注射部位反应(36.6% vs 2.6%)、腹泻(22.0% vs 0%)、头痛(7.3% vs 20.5%)、疲劳(4.9% vs 15.4%)。此外,这两组溶血不良事件的发生率分别为9.8%(4/41)和23.1%(9/39)。
Pegcetacoplan是首 款、也是唯一一款在平均血红蛋白水平上显示优于eculizumab的在研药物,预计有望成为PNH临床护理新标准。此外,pegcetacoplan还被开发用于治疗地图样萎缩(GA)、C3肾小球病等疾病。
关于补体及其抑制剂
补体是一种血清蛋白质,主要介导免疫应答和炎症反应,能够被抗原-抗体复合物或微生物所激活,进而导致病原微生物裂解或被吞噬。补体系统不仅是机体发挥天然免疫防御的重要效应机制,也是主要的体液免疫效应机制之一。但补体异常过度激活时可造成组织器官损伤,引起PNH(阵发性睡眠性血红蛋白尿症)、不典型溶血尿毒症(aHUS)、C3肾小球病、老年黄斑变性(AMD)等多种疾病。
研究表明:补体系统的活化主要通过经典途径(Classical pathway)、旁路途径(Alternative pathway)和凝集素途径(Lectin pathway)这3条既相对独立又相互联系的途径。而三条途径产生的C5转化酶,均可裂解C5,引发共同终末效应,进而发挥调理吞噬、裂解细胞、介导炎症、免疫调节和清除免疫复合物等多种生物学效应。
目前,靶向这三条路径相关靶点的药物开发均已经成功转化。其中,C5补体抑制剂,除了上述提到的Soliri和Ultomiris,还有多款在研药物,如Akari公司的nomacopan(以前称为Coversin)、VERIC bio公司的Zimura(avacincaptad pegol)和RaPharmaceuticals开发新型大环肽类zilucoplan,其中nomacopan治疗PNH的III期研究CAPSTONE在今年初达到主要终点,Zimura在今年4月份被FDA授予治疗干性老年黄斑变性(AMD)相关地理萎缩(GA)的快速通道资格,而zilucoplan曾被FDA授予治疗重症肌无力(gMG)孤儿药资格。
此外,目前还未有靶向补体C3、C1和MASP-2(甘露聚糖结合凝集素相关丝氨酸蛋白酶-2)的药物获批,其中进展较快的有Apellis的APL-2(pegcetacoplan,靶向C3)、赛诺菲的sutimlimab(靶向C1)和Omeros的Narsoplimab(OMS721)(靶向MASP-2)。Sutimlimab治疗原发性冷凝集素病(CAD)的生物制品许可申请上月被FDA拒批。Narsoplimab是首 个阻断补体凝集素途径的抗体药物,曾被FDA授予治疗造血干细胞移植相关血栓性微血管病(HSCT-TMA)的突破性 药物资格和孤儿药物资格,近日已递交生物制品许可申请。
参考资料:
[1] https://www.novartis.com/news/media-releases/novartis-investigational-oral-therapy-iptacopan-lnp023-receives-fda-breakthrough-therapy-designation-pnh-and-rare-pediatric-disease-designation-c3g
[2] https://www.medsci.cn/article/show_article.do?id=27191915382c
[3] http://www.rrrry.com/art_49901.htm
[4] https://zhuanlan.zhihu.com/p/337312734
[5] https://www.firstwordpharma.com/node/1810685?tsid=1



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57