2021年3月29日,上海璎黎药业有限公司(简称:璎黎药业)宣布其自主研发的新药Linperlisib(YY-20394)用于治疗复发/难治滤泡性淋巴瘤(r/r FL)2期注册临床试验初步完成。试验结果表明,针对意向治疗人群,Linperlisib在有效性和安全性方面均取得了统计和临床意义的提高。
Linperlisib是璎黎药业开发的一种口服PI3Kδ抑制剂。临床前研究显示,linperlisib可通过抑制PI3Kδ蛋白的表达,降低AKT蛋白磷酸化水平,从而诱导细胞凋亡,抑制恶性B细胞及原发肿瘤细胞的增殖。在中国,linperlisib治疗复发和/或难治滤泡性淋巴瘤的申请已于2020年9月被纳入突破性治疗品种。值得一提的是,2021年2月,恒瑞医药已与璎黎药业达成合作,获得了该药在大中华地区的联合开发权益以及排他性独家商业化权益。
本次公布的是一项单臂、开放、多中心2期临床试验(YY-20394-002),旨在评估linperlisib治疗复发和/或难治滤泡性淋巴瘤患者的有效性和安全性,主要研究终点是由独立数据评估委员会(IRC)评估的总缓解率。在长达二年多的试验中,共纳入93例接受过二线或二线以上全身系统治疗后进展(曾接受过美罗华和至少一个烷化剂治疗)的复发和/或难治滤泡性淋巴瘤患者。
2期注册临床数据显示,linperlisib在复发/难治滤泡性淋巴瘤受试者中表现出显著的临床益处:在89例可评估的复发/难治滤泡性淋巴瘤的患者中,linperlisib达到了80%以上的客观缓解率,以及95%以上的疾病控制率,且口服给药安全可控,耐受性好。
目前linperlisib正在中国和全球范围内开展10项临床试验。除了单药治疗研究,璎黎药业也在探索linperlisib与其他抗肿瘤药物进行联合的方式,如linperlisib联合GEMOX治疗复发/难治弥漫大B细胞性淋巴瘤患者等。
关于 PI3K抑制剂
PI3K全称为磷脂酰肌醇-3-激酶,于上世纪八十年代被科学家发现。由于其在癌症发生和进展中起的重要作用,已成为研究人员开发癌症靶向药的热门靶点之一。
PI3K由三个亚基组成。根据其不同的结构和特定的底物,PI3K分为3类:I类、II类和III类。I类PI3K是与人类癌症最相关的类型,包括PI3Kα、PI3Kβ、PI3Kδ、PI3Kγ四个亚型。II类PI3K和III类PI3K主要控制膜运输,间接调节信号转导。其中,II类PI3K成员包括PI3KC2α、PI3KC2β和PI3KC2γ三个亚型,III类PI3K由催化亚基V ps34和调节亚基 V ps15组成。
全球范围内已获批上市的PI3K抑制剂
PI3K几乎介导50%恶性肿瘤的发生。其信号通路的过度活跃与肿瘤的进展、肿瘤微血管密度的增加、癌细胞的趋化性和侵袭性增强有显著的相关性。目前全球总共批准5款PI3K抑制剂,即吉利德的idelalisib(Zydelig)、拜耳的Copanlisib(Aliqopa)、Verastem公司的duvelisib(Copiktra)、诺华的alpelisib(BYL719,Piqray)和TG Therapeutics的Umbralisib(Ukoniq)。其中,拜耳Copanlisib在中国提交的上市申请已纳入优先审评,有望于近期在中国上市。
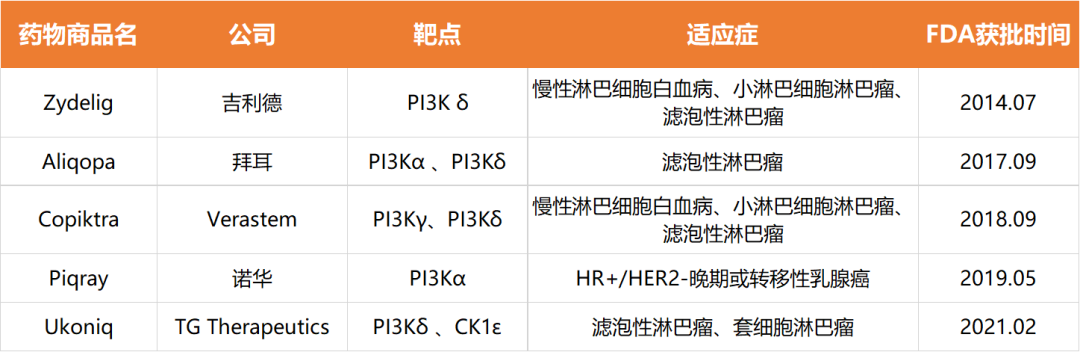
(根据公开资料整理)
国内PI3K抑制剂研发布局
在中国,尚无PI3K抑制剂获批上市,但企业已通过外部引进和自主研发的方式积极投身到这一领域的研发之中,十多款PI3K抑制剂在研药已迈入到临床阶段。
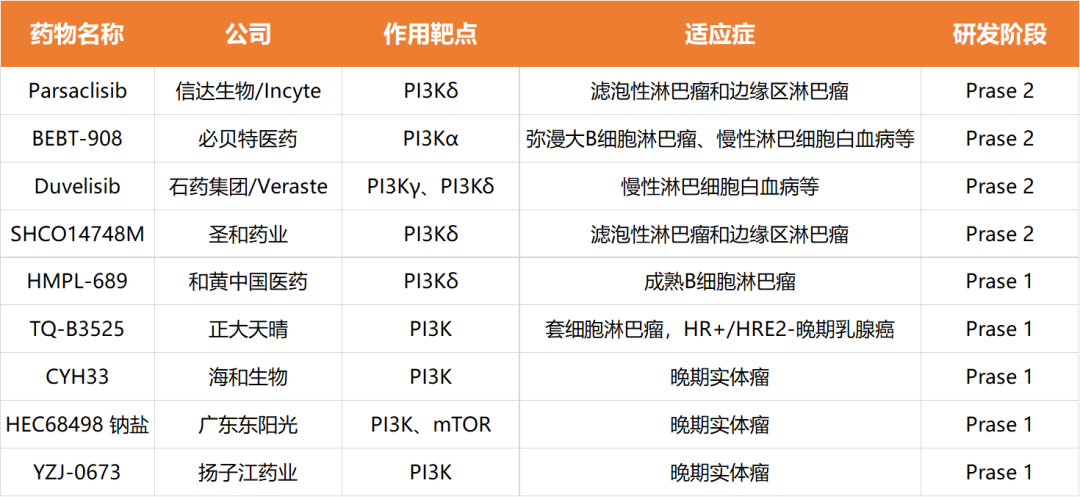
(根据公开资料整理)
值得一提的是,2021年3月31日,信达宣布,其旗下Parsaclisib已通过国家药品监督管理局药品审评中心公示期,纳入突破性治疗药物品种,拟定适应症为复发/难治性滤泡性淋巴瘤。
2018年12月,信达生物与Incyte就Parsaclisib等三个处于临床试验阶段的候选药物达成战略合作。根据协议条款,信达生物拥有Parsaclisib及其他两个候选药物在中国大陆、中国香港、中国澳门和中国台湾地区的开发和商业化权利。
在2020年举行的第62届美国血液学年会(ASH)上,Incyte公司报道了Parsaclisib治疗复发/难治性滤泡淋巴瘤的一项临床研究数据。该研究显示,Parsaclisib单药在r/r FL患者 (N=95) 中的客观响应率达到75%,中位无进展生存期达到15.8个月。
滤泡性淋巴瘤是全球第二常见的淋巴瘤类型,是最常见的惰性淋巴瘤,在非霍奇金淋巴瘤中发病率仅次于弥漫大B细胞淋巴瘤,具有易向弥漫大B细胞淋巴瘤转化,缓解后复发率极高的特点。近年来,免疫治疗逐渐取代化疗和放疗,针对不同类型淋巴瘤都显示出良好的临床治疗效果,但其安全性、药效持续性以及肿瘤适应症选择方面仍然面临瓶颈。Linperlisib、Parsaclisib治疗复发/难治滤泡性淋巴瘤取得了令人欣喜的结果,也表明这种新型PI3Kδ选择性抑制剂有望为罹患这一重疾的人群带来一项新的疗法。
参考资料:
1.Retrieved Mar 29 2021, from
https://mp.weixin.qq.com/s/6wSAcFWAB9HogX6X60L9ow
2.Zhang, M., Jang, H., & Nussinov, R. (2020). PI3K inhibitors: review and new strategies. Chemical science, 11(23), 5855–5865. https://doi.org/10.1039/d0sc01676d
3.信达生物官网



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57