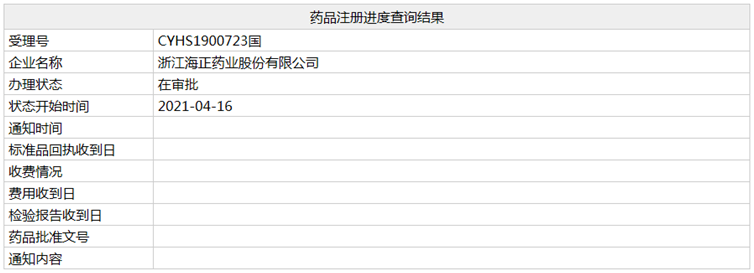
近日,海正药业4类仿制药「盐酸鲁拉西酮片」的上市申请(相关受理号为CYHS1900723)在NMPA的状态变更为"在审批",预计不日将正式被批准用于治疗成人**分裂症,成为国内该品种的首仿。
**分裂症是复发率很高的慢性疾病,除了会伴有幻觉、妄想、言语紊乱等阳性症状以及情绪表达减少或动力缺乏等阴性症状之外,还常会伴有记忆力、注意力、执行能力低下等认知功能障碍和坐立不安、抑郁等情绪症状。随着时间的推移,各种各样的症状出现,生活和就业会变得愈发困难。据中国**卫生调查(CMHS)显示,国内**分裂症及其他**病性障碍患者数量或达一千万。
目前常用的非典型抗**病药中,大多对阳性症状的控制尚可,但并不能完全解决包括阴性症状、认知症状等在内的多维度症状。而且,部分药物容易产生体重增加,糖脂代谢异常等副作用。
盐酸鲁拉西酮(urasidone HCl,Latudal)是住友制药研发的一款非典型抗**病药物,对多巴胺(D2)和五羟色胺(5-HT2A、5-HT7)受体显示出较强的亲和力,具有拮抗作用,对5-HT1A受体具有部分激动作用,而对组胺H1和毒蕈碱M1受体几乎不具有亲和力。临床研究显示:Latudal对**分裂症患者的多维度症状有良好的控制、改善作用之外,同时具有良好的耐受性和依从性。
Latudal最早于2010年10月在美国获批,截止目前已被FDA批准三个适应症,即(1)用于治疗青少年(13-17岁)和成人**分裂症;(2)作为一种单药疗法以及作为锂盐或丙戊酸的辅助疗法,用于治疗成人患者双相I型障碍(双相抑郁)相关的重度抑郁症发作。(3)用于治疗儿科患者(10-17岁)双相I型障碍(双相抑郁)相关的重度抑郁症发作。
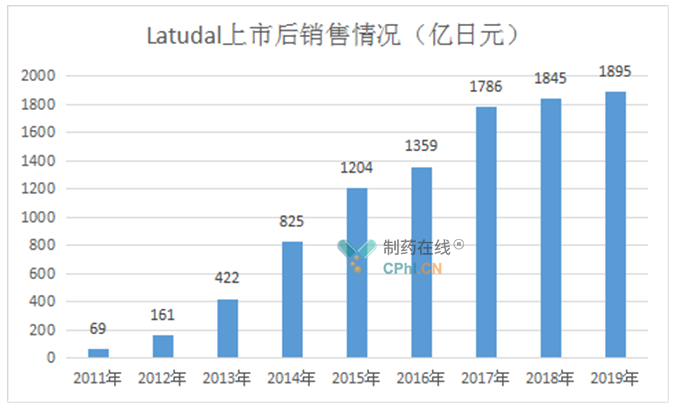
截止2020年末,Latuda已在全球27个国家和地区获批上市,凭借疗效、安全性、耐受性的综合特点优势,Latuda被众多国际治疗指南推荐使用。据公司财报,Latudal自上市累计创造了9566亿日元的销售额。
在中国,Latudal于2016年在中国台湾地区和中国香港地区被批准用于治疗**分裂症,2017年在中国台湾地区被批准用于治疗双相I型抑郁症。在大陆,Latudal于2019年1月被NMPA批准用于治疗成人**分裂症,商品名为罗舒达。而且,该药在2020年医保谈判中成功入围2020年国家医保,有望惠及更多的**分裂症患者。
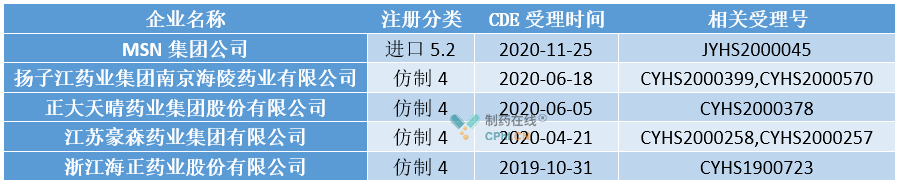
据insight数据库,目前国内已有多家企业开始布局鲁拉西酮仿制药市场。5家企业先后递交仿制药上市申请(详见下表),其中海正药业最早递交上市申请,豪森药业和扬子江药业笔者据临床试验登记情况推测其还递交了针对双相I型障碍障碍的上市申请。此外,湖南洞庭药业、石家庄四药、华海药业和辰欣药业处于BE试验阶段。
除了鲁拉西酮,住友制药在中国市场还有一款非典型**分裂症药物--洛珊®(Lonasen®,通用名:blonanserin,布南色林片)。该药高选择性阻断多巴胺D2受体亚型(D2、D3)以及5-HT2A受体。多项临床试验结果显示,布南色林不仅可以改善**分裂症的阳性症状(幻觉、妄想等),也可以改善阴性症状和认知功能。
Lonasen先后于2008年和2009年在日本和韩国获批,2017年2月在国内获批,并顺利进入2020年国家医保。据公司财报,Lonasen销售额在2017年达到销售额峰值,约126亿日元。目前,国内也有多家企业布局布南色林仿制药市场,其中仅石家庄四药一家企业递交4类仿制药上市申请(相关受理号为CYHS2100157)。
此外值得一提的是,住友制药与日本电工株式会社(Nitto)合作开发Lonasen的透皮贴片(商品名Lonasen Tape)于2019年6月在日本获批,2019年销售额达5亿日元。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57