近年来,基于铁死亡的抗癌策略获得了广泛认可,在国内外掀起了抗癌药物开发热潮。而在铁死亡药物开发中,天然药物提供了直接来源,研究已经发现很多天然产物具有铁死亡抗癌药物开发潜力,让我们一起来看一看代表性的铁死亡天然抗癌药物。
1. 青蒿素
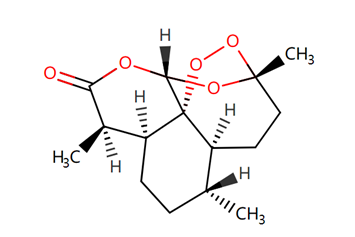
图一 青蒿素结构
青蒿素(图一)属于倍半萜类天然产物,是菊科植物黄花蒿干燥茎叶的有效成分,我国药学家屠呦呦因发现青蒿素获得了诺贝尔生理学与医学奖。研究发现,青蒿素可通过诱导肿瘤细胞的铁依赖性死亡发挥抗癌作用。机制研究显示,青蒿素可以与转铁蛋白的结合增强其对癌细胞的选择性和细胞**。
2. 双氢青蒿素
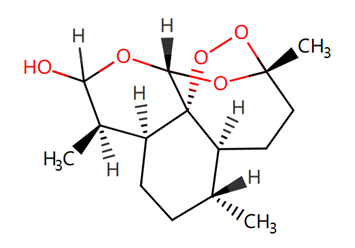
图二 双氢青蒿素结构
双氢青蒿素(图二)是青蒿素衍生物,具有较高的水溶性。针对人类肝癌细胞HepG2的实验显示,双氢青蒿素可通过芬顿样反应增加癌细胞内的活性氧(ROS),并减少GSH和GPX4的表达而诱导肿瘤细胞铁死亡,并证实外源性铁能够加速双氢青蒿素的芬顿样反应,加速癌细胞铁死亡。 又有研究证实,双氢青蒿素可以通过铁蛋白调节和铁反应元件信号通路调控细胞铁稳态,促进半胱氨酸剥夺和GPX4抑制,从而增敏细胞的铁死亡。值得一提的是,研究显示双氢青蒿素还可通过诱导恶性疟原虫铁死亡发挥抗疟作用。
3. 青蒿琥酯
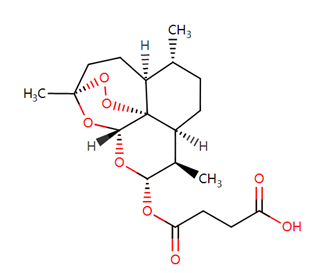
图三 青蒿琥酯结构
青蒿琥酯也是青蒿素衍生物,具有较为显著的抗肿瘤活性。研究显示青蒿琥酯有激活溶酶体的作用,并可通过增加铁蛋白水解,升高铁浓度,进而通过铁依赖性诱导铁死亡。机制研究显示,在青蒿琥酯的诱导下,肝细胞癌(SMMC-7721)细胞内的脂质过氧化水平升高,而用铁离子螯合剂去铁胺可以消除青蒿琥酯所导致的细胞内脂质过氧化。
4. 荜茇酰胺
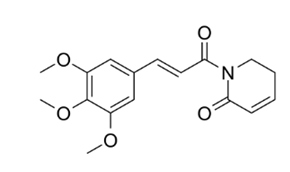
图四 荜茇酰胺结构
荜茇酰胺属于生物碱类化合物,是胡椒科植物荜茇干燥根中的有效成分。研究显示,对于胰 腺癌,荜茇酰胺可通过升高活性氧(ROS)的表达,从而诱导癌症细胞发生铁死亡。机制研究显示,荜茇酰胺杀伤效果可被抗氧化剂N-乙酰半胱氨酸、铁死亡抑制剂和铁螯合剂抑制,而凋亡抑制剂不能抑制其杀伤活性,这说明荜茇酰胺的抗癌机制与铁死亡相关。针对大肠癌细胞HT29和SW620的试验显示,荜茇酰胺调节可以调节活性氧(ROS)水平,控制GSH和Nrf2表达水平诱导铁死亡,发挥抗癌作用。
近年来,铁死亡已经成为了药物研发的热点方向。除了癌症,其还在炎症、感染、脑卒中、非酒精性脂肪性肝炎等多种其他疾病方面显示了靶向药物开发潜力。例如,研究显示丹参酮ⅡA能够抑制小鼠海马细胞内ROS、过氧化脂质活性和铁含量,从而抑制铁死亡的发生,达到保护海马细胞的作用,这显示了参酮ⅡA抗铁死亡在神经性疾病方面的治疗药物开发潜力。铁死亡做为一个药物开发的新兴领域,随着研究的不断深入,其未来在疾病的治疗方面必然还会发挥更大的作用;同时,天然产物做为药物开发的重要来源,其在铁死亡药物开发上也必然显示其支配作用,未来定会有越来越多的铁死亡相关天然药物被开发出来,惠及更多的患者。
参考资料:
1. Research Progress of Chinese Medicine on the Mechanism of Ferroptosis,2021;
2. Research Status of Ferroptosis and Inflammatory Diseases,2021;
3. Mechanisms of ferroptosis and its involvement in hepatocellular carcinoma,2020.



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57