01
Levofloxacin的研发历史
左氧氟沙星(Levofloxacin)属于第三代喹诺酮类药物。喹诺酮类(quinolones)药物是一类人工合成的抗菌药,这类药的共同特点有:
1、抗菌谱广、抗菌活性强;
2、口服吸收良好;
3、体内分布广、血浆半衰期较长;
4、不良反应相对较少。
喹诺酮类药物来源于意外的发现——世界各国在开展合成抗疟疾药物的研究过程中产生的大量副产品。1946年,美国斯特林· 怀特研究院的有机化学家勒谢(George Y. Lesher, 1926-1990)博士在进行一项实验,试图合成抗疟疾药物氯喹。在对合成过程中的副产品进行常规筛选时发现了一个副产物——7-氯-1-乙基-1,4-二氢-4-氧代-3-喹啉羖酸,它在体外对若干革兰氏阴性菌具有弱的活性。这个发现促进了设计和合成新类似物的研究。
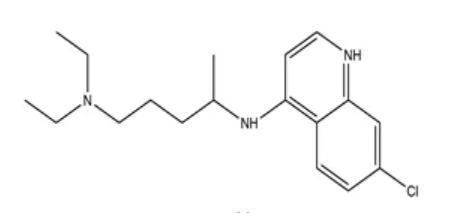
图1. 氯喹结构式
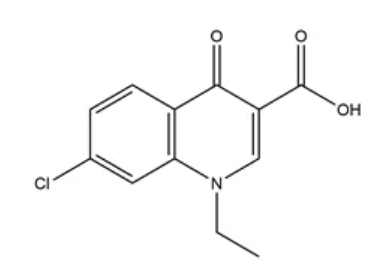
图2. 7-氯-1-乙基-1,4-二氢-4-氧代-3-喹啉羖酸结构式
1962年,勒谢博士研制出了萘啶酸,并报道其可作为新型抗菌药物。这是第一个上市的喹诺酮类药物,也是后来形成的喹诺酮家族的祖先。

图3.勒谢博士及刊发文章
多年来,国内外对喹诺酮类药物的结构进行不断地修饰,陆续开发出了多种新药物并投入临床使用。该类药物的抗菌谱伴随着研究的深入而不断拓宽,从单一抗革兰阴性菌的窄菌谱,逐渐发展成为抗革兰阳性菌、厌氧菌、分枝杆菌、军团菌、支原体和衣原体的广谱抗菌药。到目前喹诺酮类药物已经经历了4代发展。
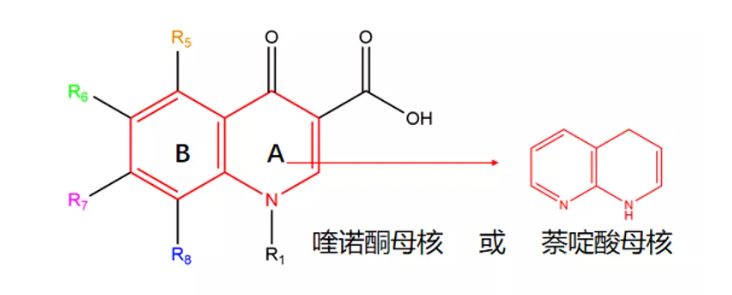
图4. 喹诺酮类结构式
第1代喹诺酮类药物:以萘啶酸为代表,抗菌谱窄且药效较弱,仅对大肠杆菌、痢疾杆菌、克雷伯杆菌等病原体有效。主要用于治疗革兰阴性杆菌所致的尿路感染,但易形成耐药性,现已基本被淘汰。
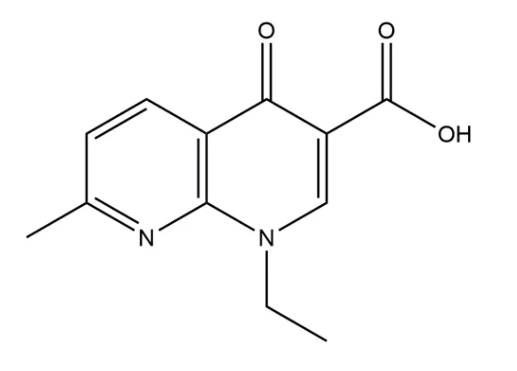
图5. 萘啶酸结构式
第2代喹诺酮类药物:包括批哌酸、西诺沙星等,其在抗菌谱较第1代有所扩大,虽然仍然对革兰氏阳性菌药效不佳,但其副作用较少,可用于治疗肠道和尿路感染。但是该其血浆浓度不高,且随着耐药性发展迅速,应用也日趋减少。
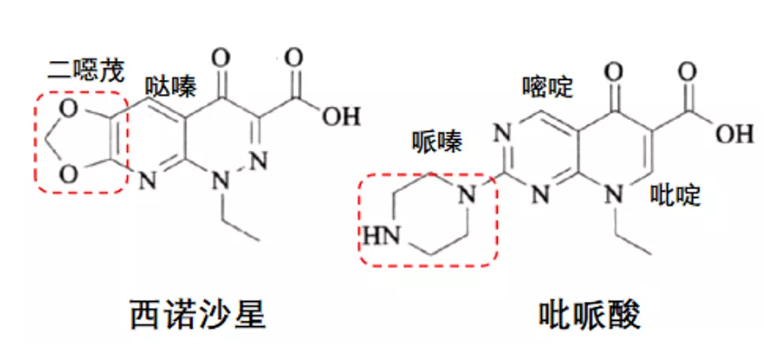
图6. 第二代喹诺酮类药物结构式
第3代喹诺酮类药物:主要有诺氟沙星、氧氟沙星、左氧氟沙星、培氟沙星、依诺沙星、环丙沙星、洛美沙星等。第3代喹诺酮类药物也称氟喹诺酮类药物,主要结构特征是在喹诺酮的6位引入氟原子,使其抗菌谱进一步扩大,对革兰氏阴性菌和阳性菌及支原体、衣原体、军团菌及分支杆菌都有抑制作用。因其效果好、抗菌谱广、副作用小等特点,目前在临床中的应用非常广泛,用于泌尿生殖系统、胃肠道疾病,以及呼吸道、皮肤组织的革兰阴性细菌感染的治疗。
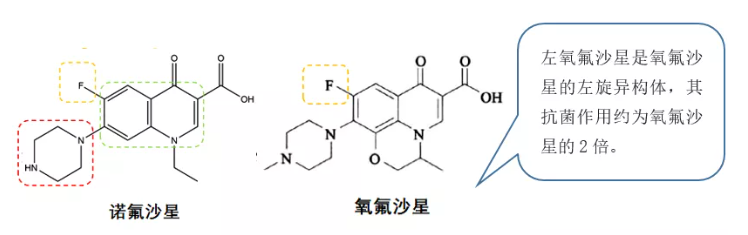
图7. 第三代喹诺酮类药物结构式
第4代喹诺酮类药物:也称新氟喹诺酮类药物,主要包括格帕沙星、克林沙星、加替沙星、莫西沙星等。抗菌谱是目前为止最 大的,其结构特点为继续保留母核6位F,并在5或8位引入氨基或甲基及甲氧基衍生物。除了保持第3代抗菌谱广、抗菌活性强、组织渗透性好等优点外,新氟喹诺酮类药物的抗菌谱进一步扩大,且对革兰阳性菌和厌氧菌的活性作用增强。
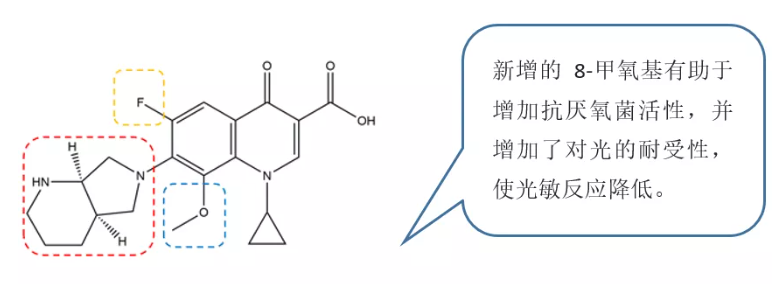
图8. 第四代喹诺酮类药物结构式
02
Levofloxacin的合成分析
左氧氟沙星是一种十分重要的药物分子,因而它的合成自然也是受到科学家的广泛关注,其中并环骨架的构建是较为容易的工作,因而如何高效构建左氧氟沙星中的手性中心成为科学家致力于解决的问题。
当前主要的合成思路有两种,即化学拆分和立体选择性合成。前者由外消旋的氧氟沙星或其前体经过物理或化学手段进行手性拆分,后者则是直接在反应中使用带有手性的底物或手性试剂进行反应得到手性产物。化学拆分包括用HPLC直接拆分外消旋的氧氟沙星(图9)、拆分氧氟沙星的前体酯(图10)等方法。立体选择性合成的底物有多种选择,其中使用较多的是三氟硝基苯和四氟苯甲酸。
以三氟硝基苯为起始原料(图11),通过多种方法得到光学活性的苯并噁嗪中间体后,再通过常用方法合成出产品。以四氟苯甲酸为起始原料(图12),加入S-2-氨基丙醇,环合水解得到最终产物,该路线经历8步反应,总收率为39.2%。
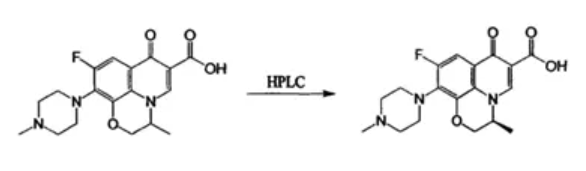
图9. 用HPLC直接拆分外消旋的氧氟沙星
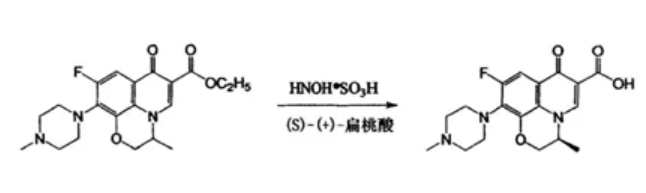
图10. 拆分氧氟沙星的前体酯
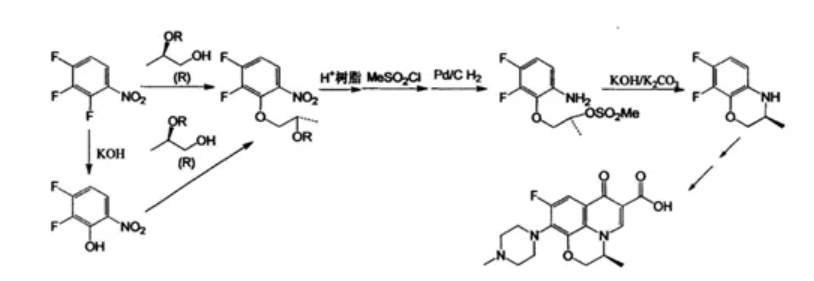
图11. 以三氟硝基苯为起始原料的立体选择性合成
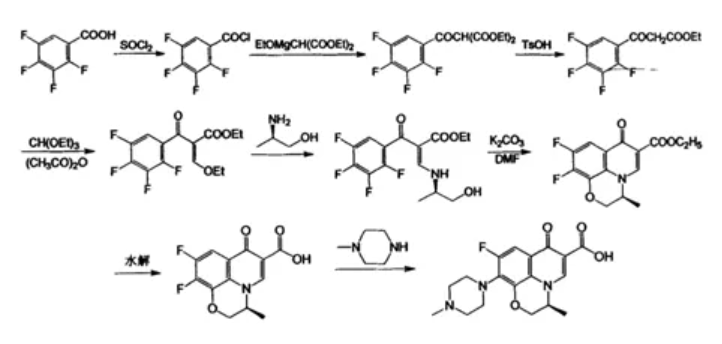
图12. 以四氟苯甲酸为起始原料的立体选择性合成,赵爱桔,2011
化学拆分最多只有50%转化为左氧氟沙星,而剩下的为活性很弱的右氧氟沙星,且目前尚无将右旋转为左旋的报道,所以化学拆分无法扩大规模而工业化生产左氧氟沙星。三氟硝基苯属于第一类危险品——爆炸 物质和物品,在使用、储藏和运输过程中都需要采取妥善措施。对于四氟苯甲酸为起始原料的合成路径来说,合成中需要的四氟苯甲酸和S-2-氨基丙醇国内均有售,且工艺稳定,收率较高,是一条比较完善的可投入工业化生产的合成路线。
03
Levofloxacin的作用机理
关于左氧氟沙星的杀菌机制,笼统地说,左氧氟沙星是通过与拓扑异构酶-DNA单链复合物结合,阻止细菌的两种拓扑异构酶(旋转酶与拓扑异构酶Ⅳ)作用,从而抑制细菌DNA的复制,导致细菌生长增殖停滞,继而死亡。
拓扑异构酶通过催化DNA链的断裂、旋转和再连接,清除在聚合酶行进过程中产生的正超螺旋,使DNA复制能够持续进行。
旋转酶(gyrase)属于Ⅱ型拓扑异构酶,其催化的反应依赖于ATP,在ATP的存在下,一个DNA双螺旋上的两条链同时出现切口,随后另一个DNA双螺旋穿过切口,切口重新连接。
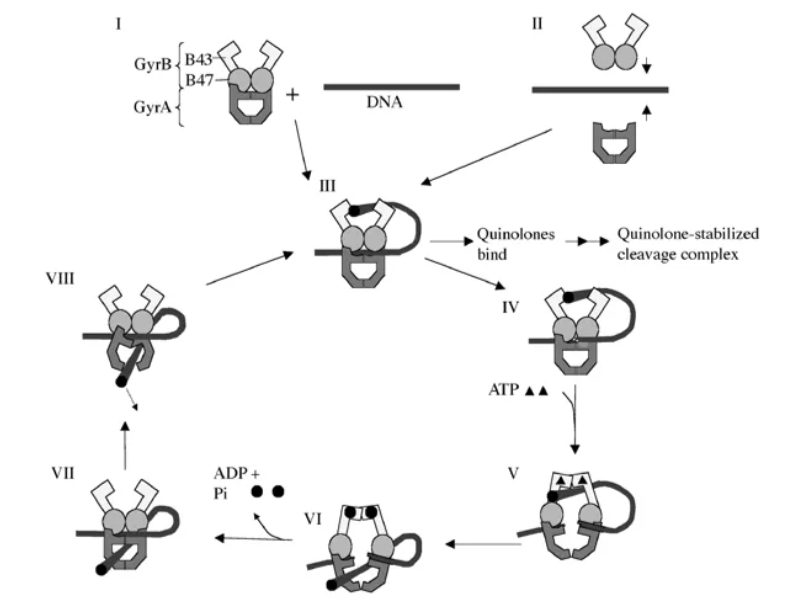
图13. 旋转酶作用机制,来源:Journal of Antimicrobial Chemotherapy , 2003, 51, Suppl. S1, 29–35 Peter M. Hawkey
喹诺酮类药物的抗菌作用模型为:拓扑异构酶与双链DNA结合,使其中一条链断裂,引入一对交错的单链缺口,酶与单链DNA断裂的5’末端共价键连接形成酶-DNA复合物,DNA的碱基暴露,易与喹诺酮C-3、C-4位的羰基形成氢键连接,形成喹诺酮-DNA-酶三元复合物。一个切口形成的口袋可以结合4个喹诺酮分子。
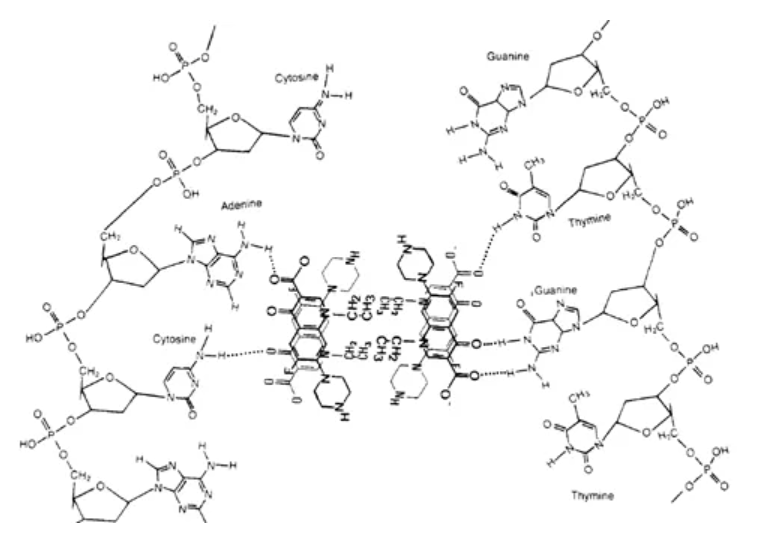
图14. 左氧氟沙星结合机制 ,来源:Biochemistry,Vol. 28, No. 9, 1989 Shen et al.
先后进入口袋的喹诺酮分子之间靠π-π堆叠的相互作用力结合,右旋的氧氟沙星的氮氧杂环上连的甲基在平伏键上而氢在直立键上,由于直立键需要向平面外伸展,所以处于平伏键的甲基由于体积比较大会阻碍堆叠作用,而左氧氟沙星的甲基在直立键向平面外伸展,分子间π-π堆积作用更强,从而与DNA结合更稳定。同时有实验表示,同样的疏水口袋只能容纳2个氧氟沙星而可以容纳4个左氧氟沙星。
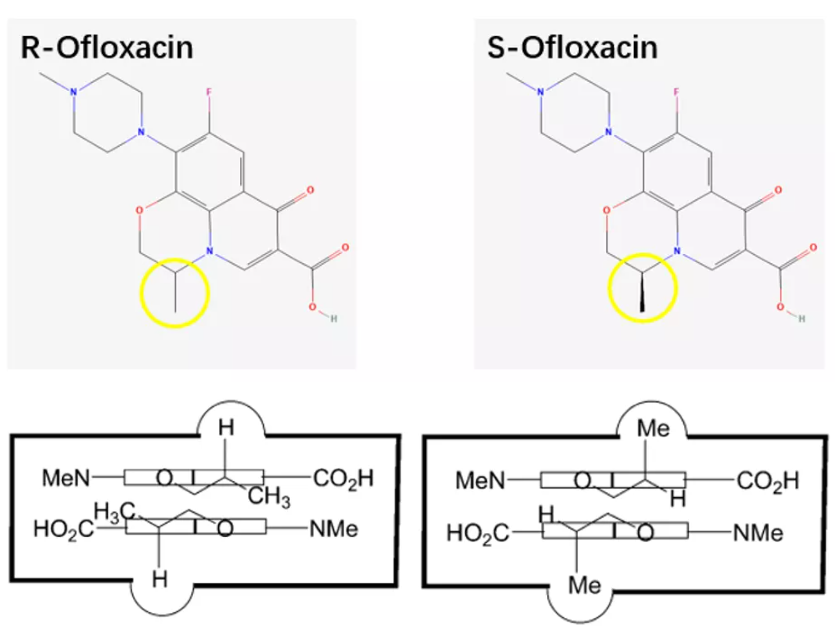
图15. 氧氟沙星与左氧氟沙星的分子对比,来源:Chem.Rev.2005,105,559-592, Lester A. Mitscher
左氧氟沙星的耐药机理主要有:
1、Ⅱ型拓扑异构酶变异:使得药物不能与酶-DNA复合物稳定结合;
2、细菌细胞膜通透性的改变:药物进入细胞依赖膜孔蛋白,外膜蛋白与脂多糖变异均可使细菌摄取药物减少而导致耐药性;
3、细菌的主动外排系统亢进:导致细菌内药物浓度降低。
04
Levofloxacin的ADME
ADME即指吸收、分布、代谢和排泄四部分。如何确保药物分子易于吸收,可以良好的分布到作用地点,不产生有毒副作用代谢产物,并快速的排出体外,是药物研发改进中困难的一环。身为明星药物之一广泛应用的左氧氟沙星,在ADME上具备有出色的表现。
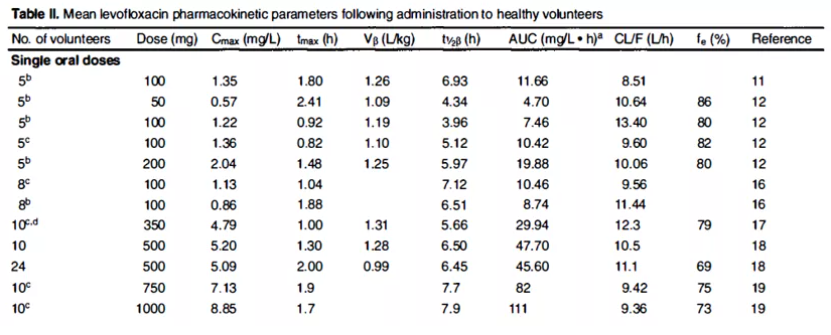
图16. 口服左氧氟沙星后的药代动力学参数,来源:Clin-Pharmacokinet , 19977, 32, 101–119, Fish, D.N.et al.
1 吸收
左氧氟沙星 50 至 500mg 单次和多次给药后,其平均分布容积范围为 1.09 至 1.26 L/kg(89 至 112L)。该数据表明药物于组织中广泛分散。在50mg-1000mg剂量的口服之后,到达血浆最 大浓度的时间集中于0.8-2.4h。并且服用药物前是否进食对药物的吸收分布并无影响。在临床试验中进行了24名健康实验者(12男12女)的单次口服500mg剂量实验,同时吃下高脂肪餐的实验组tmax延长1h,cmax下降约14%(从5.93降至5.09mg/L),因此左氧氟沙星可以不考虑饮食情况而给药。
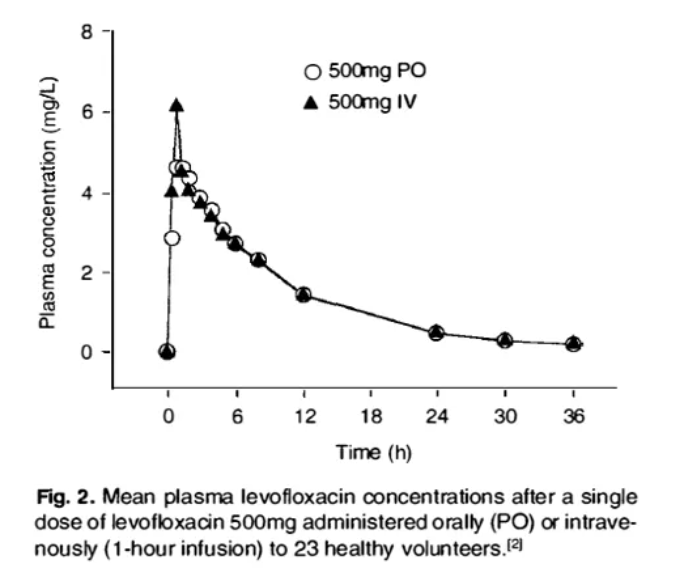
图17. 左氧氟沙星口服或静脉注射后血浆浓度变化,来源:Clin-Pharmacokinet , 19977, 32, 101–119, Fish, D.N.et al.
如图,左氧氟沙星口服和静脉注射血浆浓度相近。之所以这样是因为左氧氟沙星不仅在胃肠道中吸收速度快而且首过效应小,吸收基本完全。这一特性可以通过生物利用度来加以衡量,其绝 对生物利用度基本在99%左右。因此可以实现口服与静脉注射的互换,给药治疗上具备天然优势。
2 分布
左氧氟沙星同样可以保持和血浆浓度同样的浓度穿透胎盘,并进入到母乳之中。但是左氧氟沙星难以穿透血脑屏障,在脑脊液中浓度仅为同时血浆浓度的16%,这可能表明左氧氟沙星(类似于其他氟喹诺酮类)在治疗中枢神经系统或眼内感染方面的作用有限。与其他氟喹诺酮类药物一样,左氧氟沙星会积极渗透到吞噬细胞中,这有利于杀灭细胞内病原体。左氧氟沙星在吞噬细胞和其他组织中的大量积累导致可以观察到观察到的较大的Vd。将其暴露于 5 - 50mg/L的药物浓度后,左氧氟沙星在中性粒细胞中的平均细胞内/细胞外浓度比范围为 8.8 至 9.8mg/L。左氧氟沙星和其他氟喹诺酮类药物在吞噬细胞内的积累不仅可以增强它们对细胞内病原体的活性,还可以通过在感染部位的组织和体液中维持高且持续的药物浓度,从而提高抗细胞外病原体的活性。
3 代谢和排泄
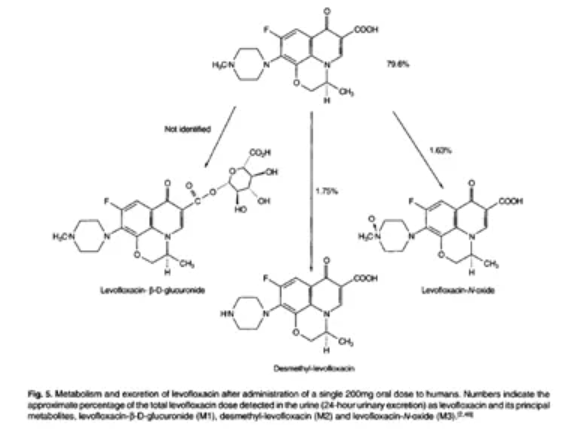
图18. 左氧氟沙星的代谢,来源:Clin-Pharmacokinet , 19977, 32, 101–119, Fish, D.N.et al.
如图17,左氧氟沙星的药-时曲线可以采用二室模型,其特征为一级消除,曲线为双指数衰减。因此可以方便的写出其动力学过程的数学方程,进行给药的数据计算。其数据无论是每日一次、两次或三次口服或静脉给药基本保持线性和可预测的特性。
左氧氟沙星的半衰期在9-11h左右,经过36-44h后,体内药物含量达到稳态血浆浓度的94%,在48h之后即达到稳态,cmax值根据口服和静脉注射分别为5.7和6.4mg/L,从而确保持久稳定疗效。
已经在人、猴子、大鼠、狗中检测出三种左氧氟沙星的代谢产物。这些代谢物是左氧氟沙星-D-葡萄糖醛酸苷 (M 1)、脱甲基-1-左氧氟沙星 (M2) 和左氧氟沙星-N-氧化物 (M3)。但在人类中仅鉴定了 M2 和 M3 代谢物。左氧氟沙星在人体中的代谢有限,主要以原形从尿液中排出。单次口服左氧氟沙星后,24 小时内只有不到 5% 的左氧氟沙星作为代谢物从尿液中排出(M2 和 M3 分别占剂量的约 1.75% 和 1.63%),≤5% 的剂量以无活性的 N-氧化物和去甲基代谢物形式存在,而约 79.6% 则以原型药物的形式在接下来的 24 小时内排出。上述左氧氟沙星在人体中的代谢特征与氧氟沙星报道的相似。由于代谢物的形成可以忽略不计,因此它们几乎没有相关的药理活性。
05
Levofloxacin的专利市场
左氧氟沙星是重要的抗菌手性代表药物在人类抗菌历史上占据了非常重要的一部分,下面将介绍一下左氧氟沙星的专利市场部分:
1 原研药专利到期
首先左氧氟沙星专利于2011年到期,同年美国FDA就批准了多家公司提交的左氧氟沙星通用名药上市的申请,准许的剂型包括片剂、口服液、注射液等等。这样国内许多公司也就加入到了左氧氟沙星仿制药的研究和专利申请;不过值得一提的是由于左氧氟沙星的原研药厂——日本第一三共株式会仍然拥有该两款原研药全部酸根、盐基、剂型的专利,因此第一三共可以针对仿制药展开合作和质量认定,从而在一定程度上保证了原研药厂的一部分权利。
2 中国的左氧氟沙星专利市场
1、中国左氧氟沙星专利分布分析(不完全统计)
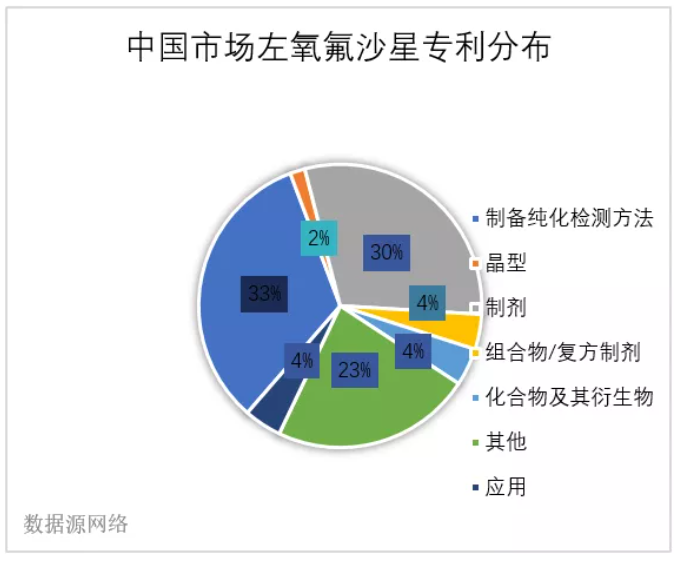
图19. 中国市场左氧氟沙星分布饼状图
在国内,左氧氟沙星的专利主要有上图几个部分.
其中,制备和纯化检测方法占据了33%的比例;各种药物制剂又占据了30%左右;在其他里面的大部分专利,其实都是关于包装盒设计的专利;
这三个方面的专利就占据了中国左氧氟沙星专利的8成以上专利;
而更为重要的晶型和化合物及其衍生物专利所占比例极少,这或许也是中国原研药物不多的原因吧,核心技术专利掌握还有很大不足,这也是我们这一代人需要继续奋斗的部分。
2、中国的左氧氟沙星市场组成
左氧氟沙星是原研厂家第一三共的主要产品之一,商品名可乐必妥(Cravit),于1993年上市。
目前我国市售的左氧氟沙星注射液有原研药和国产仿制药两类。《中国药房》2016年论文显示,国产仿制药由于制备过程药物溶解度和使用过程药物生物利用度的不同有盐酸盐、乳酸盐、甲磺酸盐这3种不同酸根。国内现在市场上,盐酸左氧氟沙星和乳酸左氧氟沙星销售也比较多,存在药剂形式也比较多,有片剂、滴剂、注射液等等。比如:左氧氟沙星片、盐酸左氧氟沙星片等等……
3 中国左氧氟沙星目前存在的挑战和机遇
1、左氧氟沙星目前存在的一些挑战
1)左氧氟沙星属于第三代广谱氟喹诺酮类抗菌药物,是日本第一制药株式会社开发上市的品种。左氧氟沙星抗菌作用强,对多数肠杆菌科细菌有较强的抗菌活性,而且对眼球感染性疾病的疗效尤其显著,因此,在国内外上市后颇受市场欢迎。
2)但是随着左氧氟沙星注射剂的大量应用,其不良反应问题也日益突显,临床用药亮起黄灯。据IMS数据,2015年全球左氧氟沙星原研药品市场创下了3.09亿美元的新低,同比上一年下滑20.75%。
3)2016年,美国食品药品监督管理局(FDA)发布通告,提示急性鼻窦炎、急性支气管炎和单纯性尿路感染药物治疗时,氟喹诺酮类药品抗菌治疗引发相关严重不良反应的风险通常大于效益。
随着 2016 年门诊输液全面叫停,以及「能不用就不用、能少用就不多用,能口服不肌注、能肌注不输液」的治疗原则下,客观上冲击了左氧氟沙星市场,预测其增长率将有所下降。
4)早在2011年1月,国家药监部门就发布了关注13个喹诺酮类药品的不良反应通报,2013年11月再次发布通告,建议药品生产企业加强药品不良反应监测,及时修订氟喹诺酮类药品的说明书,更新相关用药风险信息及不良反应、注意事项等内容。最终在国家药监部门加大对喹诺酮类药品不良反应的监测及合理用药的督导下,曾经一路火爆高涨的喹诺酮类药物市场,逐渐在生产、销售到终端市场各环节发生了变化。左氧氟沙星的销量深受影响。
2、左氧氟沙星的未来发展前景
根据新思界产业研究中心发布的《2020-2024年中国喹诺酮类抗菌药行业市场供需现状及发展趋势预测报告》显示,在限抗令的影响下,我国抗菌药物临床应用逐渐合理化,对于喹诺酮类抗菌药市场需求也有所降低。但由于喹诺酮类抗菌药存在一定刚需性,且喹诺酮类抗菌药不断更新换代,因此当前国内喹诺酮类抗菌药市场规模保持稳定发展,到2019年国内喹诺酮类抗菌药物的市场规模约有128亿元。并且根据最新的2021年的预测,未来5年左氧氟沙星的市场规模将会继续增加。
新思界医药行业分析人士表示,国内外市场对左氧氟沙星需求旺盛,且该药临床使用频繁,其他沙星类药物竞品较少,预计未来很长一段时间,左氧氟沙星市场仍将继续保持增长态势。
致谢
感谢吴兴新老师与文敏助教对文章的撰写给予悉心指点,提出了宝贵的意见。
关于笔者
寻药真理团
他们是南京大学新药研发策略课程的学生,本篇为该课程中新药4组学生成员杨欣怡、江豪、吴栩喆、邓高、沈雷共同完成。
他们朝气蓬勃、他们斗志昂扬,他们脚踏实地学习新药研发知识,他们坚信吾爱吾师吾更爱真理。
他们是新一代医药行业接班人,他们是新药研发领域的未来之光!
*本文仅为学术内容交流,不构成任何用药建议!
参考文献
[1] Hawkey Peter M. Mechanisms of quinolone action and microbial response.[J]. The Journal of antimicrobial chemotherapy,2003,51 Suppl 1.
[2] Shen L L , Mitscher L A , Sharma P N, et al. Mechanism of inhibition of DNA gyrase by quinolone antibacterials: A cooperative drug-DNA binding model[J]. Biochemistry, 1989, 28(9):3886-3894.
[3] Mitscher L A . Bacterial topoisomerase inhibitors: quinolone and pyridone antibacterial agents[J]. Chemical reviews, 2005, 105(2):559.
[4] Fish, D.N., Chow, A.T. The Clinical Pharmacokinetics of Levofloxacin.[J]. Clin-Pharmacokinet , 19977, 32, 101–119.
[5] Cristina Vercelli, Beata Łebkowska-Wieruszewska,et al. Pharmacokinetics of levofloxacin in non-lactating goats and evaluation of drug effects on resistance in coliform rectal flora.[J]. Research in Veterinary Science , 2020, 133, 283-288.
[6] 赵爱桔. 左氧氟沙星合成工艺的研究[D]. 浙江:浙江大学,2011.



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57