帕金森病(PD)是仅次于阿尔兹海默病的第二大常见慢性进行性神经退行性疾病,以脑内多巴胺能神经元进行性丢失和路易小体形成为特征,主要表现为运动迟缓、肌强直、震颤、姿势步态异常等运动障碍,常伴有嗅觉减退、睡眠障碍等多种非运动症状,给患者和家属带来巨大的身体和**负担。
据统计,PD大约影响全球1000万人,而且随着全球老龄化的加剧,PD患病人数还将进一步增加。“开-关现象”(ON-OFF)是PD药物治疗后期的并发症,其中“开”是指药物治疗对病人起到明显的治疗效果,病人能运动;“关”是指病人在接受治疗一段时间后运动能力丧失,这是由于口服之间的低水平多巴胺引起的。
目前,PD尚无法治愈,其治疗方法和手段包括药物治疗、手术治疗、运动疗法、心理疏导及照料护理等,其中药物治疗作为首选,且是整个治疗过程中的主要手段。
全球50余款PD药物上市
这一创新疗法即将登陆中国
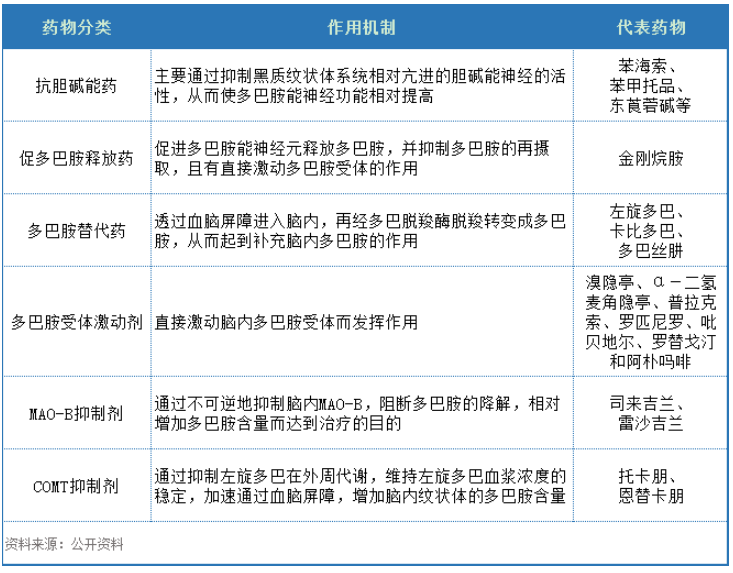
据药智网不完全统计,全球大约有50多种PD药物获批上市。根据作用机制的不同,已上市的PD药物大致可分为抗胆碱能药物、促多巴胺释放药物、多巴胺替代药物、多巴胺受体激动剂、B型单胺氧化酶抑制剂、儿茶酚-O-甲基转移酶(COMT)抑制剂六大类。
其中抗胆碱能药物主要用于伴有震颤的PD患者。
COMT抑制剂主要是作为左旋多巴的辅助性治疗,增加左旋多巴的疗效,减少左旋多巴的用量,适用于有明显波动症状的重症PD患者,是目前欧美和国内治疗指南明确推荐的、辅助多巴胺治疗PD患者的一线药物。
MAO-B抑制剂是PD一线治疗药物,主要用于早期PD患者,研究证实其通过抗氧化应激、抑制突触核蛋白凝集、减少细胞凋亡以及神经营养作用等保护神经元,部分临床试验显示其可能延缓PD进展。
PD药物分类、作用机制及代表药物
而且,近年来全球监管机构还批准了几款PD药物(详见下表),包括第三代COMT抑制剂Ongentys、MAO-B抑制剂Xadago,以及其他传统PD药物的新机型。
此外,Insightec公司的ExablateNeuro设备于2018年被FDA批准用于治疗震颤为主的PD,2021年11月又被FDA批准用于治疗患有活动性、僵硬或运动障碍症状的晚期PD患者。另,值得提及的是,ExablateNeuro在苍白球切开术中使用聚焦超声波精确定位和消融苍白球,不需要切口,不需要植入大脑,比侵入性手术感染的风险更小。
近年来获批的PD药物
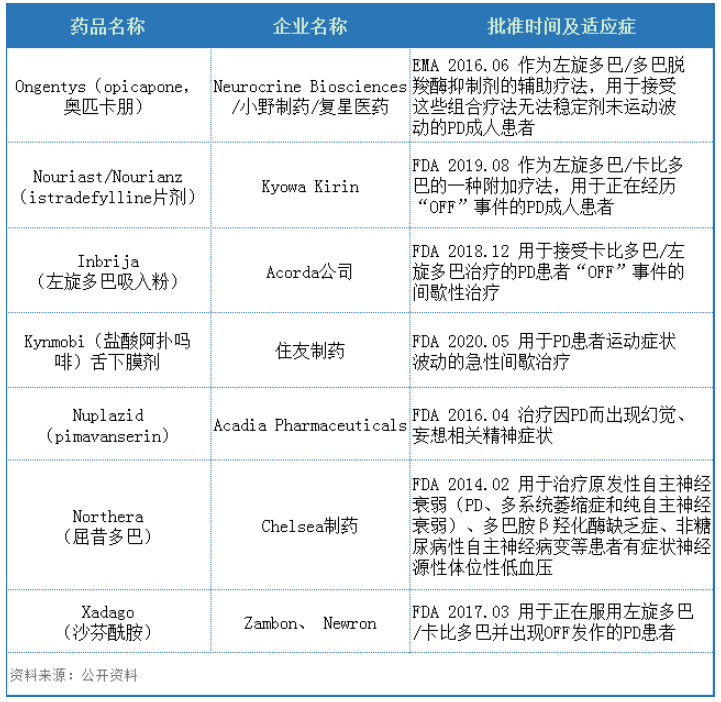
Ongentys是一种新型、口服、选择性、长效、外周COMT抑制剂,通过减少左旋多巴在血液中的分解从而保护左旋多巴,使更多的左旋多巴可以到达大脑,延长其临床效果,帮助患者实现运动症状控制。2016年6月,该药被欧盟批准作为左旋多巴/多巴脱羧酶抑制剂的辅助疗法,用于接受这些组合疗法无法稳定剂末运动波动的PD成人患者。2020年4月,Ongentys25mg和50mg胶囊剂被FDA批准,作为左旋多巴/卡比多巴的一种辅助疗法,用于正在经历运动波动的PD患者,成为第一个被FDA批准的每日一次COMT抑制剂。
istradefylline是一种口服给药的选择性腺苷A2A受体拮抗剂(腺苷是一种广泛分布于人体的神经调节剂,大脑中腺苷A2A受体被发现存在于基底神经节中,基底神经节在运动控制中起重要作用,PD患者基底神经节被发现存在退化或异常)。2013年5月,istradefylline在日本上市销售,用于接受含左旋多巴制剂治疗的PD患者,改善“疗效减退”现象,品牌名为Nouriast。2019年8月,该药在美国被批准作为左旋多巴/卡比多巴的一种附加疗法,用于正在经历“OFF”事件的PD成人患者,品牌名为Nourianz。
Inbrija是利用Acorda的ARCUS平台开发旨在向肺部提供精确剂量的左旋多巴干粉制剂,2018年12月被FDA批准用于接受卡比多巴/左旋多巴治疗的PD关闭期(OFF)间歇性治疗。值得一提的是,Inbrija是第一个获得监管批准的吸入性左旋多巴,该药便于患者自己操作,适用于OFF期的按需治疗。
Kynmobi舌下膜剂是一种新剂型的阿扑吗 啡(阿扑吗 啡是一种多巴胺D2受体激动剂,用作OFF事件的急救药品),2020年5月被FDA批准用于PD患者运动症状波动的急性间歇治疗。值得一提的是,Kynmobi是第一个也是唯一一个快速、按需治疗帕金森病OFF事件的舌下疗法,一天最多可以使用5次。
Northera是一种合成儿茶酚胺,通过脱羧直接转化为去甲肾上腺素,使得中枢和外周神经系统去甲肾上腺素水平升高。
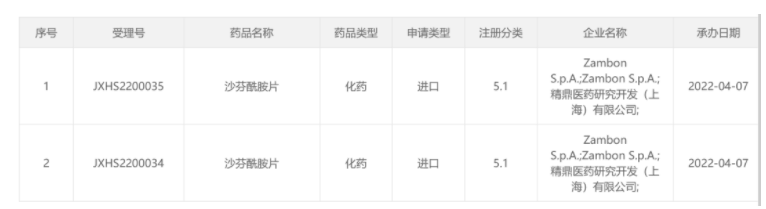
另,值得提及的是;近日CDE官网显示,ZambonS.p.A/精鼎医药「沙芬酰胺片」的进口申请获受理。沙芬酰胺是一款高选择性、可逆第三代B型单胺氧化酶(MAO-B)抑制剂,具有多巴胺能和非多巴胺能双重机制,原研药Xadago于2017年3月被FDA批准作为一种附加治疗药物,用于正在服用左旋多巴/卡比多巴并出现“关期”发作的帕金森病患者。其成为十余年来首 个在美国获批用于治疗帕金森病的新化学实体。如今中国上市申请或受理,为国内患者带来创新疗法用药新选择。
多款新疗法在研
艾伯维ABBV-951进展最快
此外,目前全球还有多款在研PD新疗法,详见下表。
部分在研PD疗法
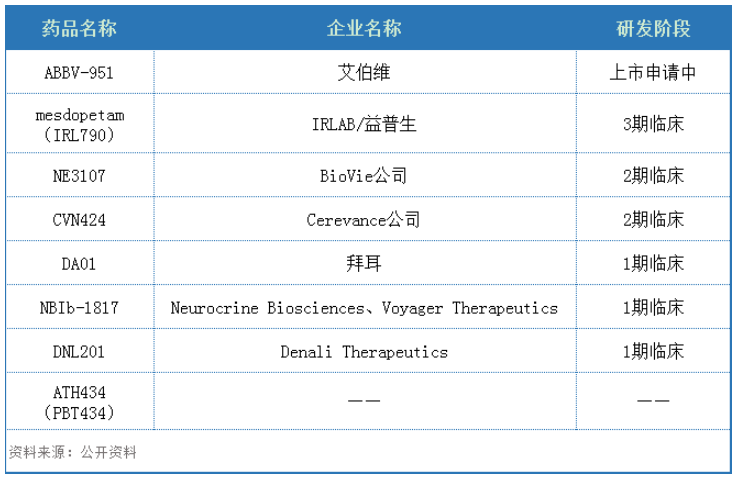
ABBV-951是一种左旋多巴前药和卡比多巴前药的持续皮下输注溶液,被开发用于治疗运动症状不受口服药物控制的晚期PD患者。已公布的该药与口服左旋多巴/卡比多巴进行的头对头优势3期研究M15-736结果显示:ABBV-951在减少晚期PD患者运动波动方面在统计学上优于口服LD/CD,达到主要终点。
mesdopetam是一种新型多巴胺D3受体拮抗剂,被开发用于PD患者预防和治疗左旋多巴诱导的运动障碍(LID),以及治疗帕金森病**病(PDP)。已完成的1b期和2a期临床项目数据显示:在正经历LID的PD患者中,mesdopetam治疗使临床相关终点有很大的改善,减少了PD患者经历运动障碍的时间、延长了患者的“ON”期。2021年07月,益普生与IRLAB签订了一项许可协议,获得mesdopetam的独家全球开发和商业化权利。
NE3107是一种口服、可穿过血脑屏障的小分子化合物,具有抗炎、胰岛素增敏和ERK结合特性,可选择性抑制ERK和NFκB刺激得炎症。临床前研究表明,NE3107与左旋多巴一样能有效改善PD运动症状。而且该药当与左旋多巴联用比单独给予NE3107或左旋多巴具有更大的促运动活性。此外,NE3107与左旋多巴联合使用可降低左旋多巴诱导的运动障碍(LID)的严重程度,但不会降低药物对运动症状的有益作用。今年1月,评估NE3107对PD患者潜在促运动影响的2期临床研究NM201(NCT05083260)完成首 例患者给药。
CVN424是基于Cerevance公司药物发现平台发现的创新疗法,选择性靶向与帕金森病相关的多巴胺D2受体依赖性间接信号通路,旨在产生和左旋多巴或脑深部刺激相同的积极效果的同时,避免不良反应。已公布的2期临床研究结果显示:接受治疗4周后,与安慰剂相比,高剂量CVN424将“OFF”期改善1.3个小时,且无运动障碍的“ON”时间增加。此外,与其他和左旋多巴同时使用的辅助疗法不同,CVN424与安慰剂相比,降低患者的白天嗜睡指标。
DA01是拜耳集团全资下属临床试验阶段生物制药公司BlueRock公司使用多能干细胞产生多巴胺能神经元的疗法,2021年7月被FDA授予治疗PD的快速通道资格认定,今年1月评估该药治疗晚期PD患者的开放标签1期研究完成首 例患者给药。
NBIb-1817是一款使用AAV2病毒载体,携带表达人类芳香族L-氨基酸脱羧酶(AADC)的转基因的基因疗法,旨在通过在大脑细胞中表达AADC酶,帮助将左旋多巴转化为多巴胺,从而改善患者的运动症状。2018年6月,该药被FDA授予再生医学先进疗法(RMAT)认定,用于治疗难以进行医学管理,有运动波动的PD患者。已公布的在该药治疗PD的1b期临床试验结果显示:在15名接受1次基因疗法治疗的晚期PD患者中,14名患者在接受治疗3年之后,仍然经历疾病分级方面的改善。该药不但能够持续改善患者的运动功能,还能降低患者口服药物的需求。
DNL201是一种小分子富亮氨酸重复激酶2(LRRK2)抑制剂,可调节溶酶体功能(LRRK2基因突变是PD最常见的遗传原因之一)。2018年12月,DenaliTherapeutics公司启动DNL201用于PD患者的1b期临床试验。
PBT434是一种新一代喹唑啉类小分子药物,旨在阻断α突触核蛋白的聚集和积累。神经病理学期刊ActaNeuropathologicaCommunications上发表的研究结果显示:在多种帕金森病动物模型中,PBT434显示出防止铁介导的神经退行性疾病和α-突触核蛋白**的潜力。
联手布局
掘金创新疗法
据MarketsandMarkets的最新市场研究报告,2022年全球PD治疗剂市场规模预计将从2017年的42.4亿美元增长到2022年的56.9亿美元,年复合增长率为6.1%。近年来,越来越多的药企开到PD市场潜力,并积极布局PD药物市场,与其他企业联合开发或引进PD新疗法。
2017年11月,伦敦大学学院与Synpromics公司达成合作,为中枢神经系统(CNS)生成一系列合成基因启动子,开发治疗PD的基因疗法。
2018年8月,AxovantSciences从OxfordBioMedica获得全球独家授权,开发并推广PD基因疗法AXO-Lenti-PD(曾用名OXB-102)。
2019年2月,艾伯维与VoyagerTherapeutics联合表示将启动一项15亿美元的基因治疗项目,此项目将专注于治疗PD以及其他同样由于α-突触核蛋白的异常累积导致的疾病。
2020年8月,渤健和DenaliTherapeutics达成一项协议,共同开发和推广Denali的LRRK2小分子抑制剂DNL151,用于治疗PD。
2021年6月,CarawayTherapeutics与艾伯维达成一项独家合作和选择权协议,开发和商业化Caraway靶向TMEM175的小分子疗法。TMEM175是一种钾离子通道,对与PD和其他神经退行性疾病有关的溶酶体功能至关重要。
2021年7月,Ipsen与IRLAB签订独家许可协议,获得D3受体拮抗剂mesdopetam的全球独家开发和商业化权利,用于治疗PD患者在接受左旋多巴治疗之后出现的运动障碍(LID)。
2021年12月,优时比宣布已与诺华达成一项全球性合作协议,共同开发和商业化优时比旗下治疗PD的在研疗法,包括潜在“first-in-class”口服小分子α-突触核蛋白错误折叠抑制剂UCB0599(目前处于2期临床开发阶段)。
2022年3月,翼思生物与STADA集团旗下英国BRITANNIA公司签署一项独家许可协议,获得后者用于治疗PD的阿扑吗 啡皮下注射液在中国大陆、中国香港和中国澳门开发和商业化权益。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57