谁是下一个“PD-1”?非ADC药物莫属。
据数据统计,全球已有14款ADC药物获批上市。从靶点来看,Claudin18.2为国内继PD-1/PD-L1之后竞争最激烈的靶点之一。
10月22日,博安生物申报的首 款ADC新药BA1301注射液临床试验申请获受理,或为ADC赛道再添一把火。
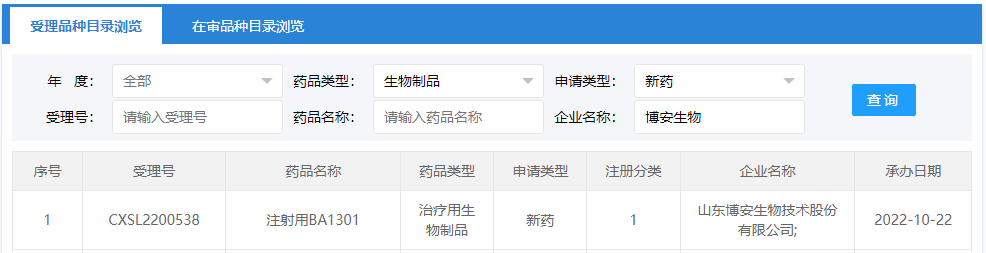
图1 CDE官网受理信息
图片来源:CDE
BA1301是一款靶向Claudin18.2的ADC新药,适应症为胃癌、胰 腺癌及食管癌,是博安生物7款在研创新抗体之一,也是博安生物申报的首 款ADC新药。
群雄逐鹿Claudin18.2-ADC
ADC药物是目前创新药领域的热门赛道,全球和中国都有大量药物在研。
据相关统计,2017年到2021年4年里,ADC药物交易首付款翻了2.5倍,交易总金额更是翻了3.84倍。未来,ADC药物的市场规模到2026年将超过164亿美元。
目前,全球已有14款ADC药物获批上市,II期至Ⅲ期产品梯队分布,还有大量处于I期阶段的ADC候选药物;从国内的研发进展来看,已有5款ADC药物获批上市,处于Ⅲ期阶段的ADC候选药物多达13种,预计国内在2-3年内即将迎来ADC药物的爆发期。
Claudin18.2靶点,为国内继PD-1/PD-L1之后竞争最激烈的靶点之一。
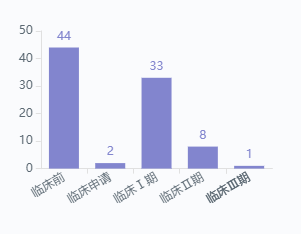
图2 Claudin18.2全球临床情况
图片来源:药智数据
目前全球超过40款产品进入临床阶段,适应症覆盖实体瘤、胰 腺癌、胃癌、食管癌、食管腺癌、胆道癌、胆囊癌、肺腺癌、结肠癌等等,天境生物、上海君实、再鼎医药、信达生物、科济生物、创胜医药、传奇生物等企业都在列。
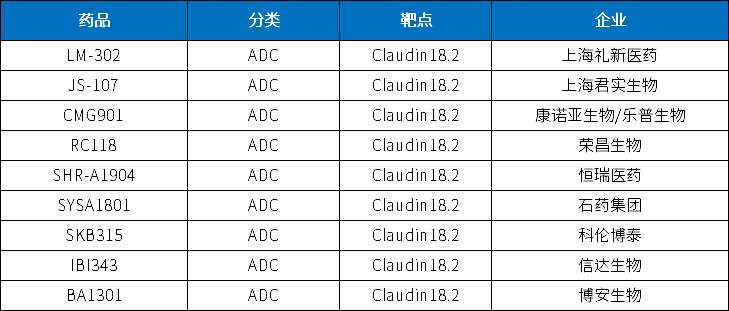
Claudin18.2-ADC已有恒瑞医药、石药、信达生物等10家药企先后布局,包括LM-302、JS-107、CMG901等在研药品(见表1)。
表1 国内部分Claudin18.2-ADC在研药物概览
博安生物有何优势?
博安生物成立于2013年,专业从事治疗用抗体开发,包括肿瘤、代谢、自身免疫及眼科等常见主要治疗领域,5月13日向香港联交所提交上市申请。
博安生物的产品管线涵盖创新抗体和生物类似药,现有1款商业化产品、5款在研生物类似药、7款在研创新抗体。

图3 博安生物产品管线
图片来源:博安生物官网
● 7款在研创新抗体
博安生物有7款在研创新抗体,分布在肿瘤、自身免疫、传染病领域。其中处于临床阶段的创新抗体包括:
新冠中和抗体LY-CovMab处于国内II期临床阶段;
Claudin18.2(ADCC)全人源单克隆抗体BA1105处于国内I期临床阶段,适应症为晚期胃癌、转移性胰 腺癌及食管胃交接部腺癌;
抗PD-L1/TGF-β双功能融合蛋白BA1201是博安生物首 个获批启动临床试验的双特异性抗体,适应症为小细胞肺癌、非小细胞肺癌、子宫颈癌、尿路上皮癌及晚期消化道癌;
广谱免疫肿瘤药物CD25抗体BA1106处于国内I期临床阶段;
BA1301注射液的临床试验申请今日(10月22日)获CDE受理,BA1301是靶向Claudin18.2的ADC新药,也是博安生物申报的首 款ADC新药;
此外,抗肿瘤CEA/CD3双抗BA1202、抗Claudin18.2抗体药物偶联(ADC)BA1301处在临床前阶段,自身免疫治疗领域的IL4R长效分子抗体BA2101处于IND阶段。
● 5款在研生物类似药
5款在研生物类似药中,代谢领域的BA6101(地舒单抗注射液,普罗力?生物类似药)的生物制品许可申请(BLA)于2021年10月14日获国家药监局受理,目前在审评审批中(补充任务审评中),预期会在2022年下半年获批上市(注册时光轴见下图):
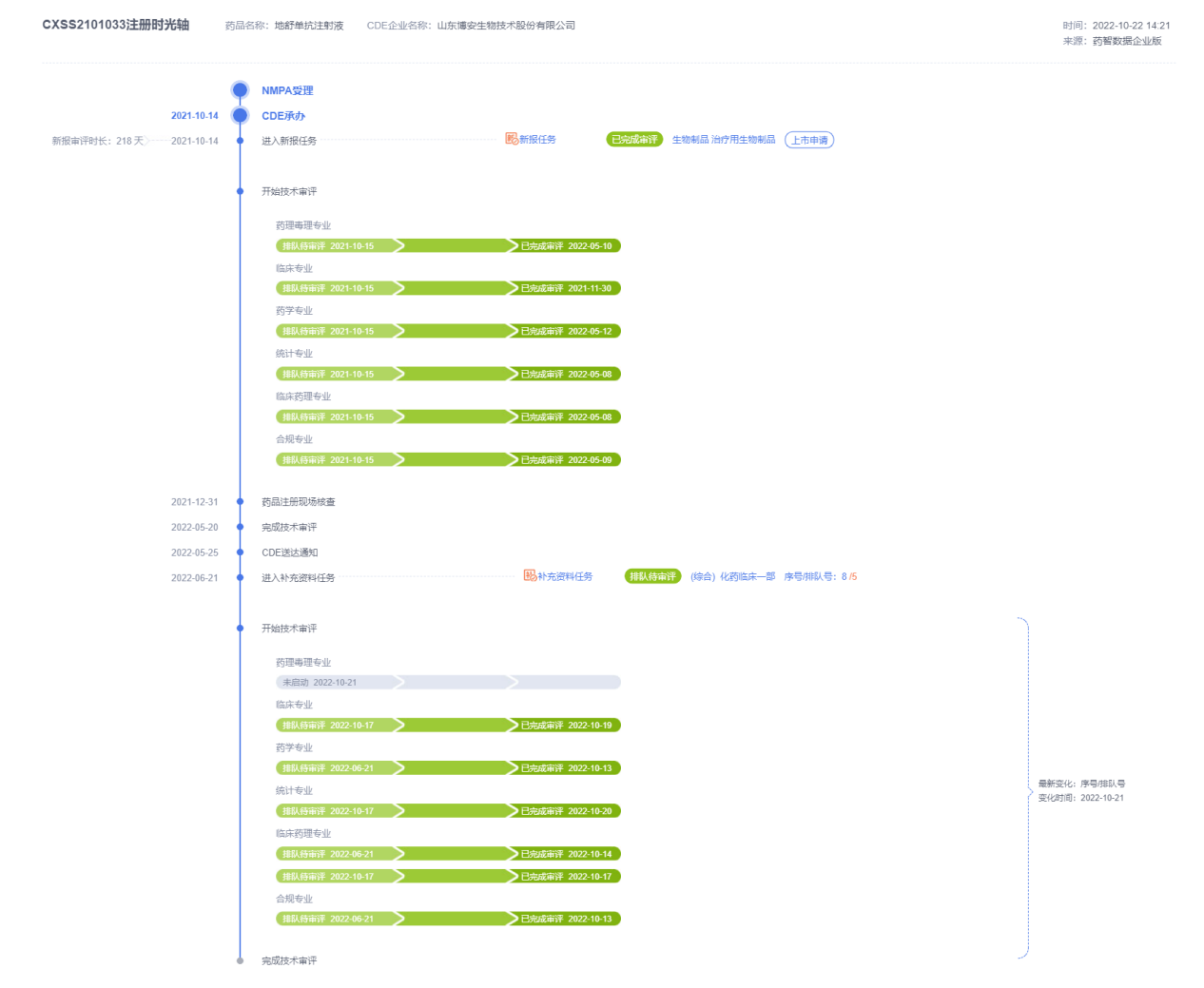
图4 地舒单抗注射液注册时光轴
图片来源:药智数据
肿瘤领域的BA1102(安加维?生物类似药)、眼科领域的BA9101(艾力雅?生物类似药)、代谢领域的BA5101(度易达?生物类似药)在华处于III期临床。
另外,BA6101和BA1102的海外开发均处于1期临床阶段。
● 商业化产品:博优诺
已实现商业化的博优诺?(贝伐珠单抗注射液)于2021年4月获批上市,主要用于治疗转移性结直肠癌、晚期转移性或复发性非小细胞肺癌、复发性胶质母细胞瘤、上皮性卵巢癌、输卵管癌或原发性腹膜癌及子宫颈癌。
2021年,实现销售收入1.59亿元人民币。
结语
尽管ADC药物赛道竞争激烈,但不同的癌种微环境不同、靶标不同。
ADC研发的根本原则就是立足于适应症本身,实现安全性和有效性的有机统一,尽可能提高患者的治疗窗口。
所以,泛偶联时代新入局者仍然有机会走出一条差异化道路。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57