研究表明,蛋白酪氨酸磷酸酶PTP和蛋白酪氨酸激酶PTK共同维持酪氨酸蛋白磷酸化的平衡,参与细胞信号转导,调节细胞的生长、分化和代谢。而酪氨酸磷酸化的失调被证实与多种疾病有关,如癌症、炎症和糖尿病等。近年来,大量的研究表明,酪氨酸磷酸酶SHP2与肿瘤的发生和进展密切相关。随着SHP2在各种类型癌症中的功能被揭示,人们普遍认为SHP2可能成为癌症治疗的潜在靶点。
SHP2的结构与生物学功能
1 SHP2的结构特征
SHP2作为一种非受体蛋白酪氨酸磷酸酶,在细胞信号转导的下游发挥重要作用。SHP2受生长因子、细胞因子和整合素受体的调控,参与细胞存活、增殖和迁移等细胞过程。SHP2的N端由两个SH2结构域(N-SH2和C-SH2)和一个具有催化活性的PTP结构域组成,C端包含两个p-Tyr位点(Y542和Y580)和一个富含脯氨酸的基序(图1)。
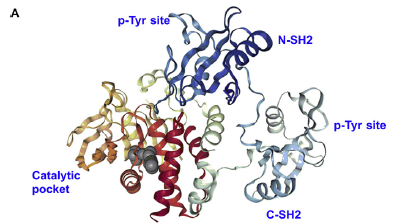
图1.SHP2的结构
在其失活状态下,SHP2蛋白被PTP域和N-SH2结构域催化表面的残基自动抑制,从而抑制SHP2蛋白的活性,限制底物进入催化位点。在生长因子或细胞因子的刺激下,SHP2通过其SH2结构域与磷酸酪氨酸位点结合而被招募,使SHP2发生构象变化暴露出催化位点,从而实现了对SHP2的准确催化活化,进而激活下游信号通路(图2)。
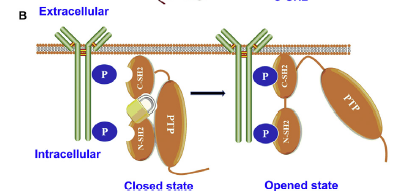
图2.SHP2的失活状态和活性状态
2 SHP2的生物学功能
SHP2在调节对生长因子、激素、细胞因子和细胞粘附分子的生物反应中至关重要。它是控制发育过程和造血功能的信号转导途径的关键组成部分。此外,它还调节多种细胞信号过程,包括控制代谢、细胞生长、分化、细胞迁移、转录和致癌转化(图3)。
SHP2是多个受体酪氨酸激酶RTKs的主要调节因子,主要促进细胞内的信号转导。其中,RAS/Erk通路是SHP2调控RTKs下游的主要信号通路,SHP2主要通过激活该通路来调节细胞的增殖、存活、分化、迁移和代谢。此外,SHP2还可以调节PI3k/AKT和JAK/STAT信号通路。
SHP2也参与调控T细胞中免疫检查点通路,如程序性细胞死亡-1(PD-1)通路。此外,SHP2是细胞粘附/迁移信号通路的正效应物,如:nf-κb、rhoa、hippo和wnt/-连环蛋白信号通路。然而,它也在某些信号通路中起负调控作用,如STAT3信号通路。此外,SHP2可以在细胞中同时具有致癌和肿瘤抑制剂的特性,这取决于它与之结合的信号通路和底物的性质。虽然SHP2的大多数功能通常需要其典型的磷酸酶活性,但它的一些功能仅依赖于其底物结合串联SH2结构域,而独立于PTP结构域。
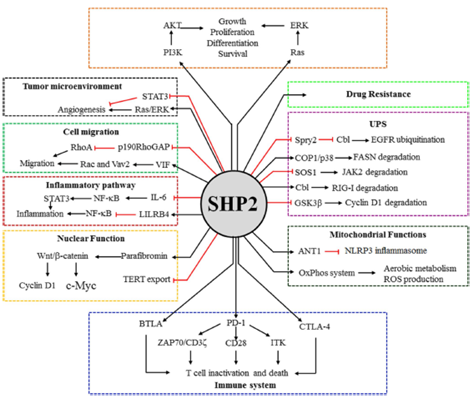
图3.SHP2多样的生物学功能
1、SHP2调节生长因子
SHP2是受体酪氨酸激酶RTKs信号通路的下游效应分子,通过激活生长因子EGF、成纤维细胞生长因子2(FGF2)、PDGF和肝细胞生长因子等,促进细胞生长。其中,RAS/Erk通路是激活RTKs下游,特别是生长因子受体的主要信号级联。SHP2作为一个中心角色,位于众多RTKs和RAS之间的节点。SHP2对于通过多种机制激活RAS/Erk信号通路至关重要。研究表明,SHP2是RAS完全激活的必要条件,并促进生长因子介导的RAS/Erk信号级联来激活许多效应因子。具体来说,SHP2直接参与调控细胞增殖或分化的转录因子。
此外,PI3k/AKT激酶的生长和生存信号通路也被激活的生长因子受体下游的SHP2调节。SHP2通过与GAB1/2和p85结合,调节Erk和AKT信号传导。有趣的是,研究发现SHP2在乳腺癌中是EGFR表达的正调控因子,而在前列腺细胞中,SHP2抑制后使EGFR表达上调。因此,抑制SHP2,干扰RAS/Erk通路信号传导,抑制肿瘤细胞生长,诱导癌细胞凋亡。
2、SHP2调节细胞因子反应
JAK/STAT信号通路是细胞外信号响应各种细胞因子和生长因子激活的主要途径之一。SHP2通过直接结合JAK和STAT蛋白的磷酸化酪氨酸残基来调控这一通路。它对细胞因子受体下游的JAK/STAT信号通路具有刺激和抑制双重作用
3、SHP2调节炎症反应
研究发现,SHP2在炎症和免疫反应的细胞因子通路中发挥作用。经典的nf-κb信号通路是由toll样受体(tlrs)和促炎细胞因子如tnf-α和il-1触发的,导致p65转录因子的激活,调节促炎和细胞存活基因的表达。SHP2通过促进il-1/肿瘤坏死因子(TNF)刺激的nf-κb激活和il-6的产生,进而促进炎症反应。当SHP2活性被抑制后,可以以nf-κb依赖的方式阻断炎症反应发生。另一方面,抑制PD-1或抑制SHP2与nf-κb通路激活因子的相互作用,可以阻断nf-κb依赖的细胞因子的释放,阻止炎症反应的发生。
4、SHP2调节免疫反应
PD-1通路是主要的肿瘤免疫逃避机制,它由T细胞共抑制受体PD-1及其天然配体PD-l1和PD-l2蛋白组成。研究发现,SHP2在免疫细胞中表达,并调节其发育、功能和分化。SHP2通过调控PD-1功能来实现对免疫反应的调节。此外,PD-1介导的SHP2激活也会导致TCR近端信号复合物的去磷酸化,PD-1介导的SHP2激活也能诱导B细胞受体(BCR)近端信号转导分子的去磷酸化。SHP2还通过去磷酸化il-1下游的T细胞激酶(itk)来促进PD-1的抑制功能。PD-1介导的SHP2激活的最终结果是通过减少细胞因子如ifn-γt细胞增殖来抑制和T细胞介导的免疫反应。
5、 SHP2调节细胞的粘附和迁移
研究发现,SHP2可以促进细胞的迁移和对生长因子受体激活的侵袭性反应。它可以调节迁移细胞中波形蛋白中间丝(vifs)的动态平衡。此外,SHP2还通过调节皮质蛋白的去磷酸化来调节PDGFR依赖的细胞迁移过程。SHP2也可以促进rhoa和FAK介导的细胞迁移过程。
6、 SHP2调节泛素-蛋白酶体系统
研究发现,SHP2还可以调节E3泛素连接酶的功能以介导底物蛋白的泛素化过程。SHP2可以通过其磷酸酶活性或适配器功能调节细胞中某些蛋白的泛素化,包括JAK2、EGFR、RIG-i、脂肪酸合酶和细胞周期蛋白D1。SHP2抑制GSK3β诱导的细胞周期蛋白D1的泛素化和降解。因此,SHP2可以调节细胞周期蛋白D1的表达和稳定性,从而促进细胞周期进程。此外,SHP2还可以促进CBL介导的EGFR泛素化过程。也有研究报道称,SHP2会破坏JAK2/socs1复合物的形成,并抑制随后的JAK2泛素化和降解。此外,SHP2还可以通过激活自噬过程来抑制奥沙利铂和氟尿嘧啶等化疗药物诱导的细胞凋亡。
SHP2在癌症中的作用
SHP2广泛的表达和在调控细胞生长、增殖、分化、迁移、凋亡和存活等多种细胞过程的主要生化途径中发挥关键作用。SHP2表达或活性的异常调控与疾病异常相关。SHP2过度表达或过度活化在多种实体肿瘤中被发现,包括肺腺癌、结肠癌、神经母细胞瘤、胶质母细胞瘤、黑色素瘤、肝癌、前列腺癌和乳腺癌等。
1 SHP2在癌症中的双面性
SHP2在多种人类癌症中过表达并发挥致癌作用,包括白血病、胰 腺导管腺癌、胃癌、乳腺癌、卵巢癌、肝癌、非小细胞肺癌、前列腺癌和黑色素瘤等。SHP2突变引起的激活在RTK驱动的致癌过程中起着重要作用。研究表明,SHP2是多种癌症关键致癌通路的组成部分,包括RAS/Erk、PI3k/AKT、JAK/STAT和nf-κb通路。SHP2控制着癌症的不同方面,包括细胞的生长和增殖、侵袭和转移、肿瘤微环境和免疫反应。
与其在血液癌和实体癌中的致癌作用相比,SHP2也被报道为在胶质瘤、骨髓瘤、食管鳞癌、结肠癌和肝癌中的肿瘤抑制因子。在肝癌中,SHP2通过激活RAS/Erk通路和PI3k/AKT/mTOR级联反应促进生长、增殖、粘附和迁移和转移,但可能通过下调il-6/STAT3炎症通路来抑制肝癌的发生。最近,pan等人也报道了SHP2在胶质瘤细胞中的抑癌作用,可能是通过STAT3和糖酵解途径。此外,PTPN11在软骨细胞中也起着肿瘤抑制因子的作用。总的来说,SHP2作为一种癌蛋白和一种肿瘤抑制因子,其肿瘤环境依赖方式的双重性质可以用于抗癌药物的设计与开发。
2 SHP2介导的耐药性
研究表明,SHP2过表达或异常激活介导了多种癌症的耐药性,包括转移性乳腺癌细胞、结肠癌和非小细胞肺癌。SHP2可以通过上调多个RTKs下游的AKT和Erk通路,降低癌细胞对临床使用的抗癌药物如奈拉替尼、奥沙利铂、奥西替尼、顺铂的敏感性。作为RTKs下游的一个关键节点,抑制SHP2是治疗大量RTK驱动的癌症以及对抗靶向抗癌治疗获得性耐药的理想策略。
SHP2抑制剂与其他抗癌药物的联用策略或许是一种富有治愈希望的新型抗癌策略。研究发现,SHP2抑制剂与治疗性使用的药物或其他抑制RTKs信号通路的小分子抑制剂的结合可以产生协同抗癌效应。此外,抑制SHP2还可以恢复癌细胞对靶向抗癌治疗的敏感性。
SHP2的抑制也可以消除对TNBC和结肠癌中的BRAF或MEK抑制剂的耐药性。一项研究发现,SHP099和MEK抑制剂联合应用在KRAS扩增的胃腺癌中也具有显著的体外抗肿瘤活性。此外,SHP2抑制剂与PD-1抑制剂联合使用也产生了协同效应,并克服了对PD-1抑制剂的耐药性。因此,靶向SHP2磷酸酶对于预防化疗和免疫治疗的内在和获得性耐药性以及消除其致癌功能,最终改善患者预后至关重要。
小结
多项研究均表明,SHP2是一个潜在的致癌靶点。在PTP家族中,SHP2是唯一一种可能导致癌症的蛋白质。同时,SHP2也是第一个被发现的致癌性磷酸酶。SHP2作为一个明星致癌靶点而备受瞩目,SHP2变构抑制剂的成功开发使SHP2完成了从“不可成药”靶点到抗癌明星靶点的转变。由于SHP2在机体发育及响应生长和刺激因子的生理和病理反应中起着重要作用。因此,靶向SHP2抑制剂可能存在一个有限的治疗窗口,如何降低SHP2抑制剂的毒 性也是研发人员后续需要解决的难题之一。此外,由于SHP2高突变率,开发SHP2降解剂也是未来研究方向之一。
参考文献:
1、A comprehensive review of SHP2 and its role in cancer. doi.org/10.1007/s13402-022-00698-1.
2、Tyrosine phosphatase SHP2 inhibitors in tumortargeted therapies. doi.org/10.1016/j.apsb.2020.07.010
3、Allosteric SHP2 inhibitors in cancer: Targeting the intersection of RAS, resistance, and the immune microenvironment. Curr. Opin. Chem. Biol. 62, 1–12 (2021)
4、Molecular mechanism of SHP2 activation by PD-1 stimulation. Sci. Adv. 6, eaay4458 (2020)
5、Emerging chemical scaffolds with potential SHP2 phosphatase inhibitory capabilities - A comprehensive review. Chem. Biol. Drug Des. 97, 721–773 (2021)



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57