多发性骨髓瘤(MM)是第二大最常见的血液系统恶性肿瘤,在临床病征上容易复发。而免疫调节药物(IMiDs)的引入可以说是多发性骨髓瘤治疗中可显著改善患者预后的一个重要里程碑。目前,IMiDs是新诊断和复发/难治性骨髓瘤治疗的基础。
研究表明,IMiDs主要通过结合CRL4 E3泛素连接酶 (CRL4CRBN) 复合物的底物受体蛋白Cereblon (CRBN) 发挥其抗骨髓瘤活性。通过结合CRBN,IMiDs改变了其底物的特性,导致骨髓瘤细胞存活所必需的蛋白质的泛素化和蛋白酶体降解。
随着IMiDs的成功,这引发了许多学者使用CRL4CRBN复合物的活性对治疗骨髓瘤的可能性作进一步探索。在本文中,探讨了骨髓瘤治疗领域中的新角色,即CRBN E3连接酶调节剂(CELMODs)的研究现状,这是新一代具有更广泛生物活性的IMIDs。此外,我们还讨论了一种新型靶向蛋白水解策略,即靶向蛋白水解嵌合体(PROTACs),利用CRL4-CRBN降解可能与骨髓瘤和其他恶性肿瘤的治疗有关的不可成药的蛋白质。
背景介绍
泛素-蛋白酶体途径在蛋白质降解过程中起着至关重要的作用。这一过程是由参与泛素激活酶(E1)、泛素结合酶(E2)和泛素连接酶(E3)的一系列酶反应介导的,这些酶反应在整个泛素化途径中会被ATP循环和激活,其中E3的作用是确定蛋白酶体中泛素化和随后降解的底物特异性。
人类基因组编码600多个E3泛素连接酶中,cullin-ring泛素连接酶(CRLs)是最大的E3连接酶家族,参与许多细胞稳态过程,如信号转导、细胞周期调控、DNA损伤反应、转录调控和胚胎发育等。CRL4 E3泛素连接酶是由锌指结构域蛋白(ROC1,也称为RBX1)、Cullin4(Cul4)支架蛋白和DDB1-Cul4相关蛋白组成的复合物,决定了CRL4 E3活性的底物特异性。cereblon(cereblon,CRBN)是CRL4 E3底物受体之一,对免疫调节药物等小分子的作用至关重要。通过IMiDs靶向CRBN可改变其对非生理蛋白的底物特异性,这些蛋白随后可被相应的蛋白酶体识别和降解。(图1A)
而这种作用机制在多发性骨髓瘤(MM)的治疗中显示出特别的相关性,所以 IMiDs的引入改变了MM患者的传统治疗药物,且显著改善了他们的预后。
虽然作用于CRBN的E3连接酶相关功能似乎是IMiDs 抗骨髓瘤活性的主要机制,但最近的报道表明,IMiDs也通过调节CRBN的其他特性(如伴侣功能)发挥作用。因此,为了强调更广泛的生物活性,下一代的免疫调节剂被称为“celmod”(Cereblon E3连接酶调节剂)。近年来,CRL4CRBN复合物和其他E3连接酶被广泛探索为通过异双功能小分子降解典型的“不可成药”蛋白的靶点,称为蛋白水解靶向嵌合体(PROTACs)。
本文主要介绍了在多发性骨髓瘤未来的治疗方法中,以CRBN依赖的方式调节CRL4CRBN E3连接酶活性的方法。
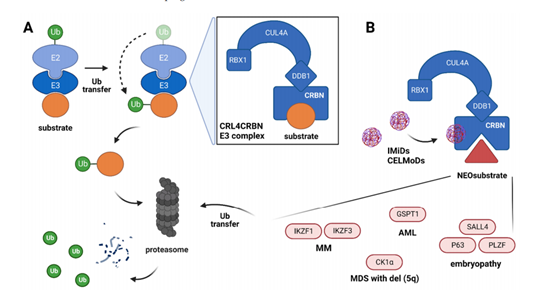
图1.CRL4CRBN E3连接酶复合物泛素化研究进展
免疫调节药物(IMiDs)
1、 IMiDs的作用机制
在2006年引入的沙利度胺是第一类的免疫调节剂,是MM治疗的里程碑之一。连同其新一代的衍生物里,如来那度胺和泊马度胺,以及蛋白酶体抑制剂和单克隆抗体,这些药物被用于治疗MM患者。沙利度胺及其类似物在阐明其作用机制之前,主要被认为是通过诱导IL-2(interleukin)和干扰素-γ等细胞因子的产生来调节T细胞、NK和NK-T细胞的功能。后来发现,沙利度胺及其类似物除了具有抗血管生成、破坏骨髓瘤细胞-骨髓基质相互作用和降低破骨细胞生成等作用外,故被称为免疫调节药物。随后研究表明,CRBN的表达是IMiDs抗骨髓瘤活性所必需的,因为研究发现CRBN基因的敲除导致了骨髓瘤细胞对来那度胺和泊马度胺产生了耐药性。
2014年,研究人员首次阐明了免疫调节剂的关键作用机制。两项研究表明,来那度胺与CRBN的相互作用改变了其底物特异性,从而诱导转录因子IZKF1/ 3的蛋白酶体依赖性降解。IKZF1和IKZF3被定义为CRBN的“新底物”,因为它们只有在存在IMIDs的情况下才成为CrBN的靶标。IKZF1/3的降解调控IRF4和MYC等其他基因的表达,对MM细胞的增殖和存活至关重要。而IKZF1/3-IRF4-MYC转录轴的破坏在MM细胞存活中起到了关键性作用 ,与原发性积液淋巴瘤细胞系的研究相反,其中IMiDs独立于IKZF1和IKZF3触发IRF4的表达下调。
最近的研究报道了多种潜在的IMIDs新底物,这些新底物需要在生理条件下验证并转化为IMIDs的临床应用。在IMiDs的作用下, CRL4CRBN E3连接酶的可以与新底物发生相互作用。在IMiDs活性下降解的新底物库的差异可能反映了在MM治疗期间观察到的各种不良事件。沙利度胺最常见的副作用是慢性轴突神经病变,而其他以骨髓抑制为特征的药物是最常见的毒 性。来那度胺和波马利度胺的骨髓抑制作用是指IKZF1的降解和随后下调转录因子PU.1和GATA1,前后两者分别导致中性粒细胞减少和血小板减少。由于与沙那度胺和波马利度胺相比,沙利度胺对IKZF的降解作用要低得多,它可能不会像它的新衍生物那样引起这种毒 性。
此外,IMiDs还可以调节CRL4CRBN E3连接酶的活性,以降解与特定新底物具有不同亲和力的各种蛋白。底物特异性的独特模式可能会转化为这些药物的临床疗效和毒 性特征的多样性。
2.2.IMiDs的临床疗效
尽管自来那度胺引入以来,沙利度胺在MM治疗中的作用一直在稳步下降,但在许多来那度胺供应不足的国家,沙利度胺、地塞米松和硼替佐米(VTD)的联合仍是初诊MM患者的关键方法,这些患者有资格接受大剂量化疗,随后进行自体干细胞移植(Auto-HSCT)。最近,Auto-HSCT前的VTD(沙利度胺联合长春新碱V以及吡喃阿霉素T和地塞米松D治疗方案)诱导已被证明在近95%的患者中发挥了有效反应(至少部分反应部分缓解),证实了以前报道的结果。
如最近的第3期Cassiopeia试验所示,通过添加Daratumumab可以进一步提高VTD在反应深度、可测量残留疾病(MRD)阴性率和无进展生存率(PFS)方面的临床益处,Daratumumab是一种针对CD38的一流单克隆抗体,即通常在MM细胞表面表达的抗原。
复发/难治性MM的治疗是临床实践中的一大挑战。对于以前没有接触过来那度胺的患者,单独使用来那度胺(特别是在虚弱患者中),或与卡非佐米(Aspire试验)Ixazomib(电气石试验),Daratumumab(Pollox试验)或Elotuzumab(Eloquent-2试验)联合使用是高度相关的治疗选择。
反过来,对于来那度胺难治患者,除了无IMID方案(如DKD[CANDOR试验],DVD[Castor试验]和KD[Endeavor试验]外,以泊那度胺为基础的方案也具有重要的临床价值。根据以前的治疗、表现状况和共病情况,复发/难治性MM患者可以单独或与抗CD38抗体(即达拉图单抗(Apollo试验)或伊沙妥昔单抗[ICARIA-MM试验]、伊洛妥珠单抗(Eloquent-3试验)、蛋白酶体抑制剂(即硼替佐米[OptimisMM试验][65]、卡非佐米[66]和伊沙佐米以及细胞毒 性药物(如环磷酰胺)联合使用,但这最终还是要取决于复发/难治性MM患者。免疫调节剂随机临床试验的结果总结在(表1)中。
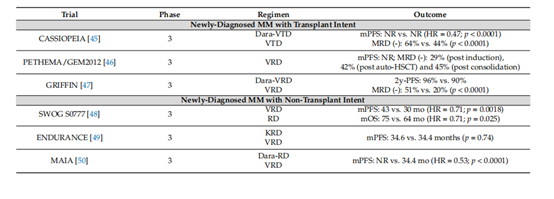
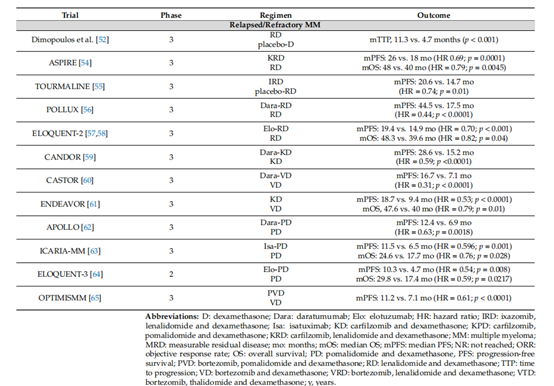
表1. IMIDS随机临床试验结果总结
CRBN E3连接酶调节剂(CELMODs)
1、Celmods的作用机制
尽管 关于免疫调节药物(IMiDs)之间的作用机制仍未完全阐明,但已有研究发现,关于CELMODs结构的第二个扩展区域(对应于沙利度胺中的邻苯二甲酰亚胺环)在每个 CELMoD 之间变化,并决定与 CRBN 和新的 CRL4CRBN E3 底物的相互作用,如图 2A、B所示。
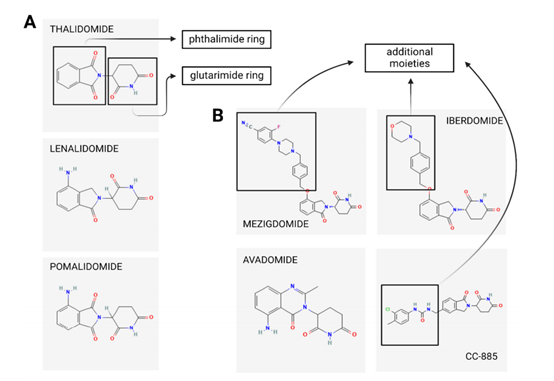
图2.IMIDs/CELMoDs在化学结构和IKZF1降解能力方面的差异。
区分CELMoDs与IMiDs的关键功能之一是CELMoDs增强了对CRBN的亲和力。尽管如此,与来那度胺或波马利多胺相比,CELMoDs的CRBN亲和力大约高10-20倍。与经典IMiDs相比,观察到CELMODs在IKZF1和IKZF3降解中更强的效力(图2C)。
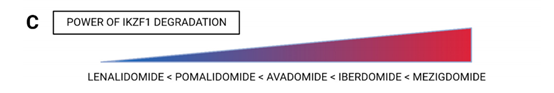
图2.IMIDs和CELMODs的在IKZF中降解效力的比较
3.2CELMODS的临床疗效
(1)CC-92480(美齐格米特)
最近报道了临床1/2阶段CC-92480-MM-002研究的初步结果。共19例复发/难治性MM患者在前一治疗中位数为3(范围,2-4)线后接受了CC-92480(美齐多米)、硼替佐米和地塞米松的联合治疗。
(2)伊伯多胺(CC-220)
根据1/2期CC-220-MM-001研究(NCT02773030)的初步结果显示,三联用伊伯多胺(CC-220)在重度预处理的MM患者中显示出良好的安全性和临床活性。Iberdomiddaratumumab-地塞米松(IBERDD)队列分别包括63%和58%的DaratumumaMability和四重难治(定义为对≥1个亚胺、1个PI、1个抗CD38单克隆抗体和1个类固醇的难治)患者。同样,在伊伯多胺-硼替佐米-地塞米松(IBERVD)队列中,难治性患者的比例很高(PI型难治性,76%;4型难治性,48%)。然而,IBERDD组和IBERVD组的客观反应率分别为35%和50%。
重要的是,对Ibervd的反应与Daratumumab和Bortezomiberefrictory无关。值得强调的是,很大一部分患者从以伊伯多胺为基础的治疗中获得了临床益处,因为获得了最小的反应或稳定的疾病。临床获益率和疾病控制率分别为47%和88%(IBERDD队列)和65%和85%(IBERVD队列)。细胞减少是联合治疗最常见的并发症。IBERDD联合治疗复发/难治性MM计划在第3期Excaliber-RRMM试验(NCT04975997)中与DRD进行比较。
此外,IBERVD作为不符合HDT-Auto-HSCT条件的MM患者的一线治疗方法,将在2期Borealis试验(NCT05272826)中进行评估。在1/2期CC-220-MM-001研究(NCT02773030)中,对伊伯多胺联合地塞米松进行了评估。107例入组患者几乎全部为三重难治(IMID、PI和抗CD38单克隆抗体难治),25%有髓外疾病,30%有高危细胞遗传学。依伯多胺和地塞米松治疗导致26%的患者有反应。中位PFS和OS分别为3个月和11个月。
有趣的是,以前接受过抗BCMA治疗的患者有类似的反应率(ORR为25%)人们对联合疗法的毒 性没有出现新的担忧。伊伯多米-地塞米松联合其他抗骨髓瘤药物如卡非佐米(NCT05199311,NCT02773030)、伊沙佐米(NCT04998786)、环磷酰胺(NCT04392037)和idecabtagene Vicleucel(Karmma-7试验,NCT04855136)的有效性和安全性目前正在几项早期研究中进行调查。
靶向蛋白水解嵌合体(PROTACs)
选择性蛋白质降解技术是一种极具临床潜力的的治疗策略,这种治疗方法不单单适用于MM患者。PROTAC策略是通过募集E3泛素连接酶,使其对目标靶向的蛋白质(POIs)泛素化和降解。近年来,随着对泛素化作用机制的广泛研究推动了PROTAC降解剂的发展。PROTAC分子由三个部位组成:
(1)一种与目标蛋白特异性结合的小分子化合物。
(2)一种与E3泛素连接酶特异性结合的化合物。
(3)一种连接靶蛋白配体和E3泛素连接酶配体的连接链。
PROTAC技术不需要与目标蛋白的较高结合力,因此在克服经典小分子蛋白抑制剂的潜在局限性(非共价抑制剂的瞬时靶向,蛋白质过表达或点突变引起的耐药性)方面具有很大的优势。这种新的策略可以有效针对“不可成药”靶点,如关键的致癌蛋白。
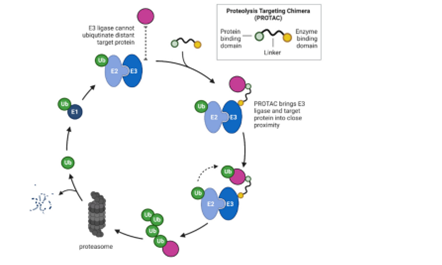
图3. PROTAC介导的靶向蛋白质降解的机制
目前,大多数PROTACs使用CRL4CRBN和VHL两种E3泛素连接酶作为招募连接酶。因此,IMIDs通常被认为是PROTAC“分子胶”部分的先驱,因为它们促进了CRBN与许多治疗相关的新底物的相互作用的发现。
2015年开发了第一个基于CRBN的靶向降解BRD4的PROTAC,以沙利度胺为CRBN E3泛素连接酶配体和溴结构域作为靶向蛋白。结果表明,DBET1在MM和AML细胞系中诱导高选择性的CRBN依赖性BET蛋白降解。基于CRL4CRBN-聚马立度胺相互作用的下一代PROTACs也针对BET蛋白(ARV825),该PROTAC显示出对MM细胞较强的抑制活性,并且在小鼠移植瘤模型中也表现出较好的抑制效果。此外,研究人员还开发了针对其他 MM 有前景的癌蛋白(如 CDK4 和 CDK6 和 MCL-1)的有效 PROTAC。
值得注意的是,使用 IMiD 或 CELMoD 治疗期间不可避免出现 MM 细胞的获得性耐药,这可能会造成CRBN 表达改变和编码 CRBN 的基因突变来影响基于CRL4CRBN E3 泛素连接酶的 PROTAC 的疗效。幸运的是,人类基因组编码了 600 多种 E3 泛素连接酶。到目前为止,只有少数几种被用于 PROTAC 的生成:VHL、MDM2、IAP(凋亡蛋白抑制剂)和 CRBN。
2022年8月,ARV-110(Adrent,NCT0388861)和ARV-471(Veritac,NCT04072952)的临床试验正在进行第二阶段试验。在血液学领域,具有IMiD样活性 (NX-2127) 的首 个口服BTK降解剂的人类1期试验目前正在招募复发/难治性B细胞恶性肿瘤患者 (nct04830137)。同样的,另一种基于IMID的BTK降解剂(NX-5948)已进入1期试验,用于复发/难治性B细胞恶性肿瘤的患者,包括原发性中枢神经系统淋巴瘤(NCT05131022)。最近,同样基于IMID的STAT3降解剂(KT-333)被批准用于治疗成人难治性B细胞非霍奇金淋巴瘤、T细胞淋巴瘤和实体瘤,正处于临床I期试验。
小结
IMIDS的引入彻底改变了多发性骨髓瘤的治疗前景,并与抗癌疗法联用显著改善了MM治疗结果。沙利度胺从致畸的“黑暗药物”到第一类IMID的发现,以及对其作用机制的广泛研究,为我们精确和重新理解蛋白质泛素化过程提供了一个全新的视角。尽管IMIDs是MM治疗中最重要的药物之一,但针对IMIDs的适应症也正在扩大到其他恶性肿瘤领域,如血液系统恶性肿瘤。例如,来那度胺对复发的套细胞淋巴瘤、滤泡性淋巴瘤和边缘区淋巴瘤均有疗效。期待更多的IMIDs获批上市,为患者带来福音。
参考文献
[1] Cullin-RING E3 Ubiquitin Ligases: Bridges to Destruction. Macromol. Protein Complexes 2017, 83, 323–347
[2] The Myeloma Drug Lenalidomide Promotes the Cereblon-Dependent Destruction of Ikaros Proteins. Science 2014, 343, 305–309.
[3] Cereblon loss and up-regulation of c-Myc are associated with lenalidomide resistance in multiple myeloma patients. Haematologica 2018, 103, e368–e371.
[4] Rapid Progress in the Use of Immunomodulatory Drugs and Cereblon E3 Ligase
Modulators in the Treatment of Multiple Myeloma. Cancers 2021, 13, 4666.
[5] CRL4 E3 Ligase Complex as a Therapeutic Target in Multiple Myeloma.[J] .Cancers (Basel), 2022, 14: undefined.



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57