2022年12月24日,根据CDE官网,阿斯利康新药依库珠单抗(Eculizumab)新适应症在国内申报新适应症。
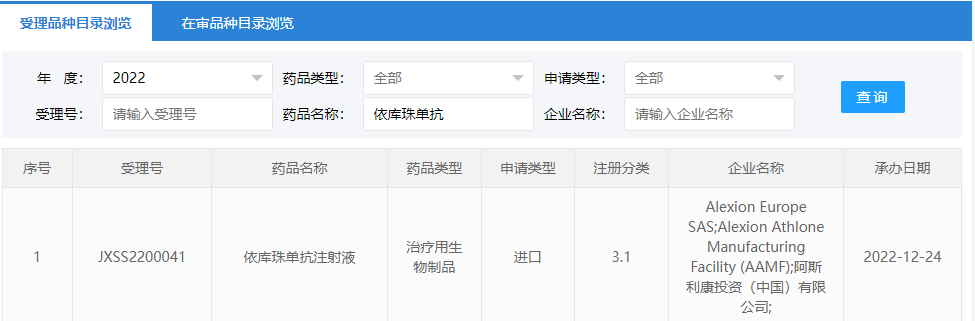
依库珠单抗是一款“first-in-class”C5补体抑制剂,该抗体对C5有高度亲和力,抑制末端补体蛋白C5。
目前,依库珠单抗已在美国、欧盟、日本等市场获批用于治疗:阵发性睡眠性血红蛋白尿症(PNH)、非典型溶血性尿毒症综合征(aHUS)、AchR抗体阳性全身型重症肌无力(gMG)成人患者,抗水通道蛋白-4 (AQP4) 抗体阳性视神经脊髓炎谱系障碍(NMOSD)成人患者4项适应症。
在国内,依库珠单抗于2018年9月获批用于治疗成人和儿童阵发性睡眠性血红蛋白尿症(PNH)和非典型溶血性尿毒症综合征(aHUS),2022年11月,阿斯利康宣布这两项适应症在国内上市,商品名为“舒立瑞”。
2022年12月24日,阿斯利康再次在国内申报新适应症。
补体系统药物国外市场正在兴起,
国内竞争小
自2007年依库珠单抗成为首 个获批的C5抑制剂,靶向补体系统的药物开发如火如荼。除了4种C1酯酶抑制剂(C1-INH)用于治疗遗传性血管性水肿(病因为C1酯酶抑制剂缺乏)外,还包括Ravulizumab、Pegcetacoplan、Sutimlimab、Avacopan、Avacincaptad等用于治疗阵发性睡眠性血红蛋白尿症,、非典型溶血性尿毒症综合征、全身型重症肌无力、视神经脊髓炎谱系障碍、冷凝集素病、ANCA相关血管炎和地图样萎缩等适应症。然而,国内目前只有依库珠单抗获批用于治疗阵发性睡眠性血红蛋白尿症和非典型溶血性尿毒症综合征。
补体系统已获批药物(美国和中国)
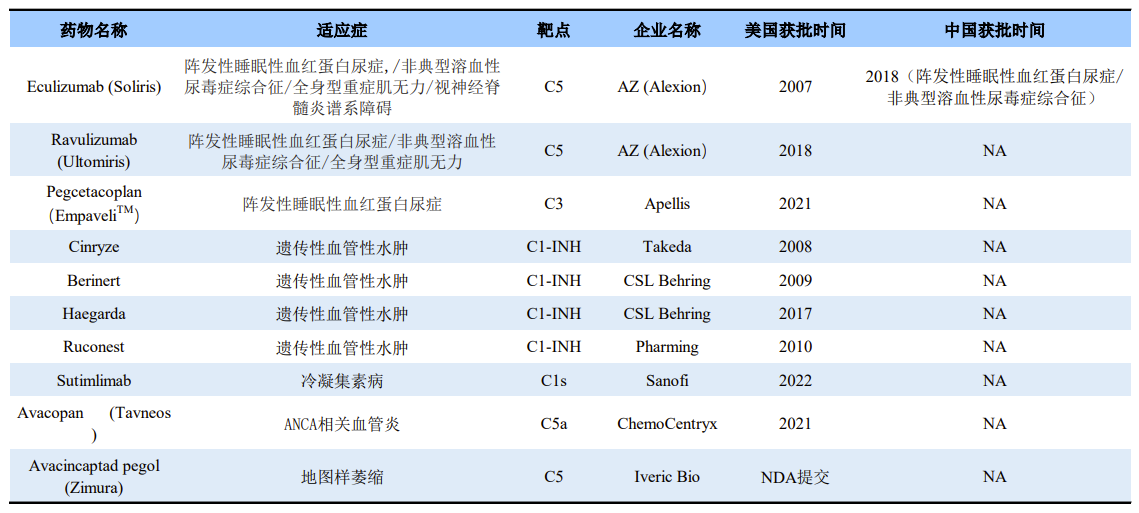
除了治疗遗传性血管性水肿的药物为C1-INH外,国外已上市药物的靶点主要集中在C1、C3和C5。正在开发的靶点还包括C5、C1s、CFB等。
补体系统药物开发,
不同靶点的适应症选择至关重要
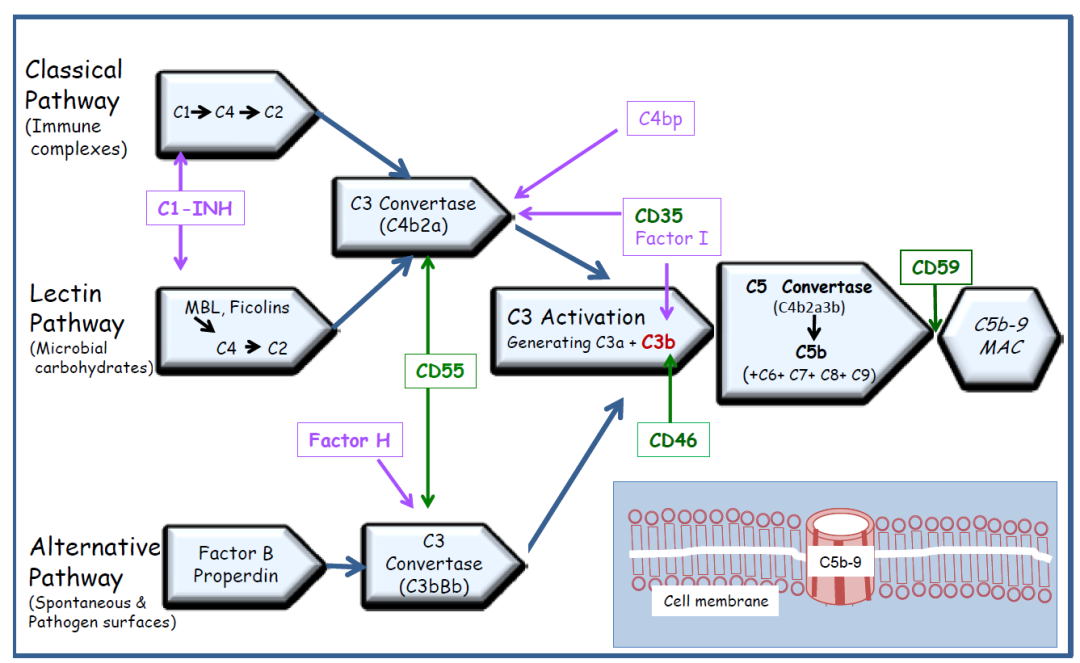
图1: 参考文献10
补体系统有三种通路——经典通路(Classical pathway)、凝集素通路 (Lectin pathway) 及旁路通路 (Alternative pathway)。如图1所示,C1处于经典激活通路的上游,C3属于三条通路的汇集点,而C5则位于通路末端。不同靶点的适应症选择有所不同。本文以溶血性疾病为例,阐述不同疾病所需的药物针对的靶点不同。
1 靶向C1s的Sutimlimab与冷凝集素病
靶向C1s的药物以赛诺菲的单抗Sutimlimab(商品名:Enjaymo?)为例,Sutimlimab是目前唯一获批用于治疗冷凝集素病的药物。
冷凝集素病(CAD)是一种淋巴组织增生性骨髓疾病,CAD导致的溶血完全依赖于补体。当所处环境温度下降于冷凝集素的反应温度范围内时,冷凝集素抗体就会与红细胞表面的同源抗原结合,募集经典补体途径的成分,C1酯酶激活C4和C2,产生C3转化酶,后者将C3裂解成C3a和C3b,最后包被C3b的红细胞被网状内皮系统中的巨噬细胞吞噬(即血管外溶血),如图2所示。因此,血管外溶血主要涉及经典补体途径,抑制经典途径的起始反应蛋白C1可以阻断下游溶血(图2),有效改善血管外溶血。
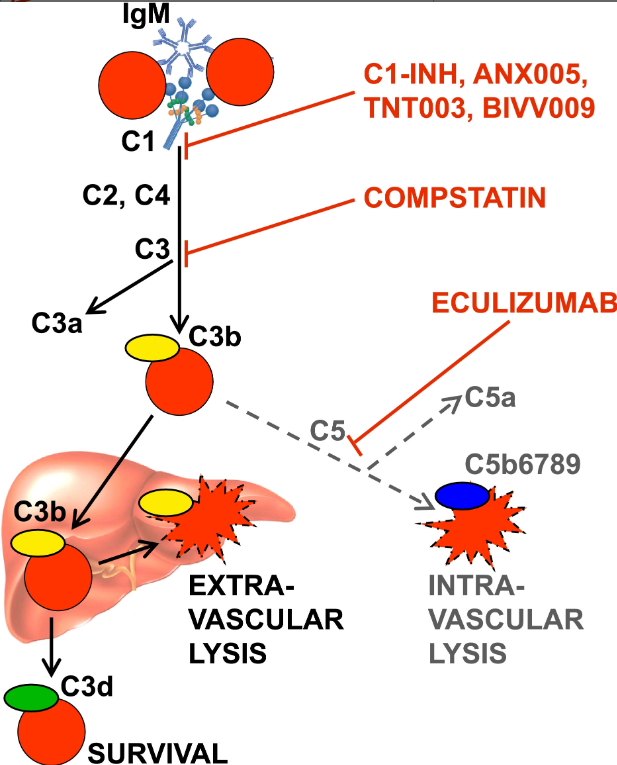
图2:参考文献11
Sutimlimab申请CAD适应症的关键临床试验是一项全球多中心、单臂、开放标签研究——CARDINAL研究。该项研究包括26周的A部分和持续2年的B部分,共纳入了24名CAD患者,纳入标准包括纳入前6个月内有输血史、血红蛋白≤10g/dL等。主要终点指标为满足复合指标的应答者的比例,应答者定义为满足血红蛋白≥12g/dL或较基线增加≥2g/dL,无输血,和未使用研究禁用的药物等三方面要求的受试者。结果提示,54.2%的受试者达到了应答指标,其中62.4%、70.8%、91.7%的受试者分别达到了血红蛋白、无输血、未使用研究禁用的药物指标。安全性方面,总体耐受性较好,常见治疗中发生的不良反应为呼吸道感染,病毒感染等。除此之外,Sutimlimab申请的支持性证据来源于一项Ib期开放标签研究。该研究纳入了6名CAD受试者,在4周给药后观察到受试者的血红蛋白增加中位数为3.9g/dL(图3),同时C1s、C3d、C4等补体蛋白均下降;停止用药后,这些变化慢慢恢复到基线水平。这项试验为Sutimlimab在CAD中的应用提供了生物学机制方面的证据。
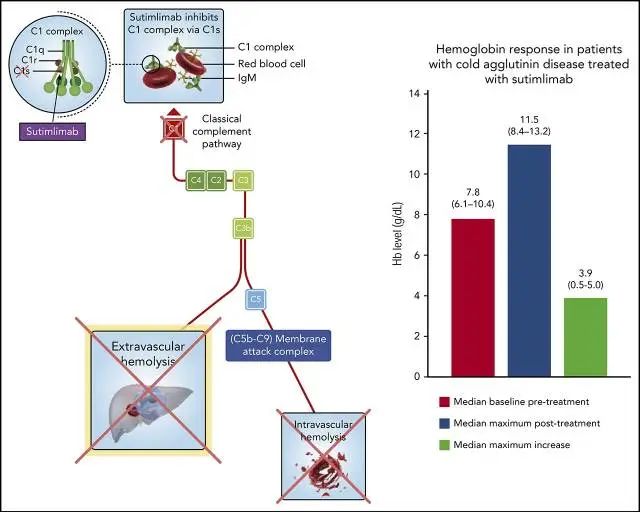
图3:参考文献12
从机制上预测,靶向C3的药物亦可发挥作用。目前,C3抑制剂Pegcetacoplan用于CAD的III期临床试验正在招募中,值得期待。另一方面,由于C5蛋白不在血管外溶血的通路上,靶向C5的依库珠单抗和对溶血的改善作用可能有限。Clinicaltrial.gov网站上显示依库珠单抗治疗CAD的II期临床研究(NCT01303952)已于2015年结束,而结果未公布,且Alexion公司官网上未显示CAD的管线,提示该试验大概率未看到积极结果。
2 靶向C5的依库珠单抗、靶向C3的Pegcetacoplan与阵发性睡眠性血红蛋白尿症
靶向C5的代表药物依库珠单抗,目前开发了阵发性睡眠性血红蛋白尿症(PNH)等适应症。补体介导的血管内溶血是PNH的主要病理机制,在正常情况下,血管内溶血由CD59阻断,CD59能阻止补体反应的最后一步,即阻止在靶细胞上形成孔的膜攻击复合体(membrane attack complex, MAC)(图1),而PNH患者红细胞缺乏将CD59连接至其表面的GPI锚而导致血管内溶血。靶向末端C5的依库珠单抗能阻止MAC复合物的形成,阻断血管内溶血。
一项为期26周的随机、双盲、安慰剂对照研究(TRIUMPH研究)和另一项为期52周的单臂研究(SHEPHERD研究)评估了依库珠单抗在伴有溶血的PNH患者中的安全性和有效性。在TRIUMPH试验中,与安慰剂组患者相比,接受依库珠单抗治疗患者的溶血显著减少(p<0.001),贫血改善,表现为血红蛋白稳定的患者增加和红细胞输注需求的减少(见表2)。在试验前按RBC输注分层的三个亚组(4-14个单位;15-25个单位;>25个单位)中均可观察到此效果。依库珠单抗治疗3周之后,患者报告的疲劳缓解且健康相关的生活质量得到改善。在SHEPHERD研究中,既往24个月内输血至少1次且血小板计数≥30,000/ml的患者接受了52周的依库珠单抗治疗。整个治疗期内可见血管内溶血持续减少(通过血清LDH水平测定),从而使得避免输血的情况增多,RBC输注的需求减少,患者疲劳减轻。详见下图。
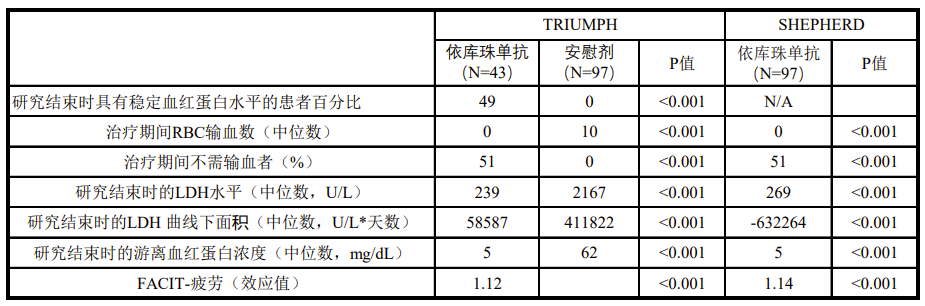
引自CDE依库珠单抗申请上市技术审评报告
Pegcetacoplan靶向C3,亦获批用于阵发性睡眠性血红蛋白尿症。PNH除了主要因C59减少导致血管内溶血外,也可因CD55减少导致血管外溶血。在正常情况下,血管外溶血可由CD55阻断,它阻止补体级联反应中MAC形成的上游C3和C5转化酶组装(图1)。PNH患者的红细胞表面若缺少CD55则会导致C3蓄积,发生血管外溶血。因此,靶向C3的Pegcetacoplan从致病机理上也可用于治疗发生血管外溶血的PNH。
Pegecetacoplan的关键临床研究是一项III期、随机、多中心、开放标签、活性对照试验,目的是比较依库珠单抗和Pegecetacoplan在使用依库珠单抗治疗且Hb 水平仍<10.5 g/dL的PNH患者中的有效性和安全性。受试者在合并使用Pegecetacoplan和依库珠单抗4周(run-in)后,进行16周的随机对照治疗,即随机接受Pegecetacoplan治疗或依库珠单抗单药治疗。主要终点指标是16周随机对照治疗后Hb水平。结果提示,主要终点指标达到显著差异,Pegecetacoplan组Hb水平较基线改变平均为2.4 g/dL,而依库珠单抗组为-1.5 g/dL,Pegecetacoplan组较依库珠单抗组Hb水平平均增加3.8 g/dL(95% 置信区间 [CI],2.33-5.34 g/dL)。这一结果说明Pegecetacoplan对于依库珠单抗难治性的PNH贫血患者具有一定有效性,提示这类患者的难治性贫血主要由于血管外溶血导致,而通过靶向C5无法完全抑制的血管外溶血可以通过靶向C3达到。
小结
依库珠单抗已被FDA批准的适应症还包括非典型溶血性尿毒症综合征,全身型重症肌无力和视神经脊髓炎谱系障碍,此三者均有补体介导免疫反应的参与,依库珠单抗可以通过抑制补体系统的末端环节,阻断补体级联反应,从而抑制炎症和膜攻击复合体形成,减少星形胶质细胞的破坏和神经元的损伤。
另一方面,已上市的C1s抗体Sutimlimab目前只成功开发了冷凝集素 这一适应症, 而其此前在大疱性类天疱疮、温性自身免疫性溶血性贫血、终末期肾病、特发性血小板减少性紫癜患者中均进行了探索性试验,后续未看到研究的继续推进,提示对于不仅仅涉及某一补体通路的疾病,单一性抑制某条通路也许不是最有效的途径。
总而言之,若整个补体系统均参与致病,则末端环节的抑制可能更有效;若主要为经典通路参与致病,则直接抑制经典通路的起始环节可能能带来最大的获益风险比。
补体相关疾病种类繁多,选择致病通路上最关键的环节或是成败的关键之一。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57