2023年1月12日,根据国家药品监督管理局药品审评中心(CDE)最新数据显示,CDE官网新增了4款1类新药的默示许可信息(不含补充申请)。经过梳理,这些1类新药适应症涉及乙肝、高眼压症、贫血、银屑病,靶点涉及PAPD5/7、EED、TYK2。
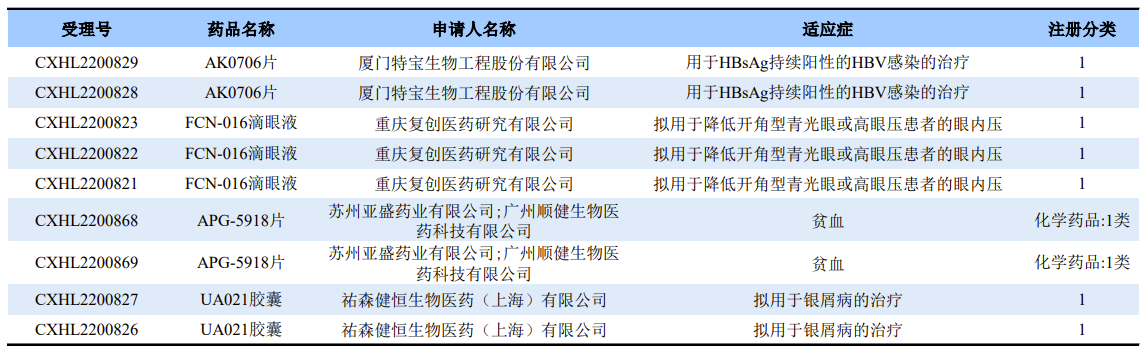
来源:CDE官网
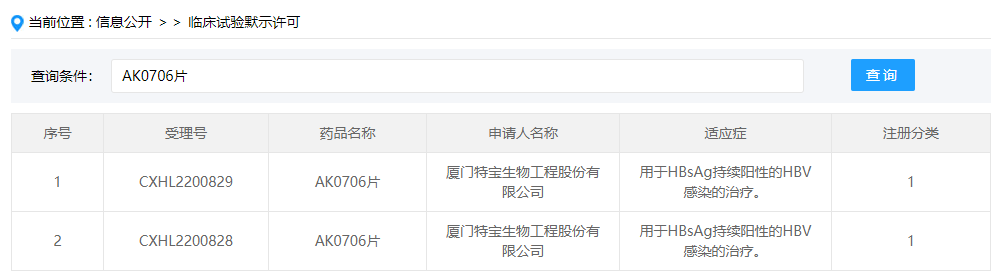
01 PAPD5/7抑制剂:AK0706片

AK0706片是爱科百发与厦门特宝生物合作开发的1类新药,这是该药在国内首次获批临床,拟开展用于HBsAg持续阳性的HBV感染的治疗的临床研究。2020年9月10日,爱科百发近日与特宝生物针对爱科百发自主研发的乙型肝炎(HBV)治疗新药AK0706在中国开发及商业化达成独家战略合作。AK0706是一种全新结构的小分子化合物,靶点为PAPD5/7,能够抑制乙肝HBeAg的活性,降低乙肝表面抗原的表达水平,有着不错的对抗慢性乙型肝炎的潜力。
最新数据显示,在我国现有的约8600万乙肝病毒携带者中,约2800万为需要治疗的乙肝患者,丙肝患者约有450万人。2020年全球有83万人死于肝癌,其中中国为39.1万,占47%。科学研究证明,我国80%的肝癌和乙肝相关,如果不采取有力的干预措施,这种状况将持续数十年,大量的肝硬化、肝癌病例将给患者家庭和社会带来沉重的经济负担。期待AK0706片能有新的临床进展,为国内乙肝患者带来新的曙光。
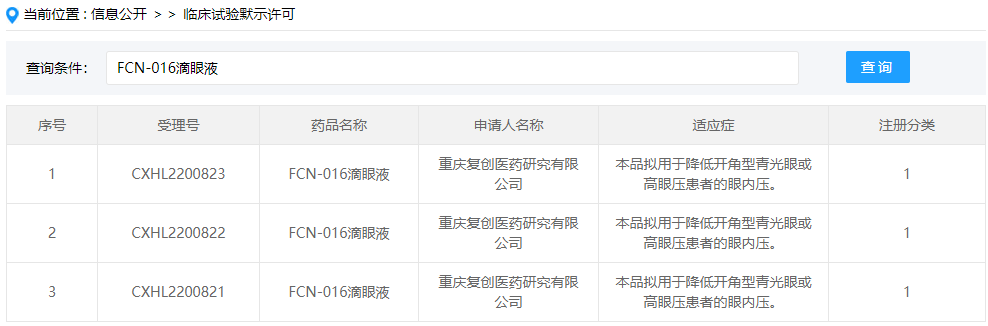
02 高眼压症新药:FCN-016滴眼液

FCN-016滴眼液是复创医药(复星医药子公司)开发的一款1类新药,目前靶点未知,这是该药在国内首次获批临床,拟开展用于降低开角型青光眼或高眼压患者的眼内压的临床研究。
青光眼是导致不可逆视力丧失和失明的主要原因之一。据统计,在2018年,全球有超过1.3亿青光眼患者。据估计,这一数字在2023年将达到1.48亿。这一进行性疾病的重要特征是眼压升高。无法控制的眼压升高会导致视神经损伤和视力丧失,降低升高的眼压目前是唯一防止青光眼疾病进展和视力丧失的有效方法。
目前国内已经有多家企业布局青光眼或者高眼压症新药的开发,例如欧康维视生物和Nicox公司联合开发的NCX470滴眼液在国内已经开展了III期临床,具有“best-in-class”的潜力;广州润尔眼科和中山大学中山眼科中心联合开发的ZOC2019619滴眼液在国内已经开展I期临床等。期待FCN-016滴眼液能积极推动临床进展,与国内其他青光眼或者高眼压症新药同台竞技,给国内患者带来更多的治疗选择。
03 EED抑制剂:APG-5918片

APG-5918是亚盛医药开发的一款选择性小分子EED抑制剂新药,此次临床默示许可适应症为贫血。APG-5918是具有高度结合亲和力,通过调节肿瘤组织表观遗传学及肿瘤微环境,在血液肿瘤、实体瘤和非肿瘤适应症(如贫血)上具有广阔的临床应用前景。目前,APG-5918在中美均开展了临床试验,研发进度令人瞩目。

2022年6月29日亚盛医药宣布,其在研原创新药胚胎外胚层发育蛋白(EED)抑制剂APG-5918获美国食品药品监督管理局(FDA)临床试验许可,将展开APG-5918的首次人体临床试验,探索治疗晚期实体瘤或血液恶性肿瘤的安全性、药代动力学和疗效。APG-5918是首 个进入临床阶段的中国原研EED抑制剂。2023年1月6日,APG-5918在国内开展的I期临床试验信息在CDE临床登记试验平台公示(CTR20230014),用于晚期实体瘤或血液系统恶性肿瘤患者的治疗。此次该药在国内取得贫血适应症的临床批件,足见亚盛医药对APG-5918临床用途不断拓展的信心,期待该药的后续的表现。
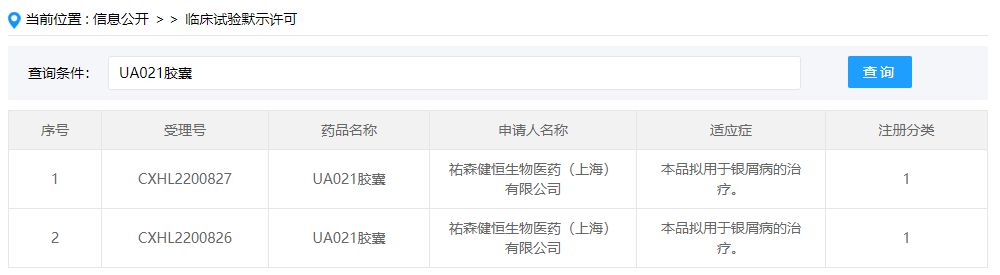
04 TYK2变构体抑制剂:UA021胶囊

UA021胶囊是祐森健恒开发的一款高效、高选择性及高口服生物利用度的TYK2变构体抑制剂,这是该药在国内首次获批临床,拟开展用于银屑病的治疗。
TYK2,即酪氨酸激酶2蛋白,属于JAK家族的一员。JAK家族包括TYK2和JAK1,JAK2,JAK3,其中TYK2是最早被发现的一个。也正是因为发现得早,当时还没有JAK家族的概念,所以并没有按照JAK来命名,这也使得TYK2成为了整个家族里一个特殊的存在。区别于其他靶向JAK蛋白的JAK抑制剂,TYK2抑制剂通过阻断TYK2蛋白及其介导的细胞信号而发挥作用。TYK2信号参与多种免疫相关疾病的病理生理过程,如银屑病、狼疮和炎症性肠炎(IBD)等,因此,该类抑制剂有望成为抑制银屑病、银屑病关节炎、克罗恩病和红斑狼疮等自身免疫性疾病导致的过度炎症的广泛选择。
目前,国内包括诺诚健华、高光制药、启元生物、百济神州、海思科等药企,都在开展TYK2靶点药物的研发,且已进入临床研究阶段。其中诺诚健华是国内TYK2靶点领域中进度相对领先的国产企业,目前有两款TYK2抑制剂已进入临床试验阶段,旗下ICP-332已启动已启动针对特应性皮炎的II期临床。期待祐森健恒的UA021胶囊能在自身免疫疾病领域的表现,给这一庞大的患者群里带来更为安全有效的治疗选择。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57