2023年3月3日,国家NMPA官网最新信息显示,恒瑞的抗PD-L1单抗阿得贝利单抗注射液、正大天晴的贝伐珠单抗注射液、海正生物的注射用曲妥珠单抗获NMPA批准同日上市。
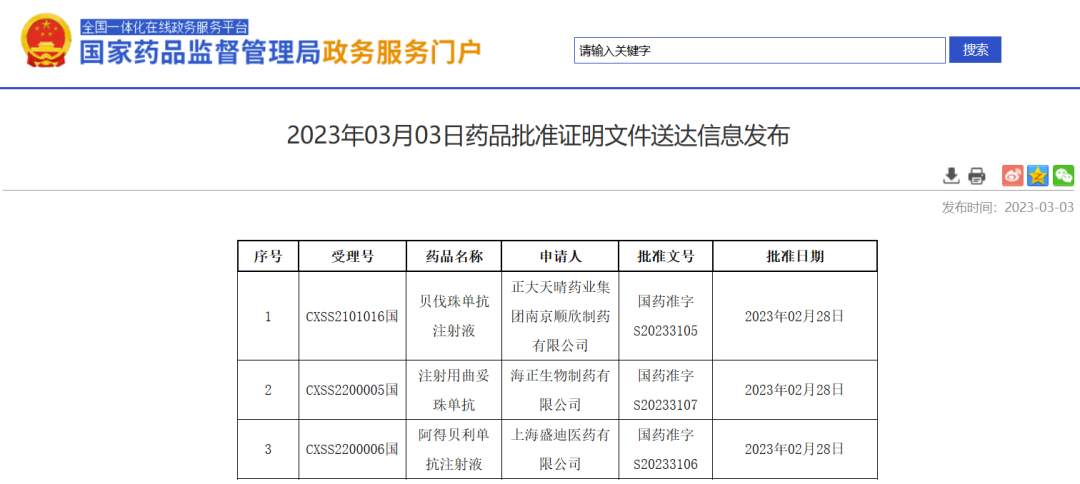
来源:NMPA官网
阿得贝利单抗
阿得贝利单抗(SHR-1316)是恒瑞医药自主研发的人源化抗PD-L1单克隆抗体,用于联合化疗一线治疗广泛期小细胞肺癌(ES-SCLC)。阿得贝利单抗能特异性结合PD-L1分子,从而阻断导致肿瘤免疫耐受的PD-1/PD-L1通路,重新激活免疫系统的抗肿瘤活性,达到治疗肿瘤的目的。
据悉,此次获批是基于一项名为CAPSTONE-1的多中心III期临床研究(NCT03711305),旨在评估阿得贝利单抗或安慰剂联合依托泊苷和卡铂一线治疗ES-SCLC的疗效和安全性。该研究由吉林省肿瘤医院程颖教授和中国医学科学院肿瘤医院王洁教授共同担任主要研究者(PI),中国47家医院共同参与。
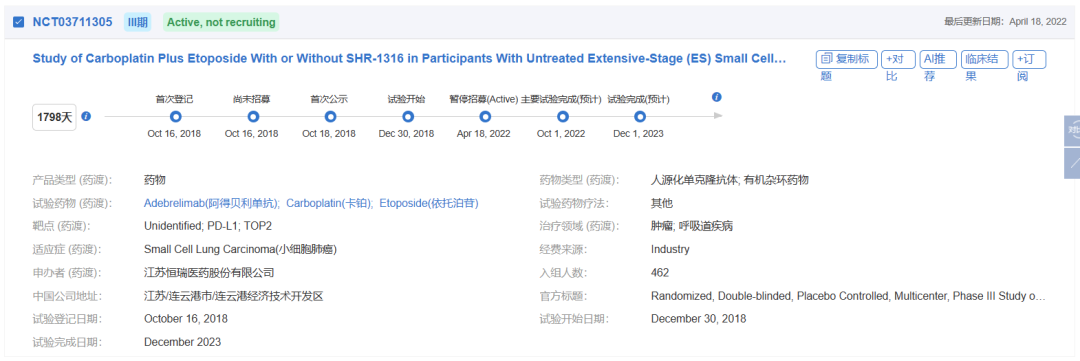
来源:药渡数据库
研究结果显示,中位随访时间13.5个月,相较于化疗对照组,阿得贝利单抗联合化疗可显著改善患者的总生存期:15.3个月vs12.8个月,2年生存率:31.3%vs17.2%,中位无进展生存期(PFS):5.8个月vs5.6个月,阿得贝利单抗显著降低患者疾病进展风险达33%。
此外,独立评审委员会(IRC)评估的阿得贝利单抗联合化疗组和安慰剂联合化疗组,6个月PFS率分别为49.4%、37.3%,12个月PFS率分别为19.7%、5.9%,ORR分别为70.4%、65.9%,缓解持续时间(DoR)分别为5.6个月、4.6个月,显示获益趋势。在试验中,阿得贝利单抗联合化疗的安全性与之前同类临床试验一致,与对照组相比,患者≥3级治疗相关不良事件发生率相当。上述结果已于2022年5月在国际学术期刊《柳叶刀-肿瘤学》(The Lancet Oncology)上发表。
根据药渡数据调研,目前多项阿得贝利单抗临床研究正在进行中,以评估其在各类实体肿瘤中的抗肿瘤作用。

来源:药渡数据库
小细胞肺癌(SCLC)是一种侵袭性强的肺神经内分泌肿瘤,分为局限期和广泛期,约70%的患者初诊时已经属于广泛期。ES-SCLC属于难治性、高侵袭性的肺癌亚型,患者治疗选择有限。早期经典一线治疗方案主要是依托泊苷联合铂类化疗,但化疗的生存获益有限。近几年,PD-L1抑制剂为代表的免疫检查点抑制剂为小细胞肺癌患者带来了新的希望。此次恒瑞的阿得贝利单抗获批上市,将为国内小细胞肺癌患者带来新的治疗选择。
贝伐珠单抗注射液
贝伐珠单抗是一种人源化抗VE GF单克隆抗体,血管内 皮生长 因子是肿瘤血管生长中所必需的一种蛋白质,贝伐珠单抗可以选择性结合VE GF,通过阻断VE GF与其血管内 皮细胞表面上的受体结合,阻断PI3K-Akt/PKB和Ras-Raf-MEK-ERK等信号通路的传导,从而抑制血管内 皮细胞的生长、增殖、迁移以及血管新生,降低血管渗透性,阻断肿瘤组织的血液供应,抑制肿瘤细胞的增殖和转移,诱导肿瘤细胞凋亡,从而达到抗肿瘤的治疗效果。
根据世界卫生组织国际癌症研究机构(IARC)发布的2020年全球癌症数据,2020年全球新发癌症病例1929万例,其中中国新发癌症病例457万例,临床上存在大量未被满足的医疗需求。原研药罗氏的安维汀(Avastin)已在全球获批用于治疗多项实体瘤,其中在中国已获批治疗非小细胞肺癌、转移性结直肠癌、胶质母细胞瘤、肝细胞癌、卵巢癌和宫颈癌等适应症。
2021年8月3日,正大天晴贝伐珠单抗注射液申报上市,申请适应症为非小细胞肺癌(NSCLC)。根据药渡数据调研,正大天晴成为国内继齐鲁制药、信达生物、复宏汉霖等企业之后,第9家该品种获批上市的企业,
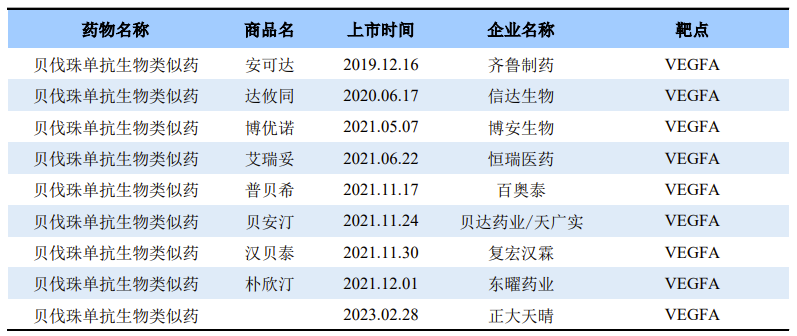
来源:药渡数据库
药渡数据-中国销量库统计数据显示,贝伐珠单抗自罗氏原研2010年在国内上市以来,销售一直呈极速上升态势,2021年销售总额超过75亿元,2022年前三季度销售额已经超过63亿元,全年销售将再创历史新高。值得一提的是,齐鲁制药的市场份额在2021年超过原研罗氏,市场占比超过50%。
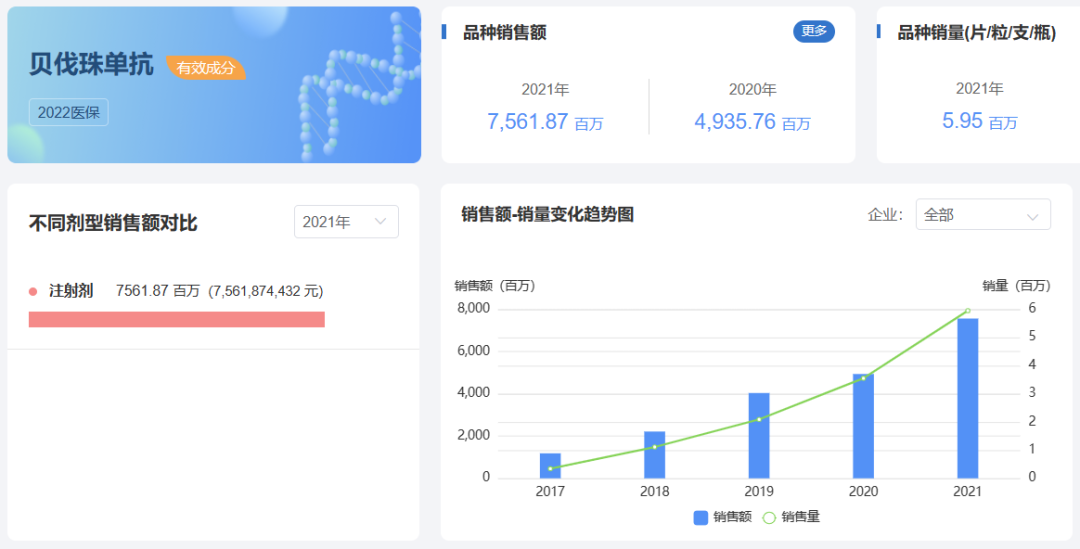
来源:药渡数据-中国销量库
注射用曲妥珠单抗
曲妥珠单抗是一种重组抗HER2(人类表皮生长 因子受体-2)人源化单克隆抗体,目前已成为HER2阳性乳腺癌和胃癌一线治疗的基石。作为一种受体酪氨酸激酶,HER2能够促进细胞生长和增殖,是乳腺癌患者的重要预后指标。
曲妥珠单抗能够特异性地与HER2的细胞外部位结合,从而抑制HER2过度表达的肿瘤细胞的增殖,其能够介导抗体依赖的细胞介导的细胞毒反应(ADCC)杀伤肿瘤细胞,从而改善HER2扩增的乳腺癌患者病情。此外,曲妥珠单抗联合化疗能够显著降低HER2阳性转移性胃癌患者的死亡风险,延长患者的总生存期。
注射用曲妥珠单抗(安瑞泽®,规格150mg/瓶)由博锐子公司海正生物研发,此次已获批原研药赫赛汀®在中国的全部适应症,HER2阳性的转移性乳腺癌、HER2阳性的早期乳腺癌以及HER2阳性的转移性胃癌。
博锐生物坚持以高品质、高标准推进药物研发,针对安瑞泽®与原研药赫赛汀®开展了I期药代动力学比对研究和III期临床有效性比对研究,同时观察安全性和免疫原性。研究结果表明安瑞泽®在质量、有效性、安全性、药代动力学和免疫原性方面与原研药赫赛汀®均高度相似。
WCRF统计数据显示,乳腺癌现已成为中国女性较常见的恶性肿瘤之一,中国新发乳腺癌约为42万例,HER2阳性乳腺癌约占乳腺癌总发病数的20%-25%。目前曲妥珠单抗已被纳入《国家医保目录》及《国家基本药物目录》,药品可及性进一步得到保障。曲妥珠单抗生物类似药也已先后被《CSCO乳腺癌诊疗指南(2021版、2022版)》,《CSCO胃癌诊疗指南(2021版、2022版)》纳入相关推荐用药。
药渡数据-中国销量库统计数据显示,曲妥珠单抗国内市场份额由2家瓜分,分别是原研企业罗氏(86.56%)和复宏汉霖(13.44%)。
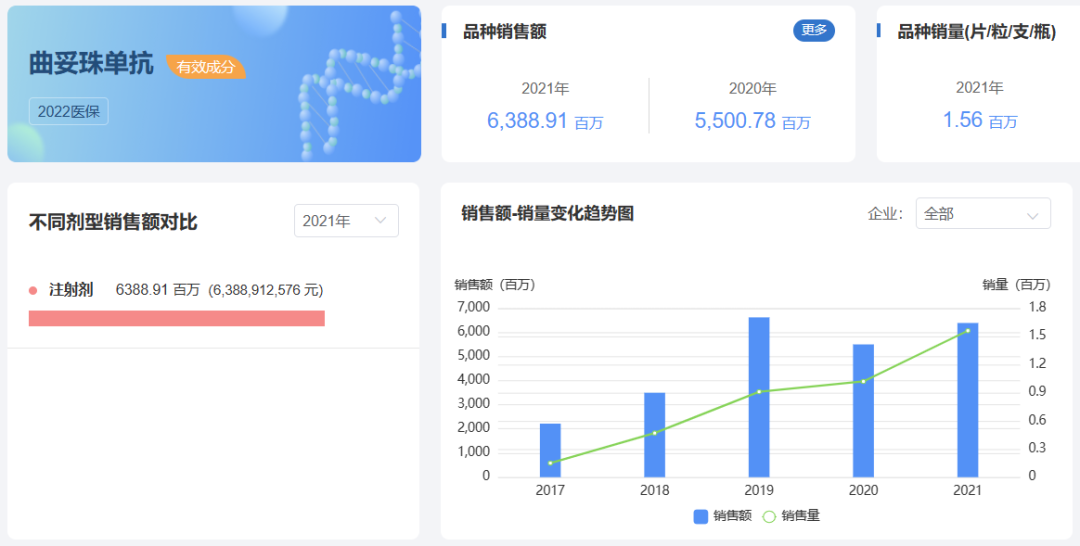
另据Frost&Sullivan统计,我国赫赛汀®生物类似药市场的销售额预计将以146.6%的复合年增长率从2019年的1亿元增长至2023年的38亿元。此次海正生物的曲妥珠单抗生物类似药获批,是继复宏汉霖的汉曲优®(2020年8月12日获批上市)后第二个获批上市的曲妥珠单抗生物类似药,安瑞泽®市场潜力值得期待。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57