•2022年,对于再鼎医药而言具备重要意义。
一则,自2022年11月11日起,再鼎医药成功摘掉了“B”标签,意味着公司的营收业绩、经营状况得到了认可;二则,再鼎医药2022年业绩也确实取得了良好成效。
2022年,再鼎医药实现总收入2.15亿美元,同比增长49%。其中,2022年第四季度的总收入6260万美元,同比增长41.7%。
更值一提的是,2022年再鼎医药亏损净额为4.433亿美元,相比2021年7.045亿美元的亏损净额减少了37.08%,这主要归因于与新商务拓展活动相关的付款减少。
再鼎医药创始人、董事长兼首席执行官杜莹博士表示,“我们预计今年将实现商业化盈利,并计划在2025年年底之前上市另外至少8款产品,实现企业整体盈利。”
再鼎医药之所以能在2025年实现盈亏平衡,与现有产品销售放量、在研管线迎来收获期不无关系。
已上市产品收入2.127亿美元均实现显著增长
2022年,再鼎医药四款已上市产品的销售收入均实现了不同程度的增长。
►尼拉帕利
则乐(尼拉帕利)是一种高效、选择性的每日一次口服小分子聚(ADP-核糖)PARP1/2抑制剂。肿瘤细胞DNA受损后,PARP抑制剂可阻断受损肿瘤细胞DNA修复功能。再鼎于2016年从Tesaro(后被GSK收购)获得尼拉帕利在大中华区(中国内地、香港、澳门和台湾地区)的独家许可。
目前,尼拉帕利已在美国、欧洲、加拿大、澳大利亚、大中华区和其他一些国家/地区上市,是唯一获得FDA、EMA和NMPA批准,无论患者生物标志物状态如何均可单药用于晚期卵巢癌一线维持治疗的PARP抑制剂。
2022年,则乐销售收入1.452亿美元,上年同期为9357.9万美元,同比增长55.2%。
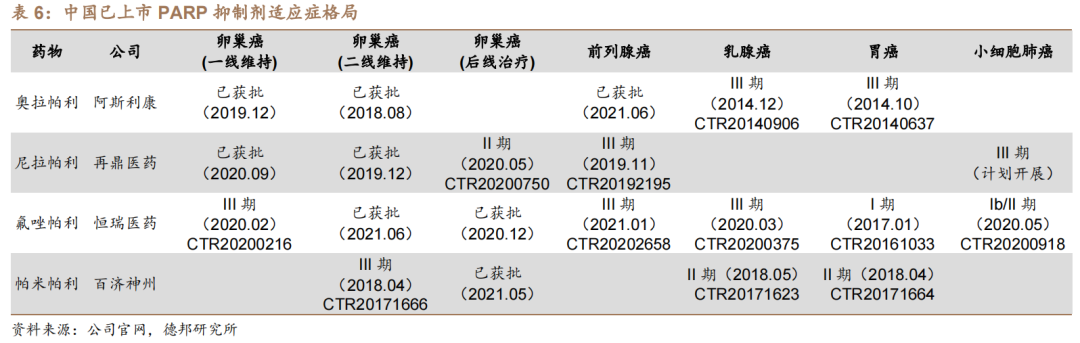
从竞争格局看,除了则乐以外,目前国内还有三款PARP抑制剂获批上市,分别为奥拉帕利(阿斯利康)、氟唑帕利(恒瑞医药)、帕米帕利(百济神州)。另外,据德邦研究所研报显示,目前中国还有超过10款在研PARP抑制剂已进入临床阶段。
►爱普盾
爱普盾(Optune)是进行肿瘤电场治疗(TTFields,一种干扰肿瘤细胞分裂的电场疗法)的新型抗癌疗法。2018年,再鼎从Novocure公司获得在大中华区商业化爱普盾的独家许可。
目前,爱普盾和Optune Lua已在美国、大中华区、欧洲和日本等国家和地区获批或上市用于治疗新诊断及复发胶质母细胞瘤(GBM)及恶性胸膜间皮瘤(MPM)。除GBM外,再鼎还将与Novocure合作开展TTFields用于多种实体肿瘤适应证的研发项目。
2022年,爱普盾销售收入4730万美元,上年同期为3890.3万美元,同比增长21.6%。
再鼎医药的产品管线(部分)
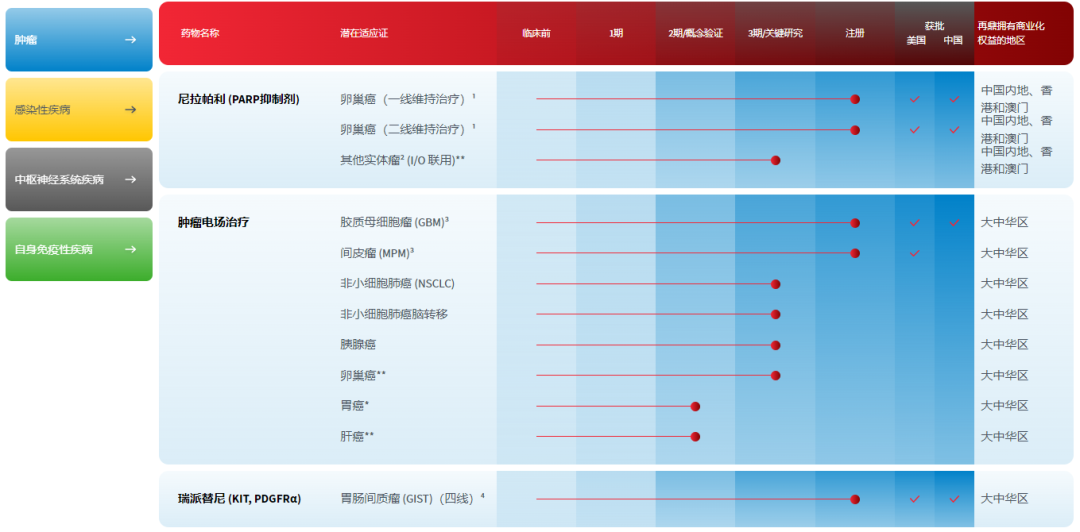
来源:公司官网
►擎乐
擎乐(瑞派替尼)是一款口服的酪氨酸激酶开关控制抑制剂,通过双重作用机制调节激酶开关口袋和活化环,从而广泛抑制KIT和PD GFRα突变激酶。2019年,再鼎从Deciphera公司获得瑞派替尼在大中华区开发和商业化的独家许可。
目前,擎乐已在美国、加拿大、澳大利亚、大中华区和其他一些国家/地区上市,是目前唯一在美国和中国获批用于治疗所有曾接受过三种或以上激酶抑制剂治疗的晚期胃肠间质瘤(GIST)患者的疗法。
2022年,擎乐实现销售收入1500万美元,上年同期为1162万美元,同比增长28.7%。
►纽再乐
纽再乐(甲苯磺酸奥马环素)是一款每日一次口服或静脉给药的抗生素,用于治疗社区获得性细菌性肺炎(CABP)及急性细菌性皮肤和皮肤结构感染(ABSSSI)的成人患者,包括院内感染和社区感染。
2017年,再鼎从Paratek Pharmaceuticals获得在大中华区独家开发、生产和商业化甲苯磺酸奥马环素的权利。2022年,纽再乐实现销售收入520万美元,2021年接近零收入。
布局差异化管线
多款核心产品进入商业化进程
以License in模式起家的再鼎医药,如今经过持续的研发投入,已经确立了“授权引进”和“自主研发”双轮驱动的研发策略。
根据财报显示,2019年、2020年、2021年再鼎医药分别投入研发1.42亿美元、2.23亿美元、5.73亿美元,同比增长18.24%、56.6%、157.42%。2022年,再鼎的研究与开发(研发)支出为2.864亿美元,2021年同期为5.733亿美元。
研发支出的减少,主要是由于新的授权引进协议的预付款减少,部分被增聘研发人员的工资及工资相关开支的增加、正在进行及新启动的后期临床研究项目增加的相关费用抵销。除去新的授权引进协议的预付款,2022年再鼎的研发支出为2.564亿美元,而2021年为2.520亿美元。
目前,再鼎医药拥有28个丰富的产品管线,其中9个全球权利的内部研发项目,适应症领域涵盖肿瘤、感染性疾病、中枢神经系统和自免免疫性疾病等,其中有不少核心品种具备潜在全球同类最 佳/同类首 创的潜力。
►Adagrasib
从Mirati Therapeutics引进大中华区的Adagrasib,是KRAS G12C的一种口服小分子抑制剂,在单一治疗和联合治疗领域都有广泛的研发,目前正在进行针对治疗KRASG12C突变的非小细胞肺癌、结直肠癌、胰 腺癌和其他实体瘤的开发,券商预计销售峰值超过20亿元。
再鼎医药管线布局
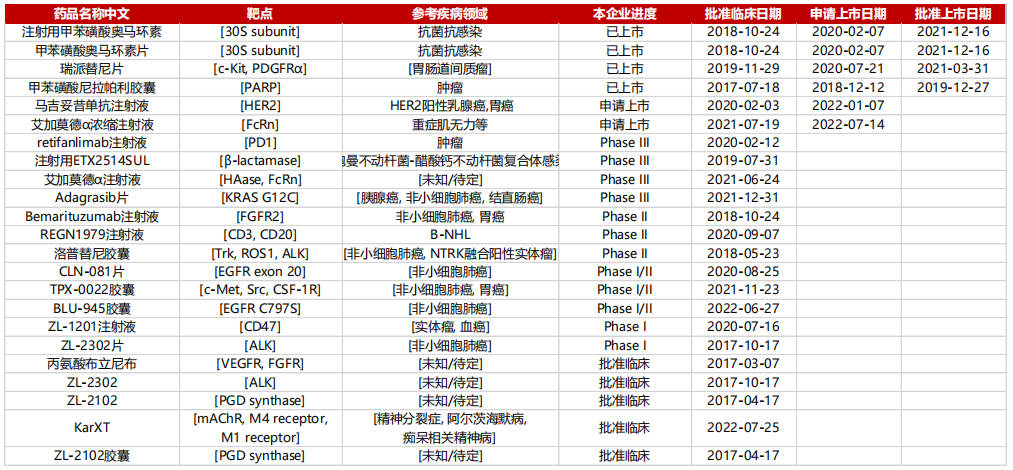
来源:中泰证券研究所
►KarXT
在中枢神经系统领域,KarXT是一款口服M1/M4型毒蕈碱乙酰胆碱受体激动剂,正在开发用于治疗精 神和神经系统疾病,包括精 神分裂症和痴呆相关精 神病性障碍。再鼎于2021年从Karuna Therapeutics获得在大中华区开发、生产和商业化KarXT的权利。
据统计,中国国内精 神分裂症患者群体规模在800万左右,加之市场缺乏有效新药,市场存在强烈需求。目前,再鼎计划于2023年年中向FDA提交KarXT用于治疗精 神分裂症的新药上市申请,有望成为50年来首 个治疗精 神分裂症的创新药物。
►Tivdak
从Seagen引进大中华区的明星ADC药物Tivdak(Tisotumab vedotin),由Genmab研发的针对组织因子(TF)的人源单克隆抗体Seagen的ADC技术组成,该技术利用蛋白酶可切割的连接子将微管破坏剂(MMAE)共连接到抗体。此前,Tivdak已于2021年获得美国FDA批准用于治疗在化疗期间或之后出现疾病进展的复发或转移性宫颈癌成人患者。
►Bemarituzumab
再鼎医药向Five Prime(后被安进收购)引进大中华区的Bemarituzumab(抗FGFR2b)是一款Fc段改良的单克隆抗体,目前正在开展用于FGFR2b过表达的晚期胃癌一线患者的全球3期临床研究和中国桥接试验。
►Odronextamab
CD20/CD3双抗Odronextamab由再生元研发,再鼎于2020年4月获得其在大中华区独家开发和商业化的权利,目前正在进行一项潜在关键的B细胞非霍奇金淋巴瘤(B-NHL)II期研究,包括滤泡性淋巴瘤(FL)、弥漫大B细胞淋巴瘤(DLBCL)和边缘区淋巴瘤(MZL),计划于2023年下半年提交用于治疗R/R DLBCL和R/R FL的生物制品许可申请。
►艾加莫德
在自身免疫疾病领域,从Argenx引进大中华区的艾加莫德(Efgartigimod),是中国首 款申请上市的FcRn拮抗剂,有望于2023年获批上市,目前正在开展包括全身型重症肌无力(gMG)、原发性免疫性血小板减少症(ITP)、慢性炎性脱髓鞘性多发性神经根神经病(CIDP)和寻常型天疱疮(PV)等多款适应症,券商预计销售峰值超过20亿元。
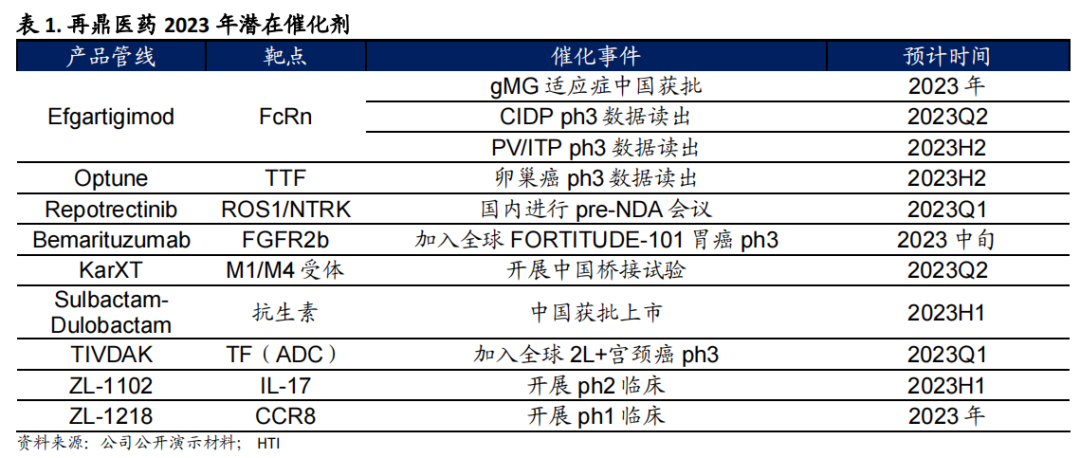
从Biotech成长为Big Pharma
现金流,是创新药企业的“命脉”。
截至2022年12月31日,再鼎医药的现金及现金等价物、短期投资和受限制现金总计10.093亿美元,资产负债状况稳健,现金可支撑其运营至2025年。
在商业化生产方面,目前再鼎已经在苏州建立了小分子制剂商业化工厂和生物制剂中试生产工厂。
其中,小分子工厂于2017年建成,用于生产临床和商业化用途的口服固体制剂,每年可生产硬胶囊剂约2000万粒,片剂约5000万片;大分子制剂中试生产工厂于2018年建成,生产用于临床研究的材料,生产面积4200平方米,配备先进的GE Flexfactory一次性生产线。
总结来看,再鼎医药2022年交出了不错的成绩单,加之凭借丰富的研发管线、商业化及生产能力,正逐渐成为一家全球领先的集研究、开发、生产和商业化一体的生物制药公司。
参考资料
1.再鼎医药官网、2022年财报公告
2.《再鼎医药-9688.HK-自研合作双驱动,管线价值有望集中兑现》,德邦证券



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57