介绍
药物递送系统是指将药物输送到靶部位发挥作用,而不会对正常细胞产生毒副作用。其目的是降低毒副作用,增强稳定性,提高生物利用度,减少降解,维持稳定有效的血药浓度。构建药物递送系统有两种策略:一种是利用递送载体提高药物的稳定性,另一种是通过共价修饰药物来暂时抑制药物活性的前药策略(prodrug)。前药策略可以避免递送载体引起的免疫原性和毒 性等安全性问题,减轻患者对递送载体的代谢负担,因此具有广泛的应用。
多肽药物复合物(PDCs)是靶向药物递送系统中的一种新兴前药策略,它由多肽、连接子和药物三部分组成,其作用机制因多肽和连接子的种类各异而不同——首先,多肽通过识别细胞表面的特异性受体进入细胞,接着连接子在一定刺激下裂解,释放药物并发挥治疗作用。这种前药策略可以潜在地提高药物的靶向性,减少对其他细胞的毒副作用。
与构建策略相似的ADC(抗体偶联药物)相比,PDC具有独特的优势:(1)多肽分子尺寸小,载药量高,更容易穿透肿瘤间质,进入肿瘤细胞。(2)多肽是高度可生物降解的,不会在体内引发任何免疫原性反应。(3)部分靶向肽可以通过改变药物的细胞进入机制,消除肿瘤细胞的耐药,实现对耐药肿瘤的有效杀伤。(4) PDC的短肽特性使其结构更加灵活,更容易修饰和偶联,可以与化学、蛋白质、肽类药物等多种药物偶联,制备靶向药物,显著降低脱靶毒 性。(5)肽片段生产工艺简单,易于规模化。因此,PDC在开发靶向给药体系方面具有很大潜力。
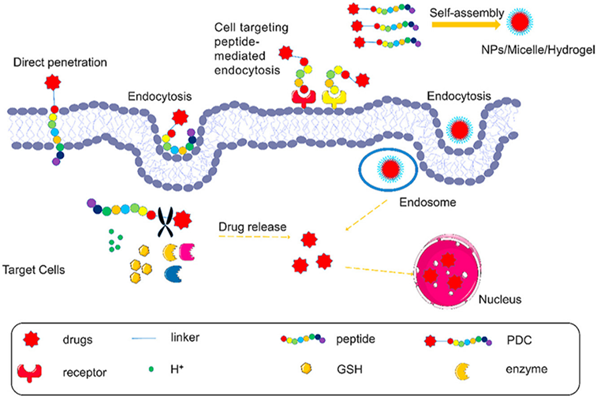
这篇文章主要介绍多肽的种类和机制,连接子的分类及裂解机制,以及用于构建PDCs的不同药物,并对PDC的临床发展现状进行总结。此外对PDC在临床应用中可能存在的障碍和挑战进行预测和展望。
多肽的种类和机制
多肽是PDC的重要组成部分,多肽可以根据其功能分为细胞穿透肽(CPPs)、细胞靶向肽(CPTs)、自组装肽(SAPs)和反应肽。细胞穿透肽(CPPs)是指小的,短的分子肽,可以进入细胞而不破坏其膜的完整性,通常由5-30个氨基酸组成。CPPs含有丰富的碱性氨基酸,如精氨酸和赖氨酸,其在生理环境下带正电荷。近年来,CPPs已广泛应用于给药系统,CPP穿透细胞膜的机制可分为两类:内吞作用和直接易位。
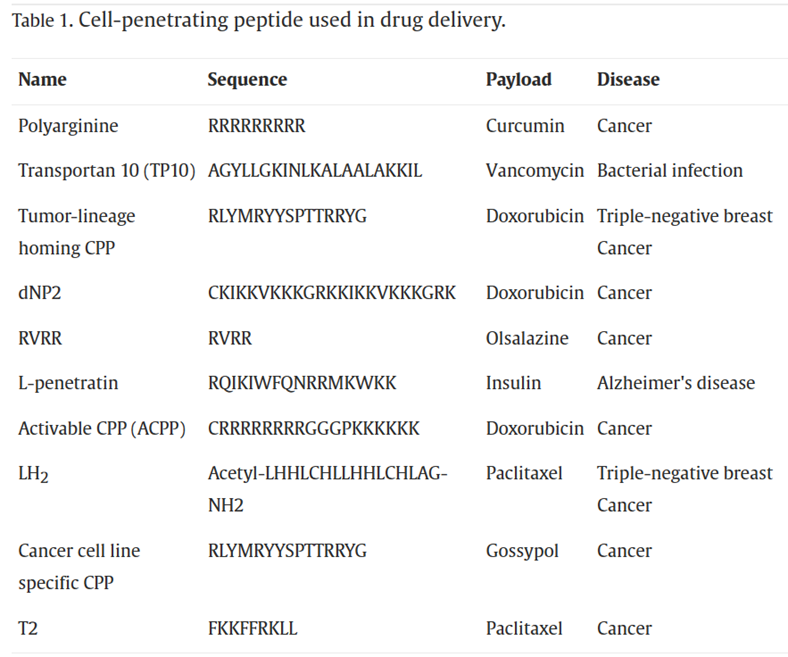
表1:应用于给药系统中的CPPs
细胞靶向肽(CPTs)被定义为与细胞或组织特异性结合的多肽。一般有两类靶向给药体系:被动靶向和主动靶向。被动靶向是指药物由于给药系统本身的性质(大小、形状、电荷等)或靶组织的特点(血管发育不良、淋巴组织回流不足等),随血液循环在病灶组织中被动积累。主动靶向是通过识别靶组织中特异性表达的受体或蛋白质,并通过受体-配体相互作用将药物主动递送到病灶组织来实现的。大多CPTs是通过主动靶向来实现递药机制的。
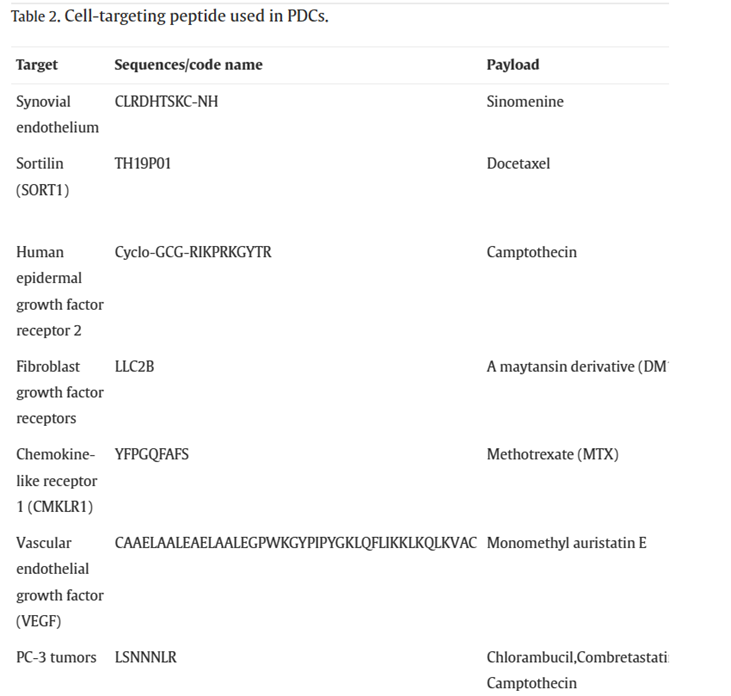

表2:应用于给药系统中的CPTs
自组装肽(SAPs)是指在没有外部刺激的情况下,通过非共价相互作用(包括范德华力、静电相互作用、氢键和堆叠相互作用),从复杂混合物中选择性地自发形成一个或多个有序结构的肽。氨基酸作为多肽的基本组成单元,其类型和排列方式是自组装多肽组装能力的基础。此外,设计自组装多肽的重点是利用多种分子间相互作用,包括氢键、静电相互作用、π-π叠加、范德华力、金属配体络合物和熵。具有自组装能力的多肽倾向于两亲性、芳香性、电荷分散性和不同的对称电荷交替排列。与普通多肽相比,SAPs的主要优点是生物相容性、生物降解性和多功能性。
反应肽是指对外界刺激作出反应而发生结构变化的肽。这种变化发生在结构水平,与自组装肽的自组装行为不同,反应性肽需要外部环境刺激才能发生结构变化。通常,外部环境刺激包括温度、pH值、酶等。一般来说,当组织或器官发生病变时,所涉及的生理环境也会发生变化。以肿瘤为例,由于肿瘤细胞过度增殖,血管结构发育不完全,肿瘤组织通常处于缺氧环境,导致其代谢过程发生变化。相对于正常组织的有氧代谢,肿瘤组织的代谢更依赖于糖酵解,其代谢产物乳酸和呼吸作用产生的CO2共同引起肿瘤微环境的酸化。肿瘤微环境的弱酸性性质也成为靶向肿瘤的一种新方法。近年来,基于反应肽的PDCs的构建引起了许多研究者的兴趣。
连接子的分类
连接子作为药物与多肽之间的连接桥梁,决定了PDCs在体内的循环时间和稳定性。理想的连接子应在循环中保持稳定,避免药物过早释放,同时能够在药物到达病灶组织后迅速有效地释放药物,同时该连接子不应影响多肽对其受体的亲和力和药物活性。
连接子的疏水性不能太强,以防止PDCs因疏水性而聚集,导致体内稳定性差,药效降低,同时具有较强的全身毒 性和免疫副作用。根据连接子的释药机制,连接子主要分为不可裂解连接子和可裂解连接子,可裂解连接子可分为pH敏感型连接子、氧化还原敏感型连接子和酶敏感型连接子。
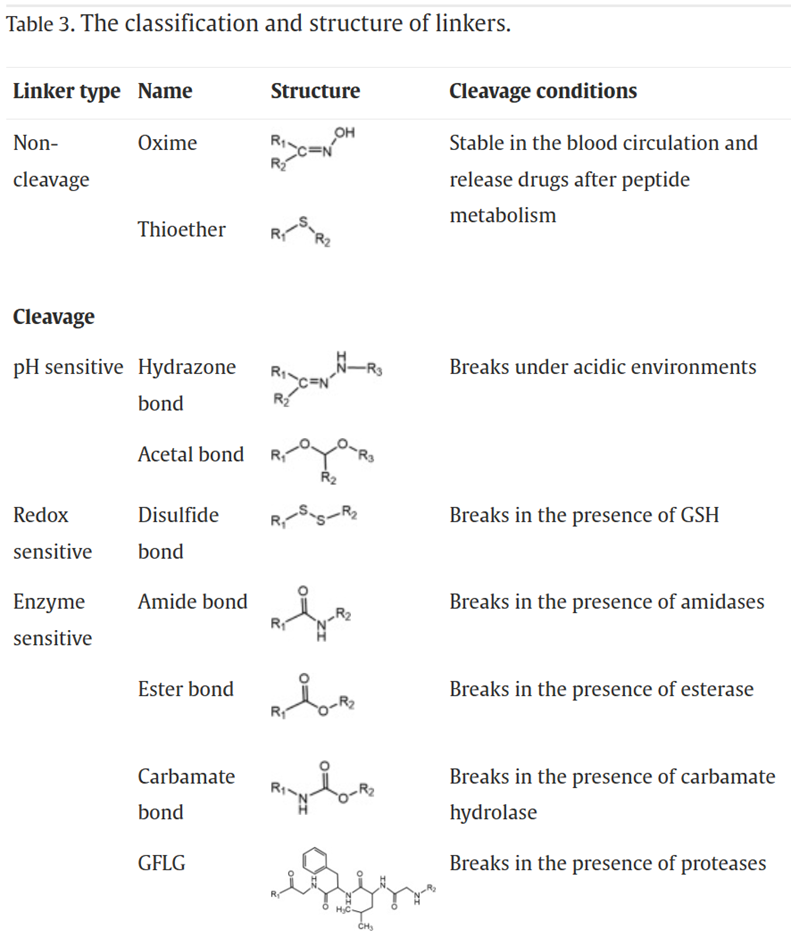
表3:连接子的结构和分类
构建PDCs的药物
PDCs的有效载荷是具有细胞毒 性或治疗作用的药物,这些药物大多存在水溶性低、选择性差、半衰期短、稳定性差等缺点,限制其临床应用。使用PDCs策略递送的药物需要有可行的附着位点,并在结合时无药理活性,当在病灶组织释放后发挥治疗作用,作用机制明确,药理活性强。与多肽偶联后,可提高药物的溶解度,促进药物的选择性,延长在体内循环时间,优化生物利用度,防止药物对其他组织的副作用和毒 性。用于PDC构建的药物可分为化学药物、蛋白质药物和多肽药物。化学药物包括阿霉素、紫杉醇、喜树碱、甲氨蝶呤、顺铂等,蛋白质类药物包括干扰素、肿瘤坏死因子,其可以通过诱导细胞凋亡和抑制细胞内蛋白质合成来达到有效的抗肿瘤治疗效果。然而,蛋白质类药物存在体内稳定性差、缺乏靶向性、生物利用度低等缺点。因此,由多肽与蛋白质药物结合而成的PDC成为解决这一问题的新思路。肽类药物是近年来新药研发的热点。
多肽药物与传统的化学药物和蛋白质药物相比,具有明显的优势:(1)多肽药物一般具有较高的活性;(2)与蛋白质类药物相比,多肽类药物分子量较小,易于人工合成,便于结构修饰;(3)多肽药物的合成效率高,随着近年来技术的进步,多肽固相合成简单,自动化程度高,易于控制;(4)副作用少。大多数肽类药物与人体序列同源性高,分子量小,无免疫原性,不会引起免疫反应。然而多肽药物的缺点也很明显。与化学药物和蛋白质药物不同,多肽药物理化性质不稳定,易氧化水解,容易结块。此外,肽类药物的半衰期较短,且清除率较快,不易渗透细胞膜。
治疗不同疾病的PDCs
PDC类药物可应用于炎症的治疗,例如萘普生Naproxen是一种非甾体抗炎药,可以通过抑制前列腺素合成来发挥抗炎作用。然而由于缺乏选择性,存在胃肠道不良反应。为了提高萘普生的选择性,Moreira等人构建了萘普生-脱氢二肽复合物,并发现它们很容易形成纳米结构的纤维超分子水凝胶,这可能是治疗炎症的极 佳策略。
此外,PDC药物广泛用于细菌感染性疾病。有效和安全的治疗细菌感染是现代医学面临的重大挑战。这在很大程度上是由于目前的抗菌药物在宿主毒 性、有效给药和增加抗菌耐药性方面的局限性。为了解决这些问题,Brankiewicz等将氟康唑fluconazole与细胞穿透肽CPT共价连接形成PDC,与游离氟康唑相比,PDC表现出更高的念珠菌杀灭效果。
此外,PDCs还可应用于治疗药物(如镇痛、疟疾和糖尿病)的递送系统,。只要药物满足PDC构建的要求,相信未来通过这种前药策略可以实现更多疾病的治疗。
PDCs药物的临床应用前景
虽然PDC具有很大的应用前景,但目前PDC领域仍处于发展低谷。到目前为止,全球只有两种PDC药物获批上市:一种是由诺华子公司开发的Lutathera,于2018年1月获FDA批准上市,用于治疗生长抑素抑制剂受体阳性的胃肠胰 腺神经内分泌肿瘤。另一种是Oncopeptipes开发的Pepaxto (Melflufen),于2020年2月被FDA批准加速上市,用于治疗多发性骨髓瘤。
除了批准上市的两种药物外,表4列出了目前正在进行临床试验的PDC药物。ANG1005是AngioChem开发的PDC药物,已进入III期临床试验。
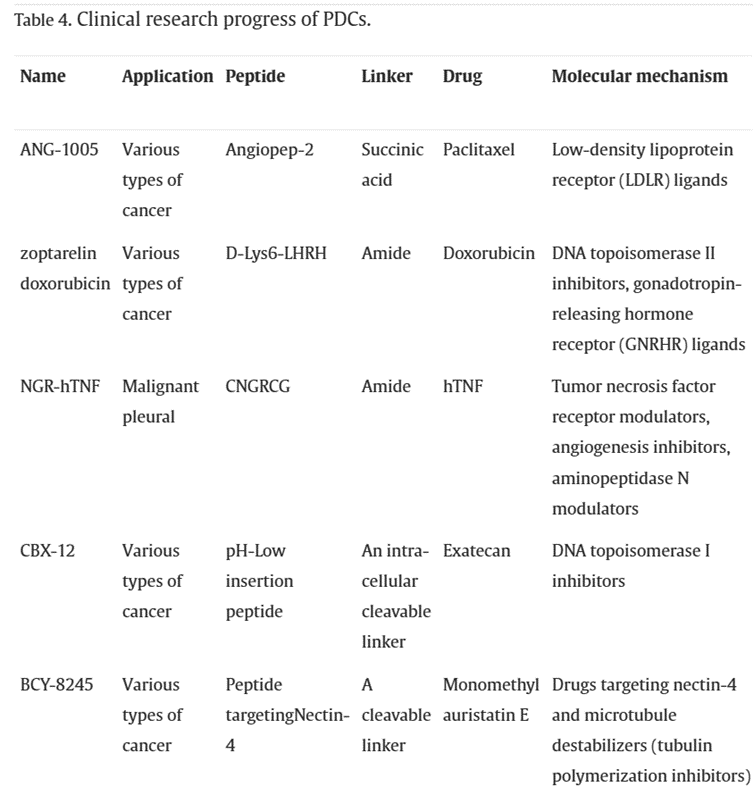
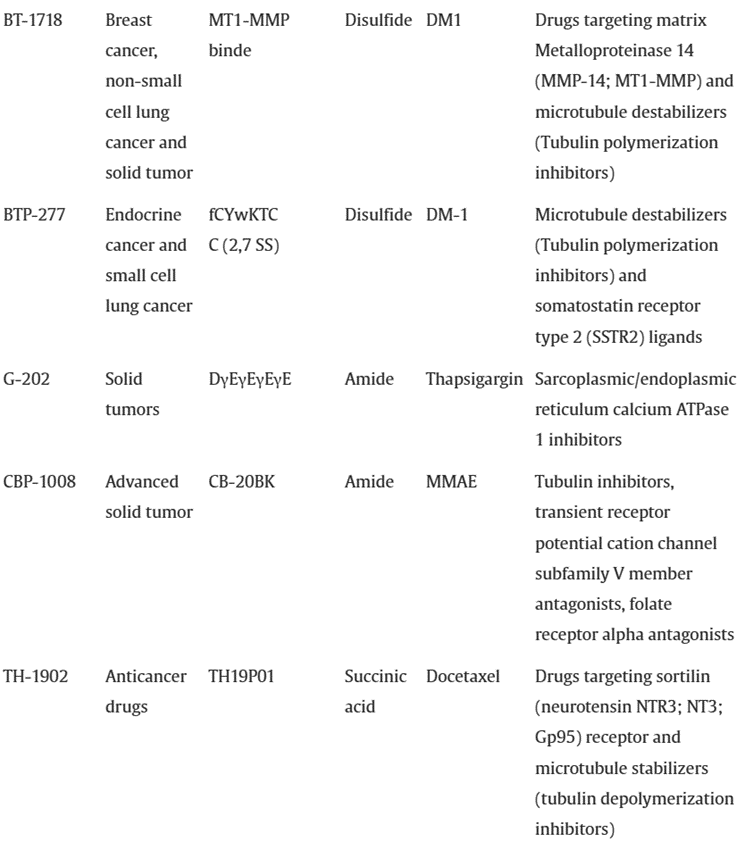

表4:正在进行临床试验的PDC药物
总结与展望
PDC药物首先通过多肽靶向递送到特定位点(主动或被动靶向),然后通过细胞穿透肽的膜穿透或受体介导的跨膜作用将PDC有效递送到细胞中,最后在环境刺激或酶作用下通过特定的链断裂接释放有效载荷,发挥药物作用。
从市场上PDC药物的数量来看,尽管PDC具有许多独特的优势,但在临床转化的道路上仍然存在许多挑战和障碍。首先从安全性考虑,从天然氨基酸中提取的多肽以水溶性的形式存在是完全可生物降解的,通常是生物相容性的,没有不良反应。然而目前尚不清楚多肽与药物偶联后,其生物相容性和生物降解性能否被保留。
其次从稳定性考虑,多肽具有较短的生物半衰期,导致PDCs在体内的分布和循环时间受到限制,药物在多肽降解之前进入病灶组织细胞的时间有限。虽然有许多方法可以延长多肽的生物半衰期,但PDC药物体积小,易于被肾 脏清除。因此建议将PDC的前药策略与载体材料应用相结合,形成尺寸合适、稳定性较高的给药体系。
第三从有效性考虑,PDCs中的连接子需要特定的环境(温度、pH、氧化还原、酶等)才能断开并释放药物,有时药物不能作为原型药物释放,甚至不能释放。此外,也没有办法确定药物在靶细胞中的释放速率和效率。因此,需要用合适的方法来证明PDC药物的疗效。
最后从给药方式来看,由于胃肠道蛋白酶的存在,与蛋白质类药物类似,PDC药物目前不能口服,只能采用侵入性注射给药,限制了其临床应用。为了解决这一局限性,建议设计口服大分子药物的给药系统,并采用适当的载体或结构修饰,以防止胃肠道系统中酶的降解,并保证PDC吸收到血液中。
高效PDCs的开发需要多功能多肽的设计和合成,我们相信随着多肽筛选技术和合成技术的进步和成熟,未来将会探索出更多的多功能肽,基于PDCs的智能纳米药物给药策略也将在未来广泛应用于临床。
参考文献
1、Liming Gong, Heming Zhao, Yanhong Liu, Hao Wu, Chao Liu, Shuangyan Chang, Liqing Chen, Mingji Jin, Qiming Wang, Zhonggao Gao, Wei Huang, Research advances in peptide?drug conjugates, Acta Pharmaceutica Sinica B,2023, 2211-3835,
https://doi.org/10.1016/j.apsb.2023.02.013.
2、U Hennrich, K Kopka, Lutathera?: the First FDA- and EMA-approved radiopharmaceutical for peptide receptor radionuclide therapy, Pharmaceuticals, 12 (2019)
doi:10.3390/ph12030114
3、MV Mateos, J Blade, S Bringhen, EM Ocio, Y Efebera, L Pour, et al. Melflufen: a peptide?drug conjugate for the treatment of multiple myeloma, J Clin Med, 9 (2020).
doi:10.3390/jcm9103120
4、P Kumthekar, SC Tang, AJ Brenner, S Kesari, DE Piccioni, C Anders, et al. ANG1005, a brain-penetrating peptide?drug conjugate, shows activity in patients with breast cancer with leptomeningeal carcinomatosis and recurrent brain metastases, Clin Cancer Res, 26 (2020)
https://doi.org/10.1158/1078-0432.CCR-19-3258



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57