2023年3月22日,Incyte宣布其PD-1抗体Zynyz(Retifanlimab)获得FDA批准上市,用于治疗转移性或复发性局部晚期默克尔细胞癌(MCC)成人患者。这也是FDA批准的第5款PD-1单抗。

Retifanlimab此次的获批基于一项开放标签、单臂的II期临床研究(POD1UM-201)数据。PODIUM-201(NCT03599713)研究是一项开放性、多地区、单臂的临床试验,评估人群为65名既往在晚期阶段未经系统治疗的转移性或复发性局部晚期的MCC患者。
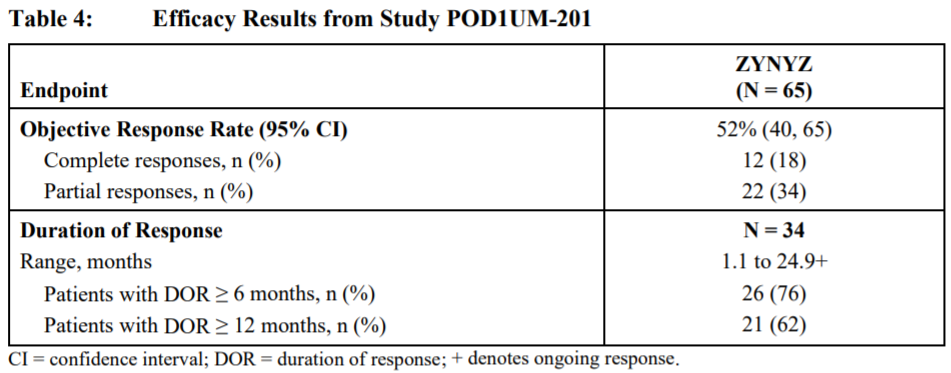
结果显示,在此前未接受过化疗的患者(n=65)中,Retifanlimab单药治疗的客观缓解率(ORR)为52%(95% CI: 40-65)。其中12名患者(18%)获得完全缓解,22名患者(34%)获得部分缓解。在获得缓解的患者中,缓解持续时间(DOR)在1.1个月到24.9个月之间。76%(26/34)患者DOR超过6个月,62%(21/34)患者DOR超过12个月。
Merkel细胞癌(Merkel Cell Carcinoma,MCC),又称为皮肤神经内分泌癌,该肿瘤发病率低,其最早由Toker于1972年首次报道,是目前已知的恶性程度最高的原发性皮肤肿瘤,预后极差,其死亡率是皮肤黑色素瘤的两倍,而且极易出现复发(约50%)和发生转移(约30%)。MCC目前缺少有效的治疗药物,传统的化疗作用有限,一直以来对医生来说都是非常棘手的疾病。进入免疫治疗时代,Retifanlimab的获批上市为更多MCC患者带来了治疗的曙光。
Retifanlimab并不是第一个获批MCC适应症的PD-1/PD-L1抑制剂, 早在2017年,FDA就加速批准Avelumab(PD-L1抑制剂)用于12岁及以上儿科和成人转移性默克尔细胞癌(MCC)治疗。这一获批基于iKnowMed数据库(一种肿瘤特异性电子健康档案系统),采集既往化疗的转移性默克尔细胞癌患者的历史数据作为对照。这是基于患者电子健康记录(EHRs)作为真实世界证据获得FDA 批准的经典案例。
BLA遭拒、再鼎“退货”
Retifanlimab的曲折命运
Retifanlimab最初由Macrogenics研发,是一种人源化的IgG4亚型的PD-1抗体。Incyte公司在2017年与MacroGenics公司签订独家全球合作和许可协议,获得Retifanlimab的全球权利。MacroGenics保留利用Retifanlimab开发产品管线的权利。2019年7月,再鼎医药以1750万美元预付款+6000万美元里程碑金额从Incyte引进Retifanlimab的大中华区权益。
Incyte对Retifanlimab适应症的布局选择避开竞争激烈的大适应症转而瞄准更为小众的适应症。但是Retifanlimab小众适应症的开局之路并不顺利。早在2021年1月,FDA就对Retifanlimab用于接受过铂类化疗或不耐受的局部晚期或转移性肛管鳞状细胞癌(SCAC)成人患者的生物制品许可申请(BLA)授予优先审评资格。令人遗憾的是,因为II期临床入组人群较少和总响应率不高的原因,当年7月FDA最终拒绝了这一申请。此消息一出,Incyte股价曾一度下跌30%,再鼎医药股价也曾一度下跌12%。
今年3月,再鼎医药在2022年财报中披露,基于竞争格局的变化,再鼎医药已经终止了与Incyte公司在大中华区开发和商业化retifanlimab的合作,自2023年1月11日起生效。再鼎医药将继续支持正在进行的临床研究的过渡工作,如用于治疗NSCLC的全球III期研究和用于治疗子宫内膜癌的全球Ι期研究的中国部分。
如果说之前被FDA拒绝批准令Retifanlimab在中国的商业化蒙上了阴影,那“基于竞争格局的变化” 则更加坚定了再鼎“退货”的决心。目前Retifanlimab在中国启动了3项临床试验,主要针对微卫星不稳定高(MSI-H)的子宫内膜癌和IV期鳞癌和非鳞癌非小细胞肺癌等热门领域。众所周知,非小细胞肺癌免疫治疗在晚期领域的竞争已经“卷”得不行,国内已经有8款PD-1单抗和3款PD-L1单抗获批晚期NSCLC适应症,整个市场已是一片红海。此外,虽然国内还没有一款针对MSI-H子宫内膜癌的PD-1/PD-L1获批,但已经有3款PD-1和1款PD-L1获批了MSI-H实体瘤适应症,覆盖人群范围更广。总体而言,后来者如果没有差异化优势,将很难搅动市场风云。或许正是基于这个原因,再鼎最终选择“退货”,及时止损。
Retifanlimab
未来路在何方?
MCC适应症的顺利获批让Retifanlimab一扫之前的阴霾,未来之路也似乎慢慢变得清晰了起来。
聚焦小众癌种避开红海市场依然是个不错的选择。Retifanlimab用于治疗肛管鳞状细胞癌(SCAC)的BLA虽被拒绝,但FDA并没有对其处以死刑,而是要求Incyte公司继续完成Ш期临床研究,在确证Retifanlimab有效性后再递交上市申请。SCAC患者实际上目前正处于无药可用的状态,而通过Retifanlimab的治疗,有1例达到完全缓解,12例部分缓解,这说明这个药物针对某些人群的确是有效的。另外还有33例患者为SD,这种带瘤生存状态,对患者也是非常有利。所以如果在II期临床研究的基础上,进一步细化受试者的入选和排除标准,将最能体现药物疗效的受试者入选到临床研究中,开展进一步的III期确证性临床研究,是有可能得到有利的结果的。
另外,如果在后续NSCLC和子宫内膜癌的临床试验中Retifanlimab能拿出优于已获批同类药物的疗效或安全性数据,亦或是在前线治疗或早期赛道有所突破,那将大大增加其未来竞争的砝码。
联合疗法方面,Retifanlimab也大有可为,未来可期。纵观Incyte的研发管线,其对PD-1/CD137双抗、TIM3、LAG 、CD73靶点均有布局,而这些靶点目前也是与PD-1药物联用的大热门。另外,由于MacroGenics保留了利用Retifanlimab开发产品管线的权利,其旗下多款产品未来都有可能与Retifanlimab一起探索联用方案。其实探索已在进行中,Margetuximab是MacroGenics公司研发的对抗体Fc端进行优化的HER2单克隆抗体,其Ib/II期MAHOGANY研究队列A公布结果显示:Margetuximab和Retifanlimab的联合在HER-2免疫组化3+且PD-L1表达阳性患者中ORR可达到53%,DCR达到73%,中位PFS时间为6.4个月。提示在胃癌抗HER-2治疗与免疫治疗之间的协同效应,并且通过两者的联合有望在一部分患者中达到“去化疗”的效果。
结 语
目前国内PD-1/PD-L1单抗已经严重扎堆,FDA却反对内卷,目前只批准了5款PD-1单抗和3款PD-L1单抗上市,适应症覆盖肺癌、肝癌、尿路上皮癌、胃癌、子宫内膜癌等,但仍存在大量未被满足的临床需求。对Retifanlimab而言,唯有聚焦未被满足的临床需求,不断拓宽自己的治疗领域和治疗边界,方能从强手林立的PD-1/PD-L1抑制剂赛道突围成功。
参考来源
1. Catenacci DVT, Kang YK, Park H, et al. Margetuximab plus pembrolizumab in patients with previously treated, HER2-positive gastro-oesophageal adenocarcinoma (CP-MGAH22-05): a single-arm, phase 1b-2 trial. Lancet Oncol 2020; 21 (8): 1066-1076.
2. Catenacci DVT, Kang YK, Yoon HH et al. Margetuximab with retifanlimab as first-line therapy in HER2+/PD-L1+ unresectable or metastatic gastroesophageal adenocarcinoma: MAHOGANY cohort A. ESMO Open 2022; 7 (5): 100563.
3. 《新药布局接连受挫,中国明星药企们的老朋友 Incyte 将如何应对危与机?》,insight数据库
4. 再鼎医药官网
5. Incyte官网



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57