海思科医药集团股份有限公司(以下简称“公司”)于近日收到国家药品监督管理局下发的《受理通知书》,基本情况如下:
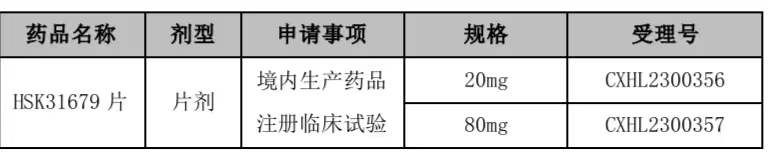
根据《中华人民共和国行政许可法》第三十二条的规定,经审查,决定予以受理。
一、研发项目简介
HSK31679 片是公司自主研发的一种高选择性甲状腺激素β受体(THR-β)激动剂,通过与甲状腺激素β受体结合,影响脂代谢过程中的关键步骤,起到降血脂和肝 脏脂肪的作用。临床拟用于治疗非酒精性脂肪性肝炎。按我国新化学药品注册分类规定,其药品注册分类为化药 1 类。
该品种“治疗成人原发性高胆固醇血症”适应症于 2021 年 11 月获 得国 家 药 品监 督 管 理局 下 发 的《 受 理 通知 书 》 , 受理 号为CXHL2101641/ CXHL2101640,于 2022 年 1 月获许进入临床,此次获得受理的适应症为“治疗非酒精性脂肪性肝炎”。
根据弗若斯特沙利文报告,全球非酒精性脂肪性肝炎(NASH)患病人数呈上升趋势,从 2016 年的 3.1 亿人上升到 2020 年的 3.5 亿人,复合年增长率为 3.1%;预计 2025 年将达到 4.1 亿人,2030 年达到4.8 亿人。我国 NASH 患病人数也呈上升趋势,从 2016 年的 3450 万人上升到 2020 年的 3870 万人,复合年增长率为 2.9%,预计将在 2025年达到 4600 万人。NASH 发病率高,且呈上升趋势,但目前 FDA、EMA以及 NMPA 均未批准任何一款针对 NASH 的药物上市,NASH 仍存在巨大的治疗空白。
二、临床试验开展情况
HSK31679 片“治疗成人原发性高胆固醇血症”适应症已在中国完成了Ⅰ期临床试验,目前正在进行该适应症的Ⅱ期临床试验。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57