看点
• 4月药审中心受理总量为1412个
• 4月化药共2个1类新药,5个改良型新药报产
• 4月新增93个按仿制药质量和疗效一致性评价申报的受理号
• 4款国产化药2类改良型新药获批新适应症
据药智数据企业版——药品注册与受理数据库最新统计,2023年4月份CDE共承办新的药品注册申请以受理号计有1412个,其中化药受理1004个,中药受理215个,生物制品受188个;2023年1-4月各类药品注册申请受理情况详见图1。
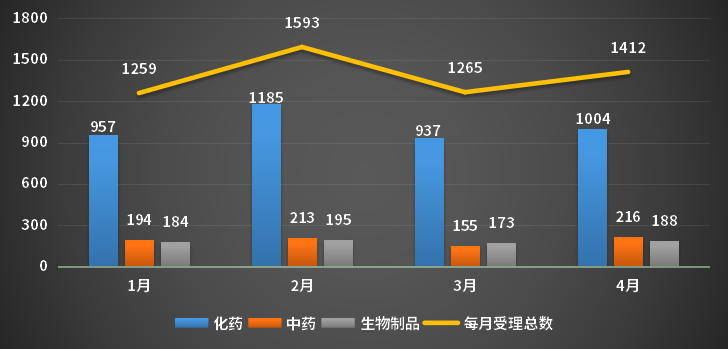
图1 2023年1-4月CDE药品受理情况
2023年4月份(注:状态开始时间(药智)从2023年4月1日至2023年4月30日)完成审评的受理号共1011个,其中化药受理690个,中药受理154个,生物制品受理165个;2023年1-4月各类药品完成审评情况详见图2。
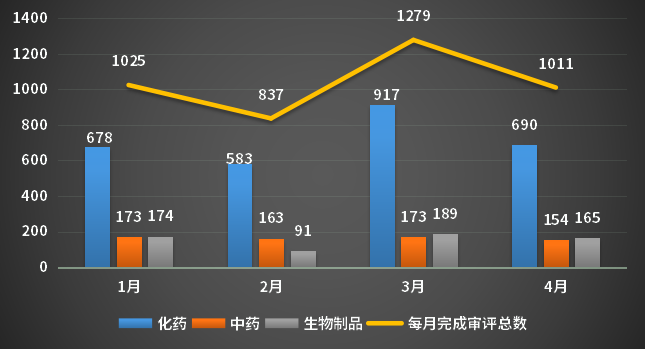
图2 2023年1-4月CDE药品完成审评情况
以下且看化药、中药、生物制品的注册受理及审评情况详细分析。
一、化药申报与审评情况
(一)化药受理情况
4月份CDE承办新的化药注册申请1004个(以受理号计),其中新药申请受理号115个,进口受理号49个,仿制申请受理号284个,补充申请498个,进口再注册36个;
以审评任务类别统计(以受理号计),IND申请131个,ANDA申请270个,NDA申请19个;2023年1-4月CDE化药各审评任务类别申请受理情况详见图3。
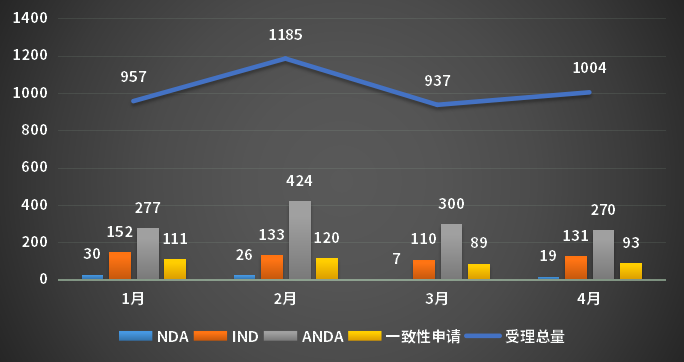
图3 2023年1-4月CDE化药各审评任务类别申请受理情况
1.化药1类国产申报情况
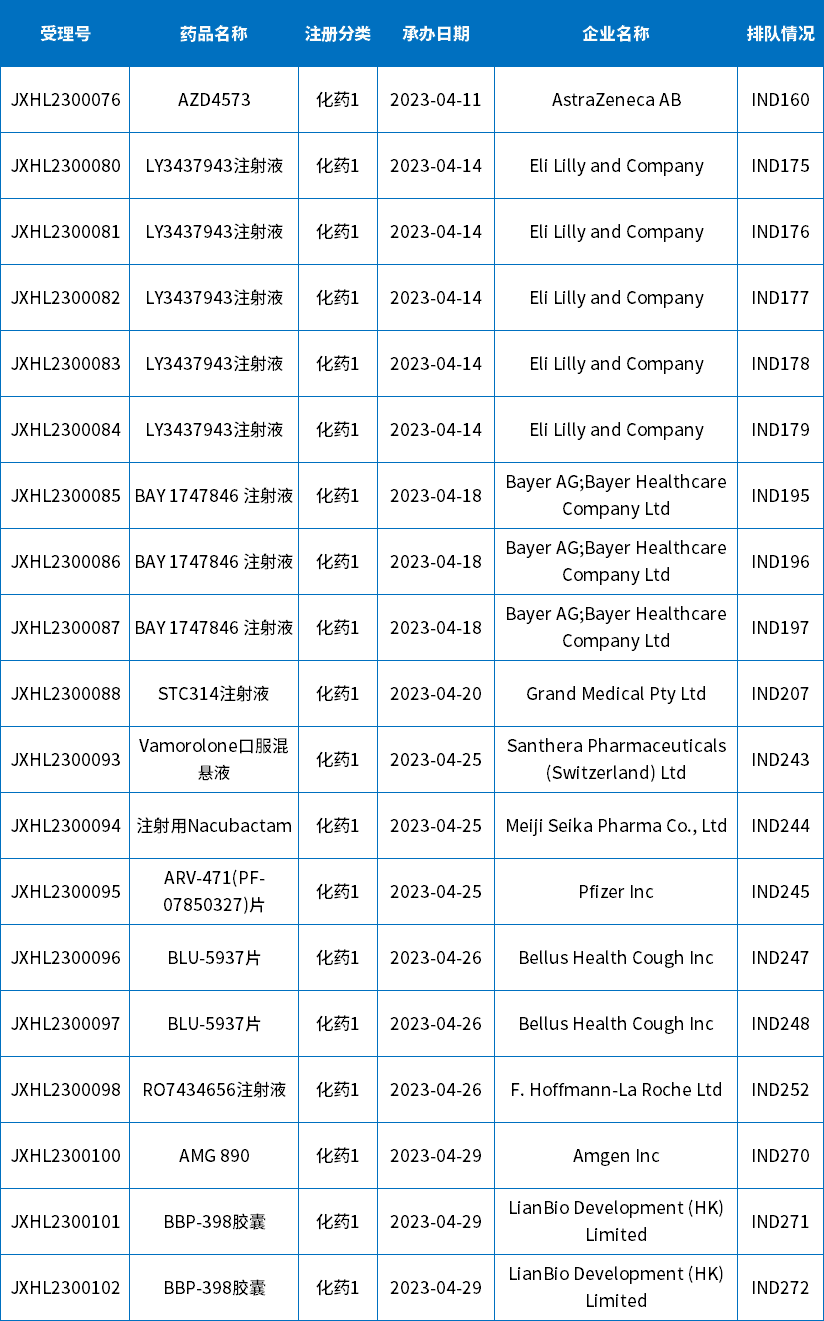
4月CDE受理化药国产1类新药共计93个(按受理号计),其中IND申请90个,涉及45个品种(按药品+企业维度统计),NDA申请3个,涉及2个品种(按药品+企业维度统计),目前均已进入相应序列排队待审;下表为4月新承办的1类国产新药。
表1 2023年4月新承办的化药1类国产新药
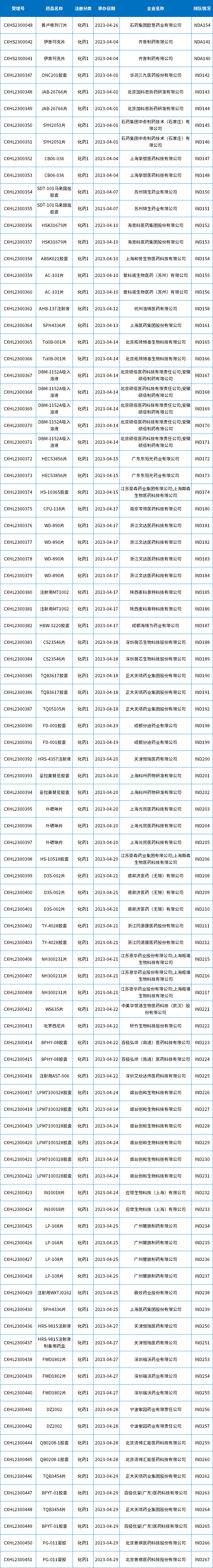
注:排队序号截止至2023年05月09日
2.化药1类进口药品申报情况
4月共19个进口化药1类受理号获得承办,其中全是IND申请,共11个品种,目前均已进入相应序列排队待审;下表为4月新承办的1类进口新药。
表2 2023年4月新承办的化药1类进口新药
注:排队序号截止至2023年05月09日
伊鲁阿克片
伊鲁阿克是齐鲁制药自主研发的1类新药,是一款高选择性的ALK和ROS1抑制剂,是一种经过多次结构优化的新型螺环结构化合物。临床前研究数据显示,伊鲁阿克对不同融合类型及耐药突变的ALK和ROS1阳性的肿瘤细胞均具有显著的增殖抑制作用。目前,国家药品监督管理局已受理其上市申请,当前已进入CDE新报序列排队待审评。
普卢格列汀片
普卢格列汀片是石药集团附属公司石药集团中奇制药技术(石家庄)有限公司开发的一种新型口服二肽基肽酶-4(DPP-4)抑制剂,被开发用于治疗2型糖尿病。
WS635片
WS635片是中美华世通拥有完全自主知识产权的1类新药,目前国家药品监督管理局已受理其临床试验申请。WS635是环孢菌素A(CsA)的3,4位双取代衍生物,是非免疫抑制性CsA类似物,当前开发的适应症为术后谵妄(Post-operative delirium,POD),是手术麻 醉后常见的中枢神经系统并发症。
CB06-036
CB06-036是上海挚盟医药自主研发用于治疗慢性乙型肝炎的小分子口服TLR8激动剂。临床前研究显示,CB06-036具有良好的选择性、活性及安全性,可以在人外周血单核细胞中诱导细胞因子,这些细胞因子能够通过多种免疫介质激活抗病毒功能。
3.化药改良型新药申报情况
4月新增化药2类改良型新药33个(按受理号计),其中IND申请22个,NDA申请11个,共涉及20个品种;2023年1-4月CDE化药改良型新药申请受理情况详见图4。
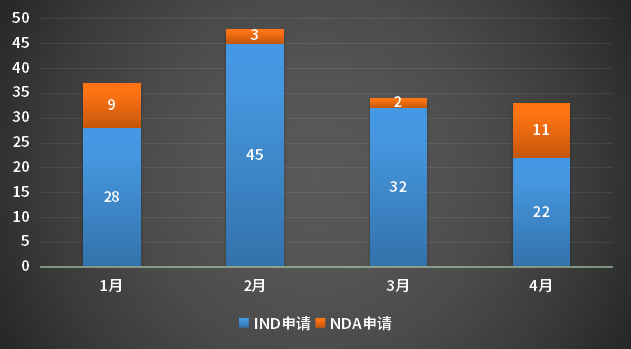
图4 2023年1-4月CDE化药改良型新药申请受理情况
其中,新承办的改良型新药上市申请共涉及5个品种;下表为5月新承办的2类改良型新药上市申请。
表3 2023年5月新承办的化药2类改良型新药上市申请
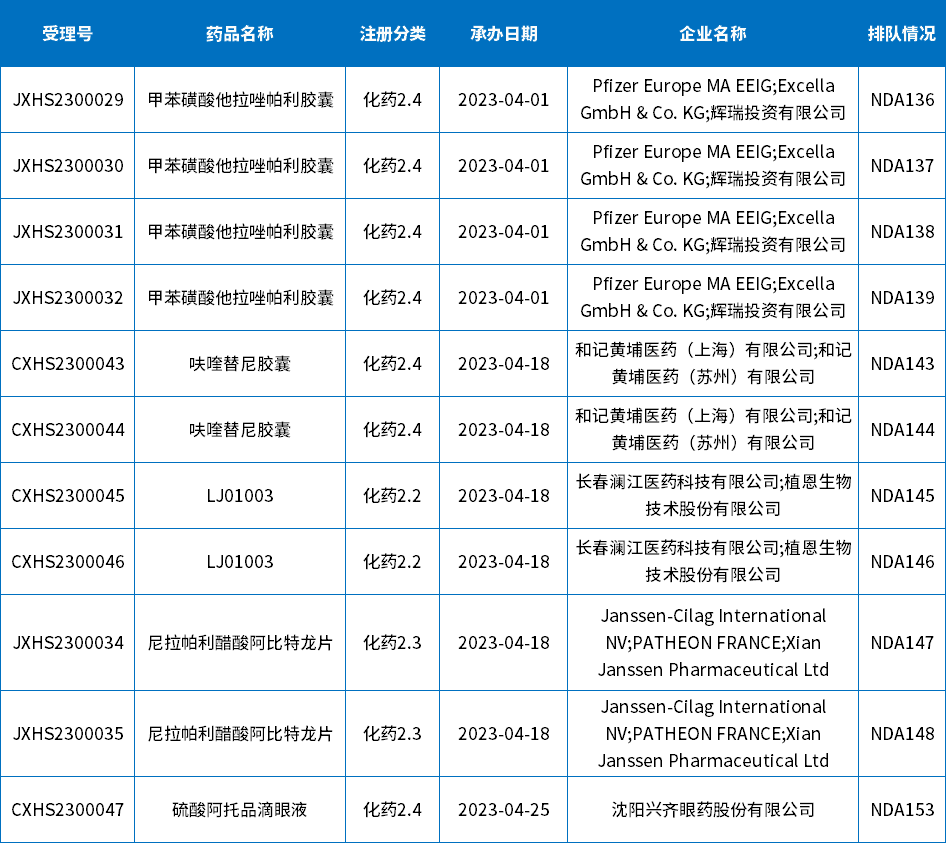
注:排队序号截止至2023年05月09日
(二)化药完成审评情况
4月,CDE完成审评的化药注册申请690个(以受理号计),其中新药申请受理号117个,进口受理号28个,仿制申请受理号151个,补充申请349个;以审评任务类别统计(以受理号计),IND申请122个,ANDA申请151个,NDA申请12个,进口再注册申请21个,一致性评价55个;2023年4月CDE化药各审评任务类别完成审评情况详见图5;
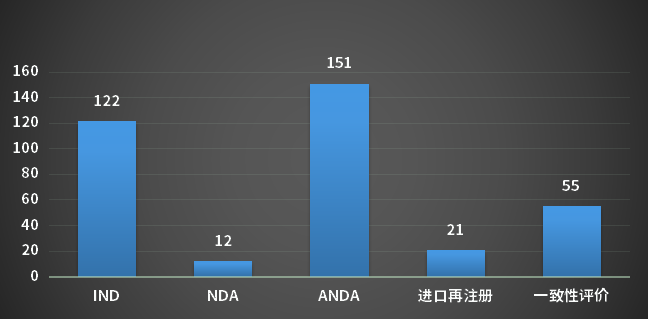
图5 2023年4月CDE化药各审评任务类别完成审评情况
以受理号审评结论来看,其中批准临床181个,批准生产136个,批准进口11个,未被批准33个;2023年4月CDE化药化药完成审评结论情况详见图6;
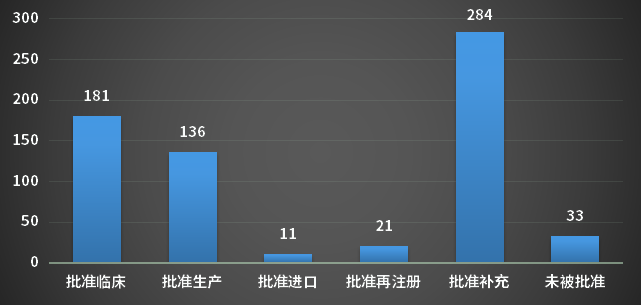
图6 2023年4月CDE化药化药完成审评结论情况
1.化药新药和进口原研获批情况
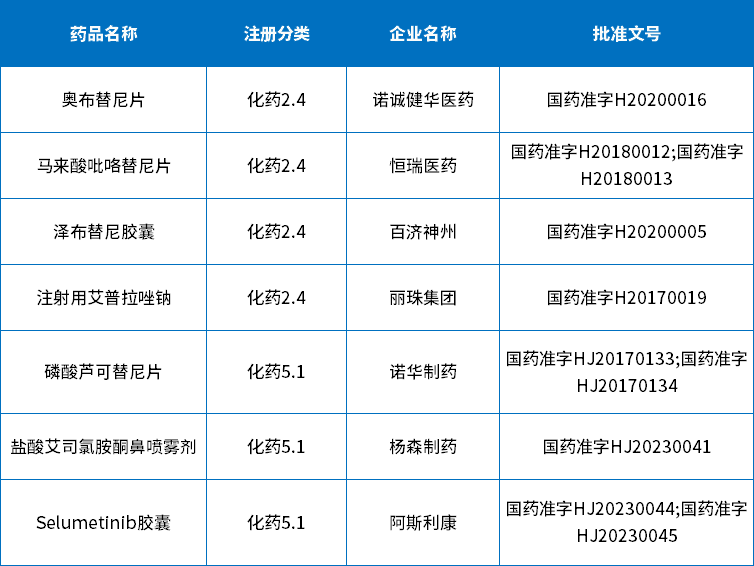
4月批准的新药和进口原研共7个,包括:1个1类新药、4个2类新药和3个进口原研批准上市;下表为4月化药获批新药和进口原研信息。
表4 2023年4月化药获批新药和进口原研信息
2.化药仿制药获批情况
4月共103个化药仿制药批准上市(按药品名+企业维度统计,排除了“氧”的数据统计),其中包括3类仿制药的35个,4类仿制药的63个,进口5.2类5个;ATC分类包括:心血管系统、神经系统等(仿制药获批具体信息请关注药智数据企业版——药品注册与受理数据库)。
二、中药申报与审评情况
(一)中药受理情况
4月,CDE承办的中药注册申请受理号共计216个,其中新药8个,补充申请208个;2023年1-4月CDE中药各申请类型受理情况详见图7。
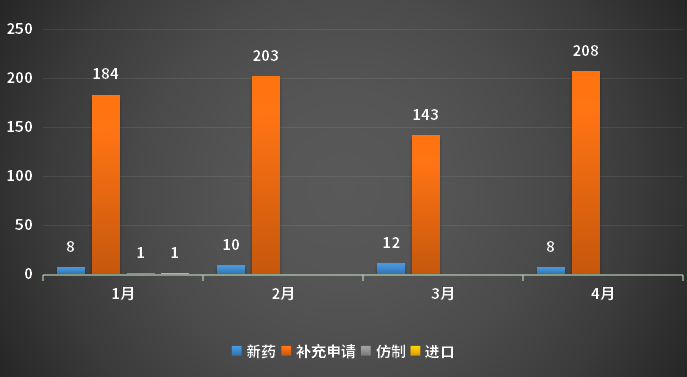
图7 2023年1-4月CDE中药各申请类型受理情况
1.中药新药申报情况
4月,共承办申请类型为新药的受理号共8个,其中,3个中药1类创新药,共涉及3个品种,均为IND申请;3个2类改良型新药申请,均为IND申请;2个3类经典名方制剂,均为为NDA申请;下表为4月新承办的中药新药。
表5 2023年4月新承办的中药新药
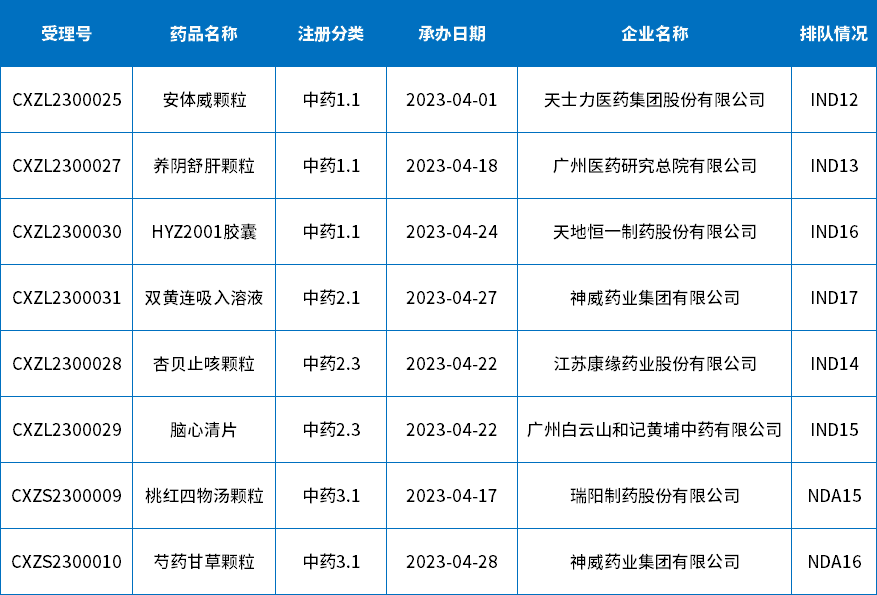
注:排队序号截止至2023年05月09日
(二)中药完成审评情况
4月,CDE完成审评的中药注册申请154个(以受理号计),其中新药受理号6个均为IND申请,补充申请144个,进口再注册4个;
在受理号审评结论方面,4月中药无新药获批上市,结论包括:批准补充137个,批准临床7个,未被批准6个。
三、生物制品审评情况
(一)生物制品受理情况
4月,CDE承办新的生物制品注册申请受理号共计188个,新药82个,补充申请72个,进口27个,进口再注册1个;2023年1-4月CDE生物制品各申请类型受理情况详见图8。
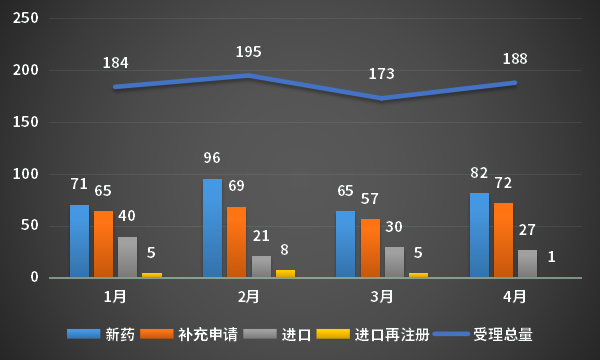
图8 2023年1-4月CDE生物制品各申请类型受理情况
1.生物制品1类新药申报情况
4月,共76个生物制品1类新药受理号获得承办,其中,临床试验申请71个,上市申请5个,目前均已进入相应序列排队待审;下表为4月新承办的生物制品1类创新药。
表6 2023年4月新承办的生物制品1类新药

注:排队序号截止至2023年05月09日
(二)生物制品完成审评情况
4月,CDE完成审评的生物制品注册申请165个(以受理号计),其中新药申请受理号81个,进口受理号12个,补充申请57个;以审评任务类别统计(以受理号计),临床试验申请91个,上市申请2个;2023年4月CDE生物制品各审评任务类别完成审评情况详见图9;
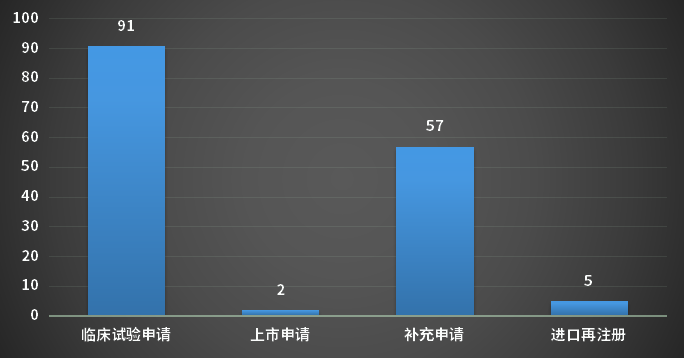
图9 2023年4月CDE生物制品各审评任务类别完成审评情况
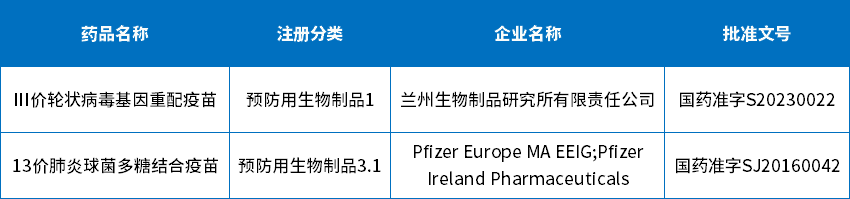
在受理号审评结论方面:批准临床112个,批准生产1个,批准进口1个,批准再注册5个,未被批准6个;4月份有1个预防用生物制品1类新药和1个3.1类预防用生物制品获批上市;下表为4月生物制品批准上市信息。
表7 2023年4月生物制品获批信息
四、按一致性评价申报品种情况
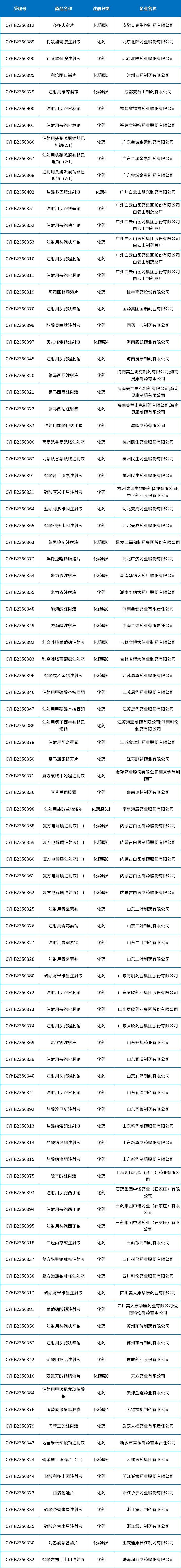
4月,新增94个按一致性评价要求进行申报的受理号和287个视同受理号。(篇幅限制仅展示一致性信息,视同及具体信息请关注药智数据企业版——药品注册与受理数据库);表8为4月新增一致性评价受理号信息。
表8 2023年4月新增一致性评价受理数据
数据来源:药智数据企业版——药品注册与受理数据库



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57