继新冠、甲流之后,近日全国多地医院儿科门诊出现呼吸道合胞病毒(RSV)感染增多的情况。不少家长在社交媒体上分享孩子感染RSV的过程,感叹RSV来势汹汹。
呼吸道合胞病毒(RSV)是一种常见的通过空气传播的RNA呼吸道病毒,通过口鼻吸入进入气管和肺部,侵入上皮细胞导致气道损伤,分泌呼吸道粘液阻塞管腔,引起呼吸困难。
RSV易感人群是儿童、老年人和免疫功能受损的成年人,超过90%的儿童在两岁之前都会感染RSV。RSV感染是全球5岁以下儿童因病毒感染而住院及死亡的首要因素。
据WHO统计,2020年全球约有3500万5岁以下儿童感染RSV,其中中国儿童患者有300万人。全球每年有多达15万人死于RSV感染。
3款RSV药品上市,
临床需求远未满足
目前,全球获批预防/治疗RSV的疫 苗药物不多,分别为阿斯利康/Sobi的Synagis(palivizumab)、阿斯利康/赛诺菲的Beyfortus(nirsevimab)和葛兰素史克(GSK)的Arexvy(RSVPreF3 OA/GSK3844766A)。
其中Synagis和Beyfortus由阿斯利康开发。2017年3月,阿斯利康与赛诺菲签署一项协议,共同开发和商业化Beyfortus。2018年11月,阿斯利康同意将Synagis在美权益连同130名相关职员打包让渡给Sobi,由Sobi全权负责商业化,同时授权Sobi共担Beyfortus在美损益。
• Synagis(阿斯利康/Sobi)
Synagis是一款抗RSV病毒F蛋白人源化IgG1κ单抗,1998年6月被批准用于支气管肺发育异常的婴幼儿、早产婴幼儿和血液动力学异常的先心病儿童,预防下呼吸道RSV感染。
不过,Synagis只能提供一个月的保护,需要注射5次才能覆盖一个典型的RSV流行季。
• Beyfortus(阿斯利康/赛诺菲)
Beyfortus是阿斯利康开发的一款长效单克隆抗体,通过结合表达于病毒粒子和受染细胞表面的RSV融合(F)蛋白达到中和RSV的目的,用于预防由RSV引起的下呼吸道疾病。
2022年11月,Beyfortus获欧盟委员会批准,作为单剂量被动免疫疗法,用于所有新生儿和婴儿,在其第一个RSV季节,预防RSV下呼吸道疾病(LRTI)。Beyfortus专为所有婴儿设计,只需给予单剂量肌肉注射,就能够从出生直至第一个RSV季节结束,全程提供持续的预防RSV疾病作用。近日,该药在国内的上市申请被CDE纳入优先审评。
• Arexvy(葛兰素史克)
Arexvy是由RSV融合前F糖蛋白(RSVPreF3,是RSV病毒进入人体细胞所需)与GSK专有的AS01佐剂组合而成,2023年5月被FDA批准用于预防60岁及以上人群因感染RSV引发的下呼吸道疾病(LRTD),成为全球首 款获批用于老年人的RSV疫 苗。
已公布的3期临床试验数据显示:接种Arexvy疫 苗将发生RSV相关LRTD(下呼吸道疾病)的风险降低了82.6%,并将发生严重RSV相关LRTD的风险降低了94.1%。
多款RSV产品在研进入3期临床,
爱司韦、PF-06928316即将出线
据灼识咨询研究数据,RSV药物全球整体市场规模(包括治疗药物及预防药物)预计将从2020年的18亿美元增长至2030年的128亿美元,年复合增长率达到21.4%。其中针对儿童的RSV药物预计将从2020年的18亿美元增至2030年的117亿美元,将占全球RSV药物市场的91.1%。
鉴于庞大的市场规模,越来越多的药企涉足RSV赛道。除了上述产品,目前全球有多款在研RSV产品(详见下表),在研RSV产品主要是预防性疫 苗。
全球在研RSV产品(部分)
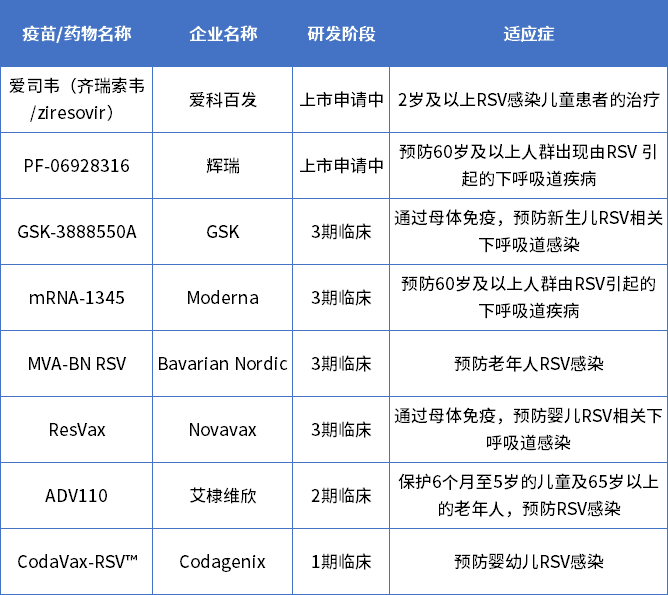
数据来源:药智数据
在研RSV产品中,爱司韦和PF-06928316进展较快,目前已递交上市申请。
GSK-3888550A、mRNA-1345、MVA-BN RSV和ResVax等已进入3期临床。其中GSK开发的GSK-3888550A是一款RSV母体疫 苗,与已获批的RSV老年疫 苗Arexvy一样含有重组亚单位融合前RSV抗原(RSVPreF3),该抗原可触发所需的免疫应答。2022年2月,评估单剂量GSK3888550A肌肉注射免疫18-49岁健康状况良好的孕妇,以预防新生儿RSV相关下呼吸道感染(LRTI)的有效性的3期双盲试验暂停患者入组和接种。
• 爱司韦(齐瑞索韦/ziresovir)
爱司韦是一款全新的RSV融合蛋白小分子抑制剂,是全球首 个成功完成3期注册临床试验的RSV抗病毒 药物,同时也是首 个在中国发现、开发,并拓展到全球的儿童创新药,也是首 个获国家药品监督管理局“突破性治疗品种”认定的非肿瘤创新药。
已完成的3期注册临床试验结果显示:爱司韦起效迅速,在治疗第3天,与安慰剂组相比,其临床症状评分改善提高了30%(p=0.002)。在RSV的重症高风险人群6个月以下的婴幼儿中,爱司韦表现出更显著的临床获益:与安慰剂组相比,其临床症状评分的改善提高了55%(p<0.001)。而且,在因RSV感染的重症监护室(ICU)患者中,爱司韦显示出显著缩短ICU治疗时间的临床获益:爱司韦组ICU平均治疗时间为3天,安慰剂组为8天(p=0.05)。同时爱司韦具有显著的抗病毒效果:爱司韦组在治疗第5天的患者的病毒载量与安慰剂组相比降低了77%(p=0.006);并且,在整个治疗期间,爱司韦组较安慰剂组的病毒载量显著降低,具有统计学差异。
治疗后6个月的随访数据显示,接受爱司韦治疗的6个月及以下婴幼儿再发喘息明显少于安慰剂组(9.0%vs.26.3%;p=0.02)。此外,AirFLO研究显示了爱司韦在婴幼儿患者中的良好安全性与耐受性。
2022年12月CDE受理其新药上市申请,并将该申请纳入优先审评程序,适应症为2岁及以上RSV感染儿童患者的治疗。
• PF-06928316(RSVpreF)
PF-06928316(RSVpreF)是辉瑞根据美国国立卫生研究院(NIH)所建立的RSV融合前F蛋白晶体结构所制造,由两种preF蛋白组成,可优化对RSV A和B株的保护。2022年12月,FDA受理PF-06928316的上市申请,用于预防60岁及以上人群出现由RSV引起的下呼吸道疾病(MA-LRTI),同时授予该申请优先审查。2023年2月,FDA再次授予PF-06928316优先审评资格,通过怀孕妇女产生主动免疫,进而预防自出生起至六个月大的婴儿出现RSV引起的MA-LRTI,PDUFA日期为2023年8月。
• mRNA-1345
mRNA-1345是一种针对RSV的疫 苗,编码一种融合前F糖蛋白,与融合后状态相比,融合前F糖蛋白可诱导更高的中和抗体反应。mRNA-1345使用了与Moderna COVID-19 mRNA疫 苗相同的脂质纳米粒(LNP),并含有优化的蛋白质和密码子序列。
mRNA-1345曾被FDA授予快速通道资格,用于预防60岁以上成人罹患RSV相关下呼吸道疾病。2023年1月,Moderna宣布mRNA-1345的3期临床试验达到主要终点,mRNA-1345预防60岁及以上RSV相关下呼吸道疾病的效力达到83.7%,且安全性良好。Moderna计划于今年上半年向监管机构提交许可申请。
• MVA-BN RSV
MVA-BN RSV是Bavarian Nordic开发的一款候选疫 苗,基于公司MVA-BN平台开发,用于预防老年人RSV感染,采用了五种不同的RSV抗原,以刺激身体对A、B RSV亚型的广泛免疫反应。此前的2期临床试验表明,该MVA-BN RSV在预防有症状的RSV感染方面显示出高达79%的疫 苗效力。
2022年3月,优锐医药与Bavarian Nordic公司超2亿美元的合作,获得MVA-BN RSV在中国、韩国和部分东南亚国家的开发及商业化授权。2022年11月,MVA-BN RSV疫 苗在国内的3期临床活CDE批准。
• ResVax
ResVax是一种以磷酸铝为佐剂的RSV融合(F)蛋白重组纳米颗粒疫 苗。2019年公布的ResVax针对母体免疫的3期临床试验结果却显示:ResVax在RSV相关LRTI的主要终点上只有39%有效,未能达到预防医学上的显著主要目的。
不过,ResVax疫 苗在次要终点上展示出两个亮点,一是显著降低了RSV相关住院人数,二是降低了严重的RSV低氧血症。
• ADV110
艾棣维欣开发的ADV110是一种针对RSV的蛋白亚单位疫 苗,由纯化的RSV G蛋白亚单位作为免疫原性成份与佐剂AE011组成,可诱导高水平的抗G蛋白特异性抗体,针对RSV感染的中和抗体,从而减少肺部病毒载量,目前已经进入2期临床试验。
已公布的1期临床试验结果表明,ADV110在低剂量、高剂量,以及单次接种和两次接种均具备良好的安全性及耐受性,并且绝大多数受试者表现出显著的抗体应答,低剂量组达到90%、高剂量组达到了100%。
• CodaVax-RSV®
CodaVax-RSV®是一款减毒活鼻内RSV候选疫 苗,采用基因编辑的方式,可防止野生型回归,加上鼻内给药途径,在动物模型中显示的临床前疗效,具有广泛的全身和粘膜免疫力,具有更可靠的安全性。
2022年11月,CodaVax-RSV®被FDA授予快速通道指定。
结 语
RSV感染被视为全球一大公共卫生危机,但目前已获批的疫 苗/药物却寥寥可数。
鉴于近年Beyfortus、Arexvy的获批,以及RSV产品的研究进展,RSV赛道似乎即将进入爆发期,爱司韦、PF-06928316有望于近两年获批上市。
期待未来有更多的RSV产品获批上市,成为人们抗击RSV的利器。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57