7月19日,CDE官网显示两款药品被纳入拟优先审评品种,分别为深圳微芯生物科技股份有限公司(以下简称“微芯生物”)的西达本胺片和广州必贝特医药股份有限公司(以下简称“必贝特医药”)的注射用BEBT-908(注射用双利司他)。
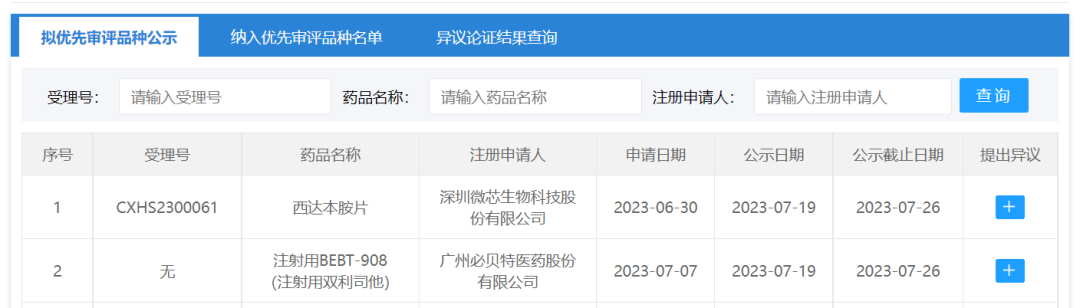
图片来源:CDE官网
1.西达本胺片
西达本胺由微芯生物开发,商品名为爱谱沙/ Epidaza。西达本胺是我国首 个获批上市的原创化学新药,也是全球首 个亚型选择性组蛋白去乙酰化酶(HDAC)口服抑制剂,主要针对第I类HDAC中的1、2、3亚型和第IIb类的10亚型,具有对肿瘤异常表观遗传功能的调控作用。
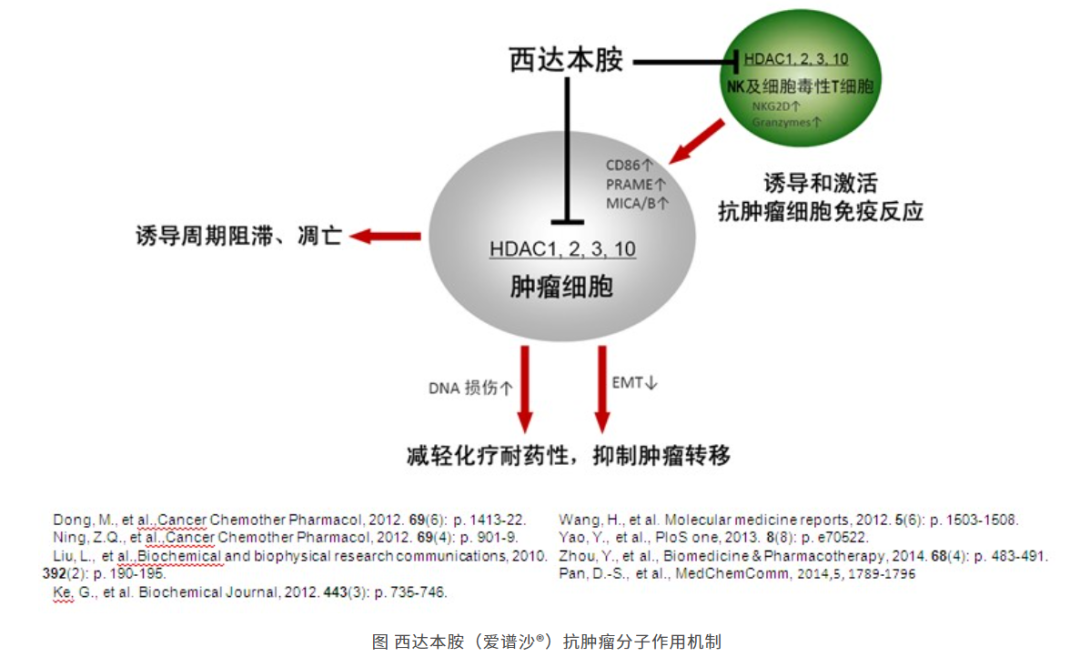
图片来源:微芯生物官网
自2014年12月获CFDA批准上市以来,西达本胺已在中国大陆、中国台湾、日本等多地获批,目前可用于外周T细胞淋巴瘤、乳腺癌、成人T细胞白血病等疾病的治疗。2017年7月,西达本胺片进入国家医保目录。
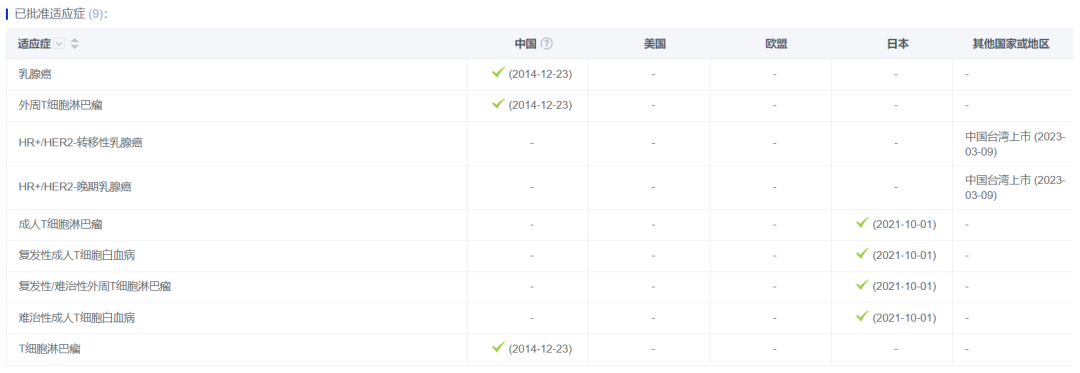
图片来源:药智数据企业版——全球药物分析系统数据库
作为微芯生物的核心产品,西达本胺片自上市以来为微芯生物贡献了近90%的营业收入,是其业绩主力。
据CDE官网显示,本次西达本胺片拟优先审评适应症为:联合R-CHOP(利妥昔单抗、环磷酰胺、阿霉素、长春新碱和强的松)用于既往未经治疗的MYC和BCL2表达阳性的弥漫大B细胞淋巴瘤(DLBCL)患者。本适应症是基于一项随机、双盲、安慰剂对照、多中心III期试验的完全缓解率(CRR)终结果及无事件生存期(EFS)期中分析结果所给予的附条件批准。

图片来源:CDE官网
随着适应症的拓展,西达本胺放量速度或将加快,有望带来更可观的销售量。
2.注射用BEBT-908
注射用BEBT-908由必贝特医药开发,是首 创全新化学结构HDAC/PI3K双靶点抗癌一类新药,具有比单靶点药物更强的破坏肿瘤细胞信使网络的能力,对多种血液肿瘤和实体瘤均有强抗肿瘤作用。
2021年,BEBT-908被纳入突破性治疗品种,用于治疗经过至少2种系统治疗后复发或难治性弥漫性大B细胞淋巴瘤(r/r DLBCL)。昨日(7月19日),BEBT-908作为“(四)纳入突破性治疗药物程序”和“(五)符合附条件批准的药品”纳入优先审评审批程序。
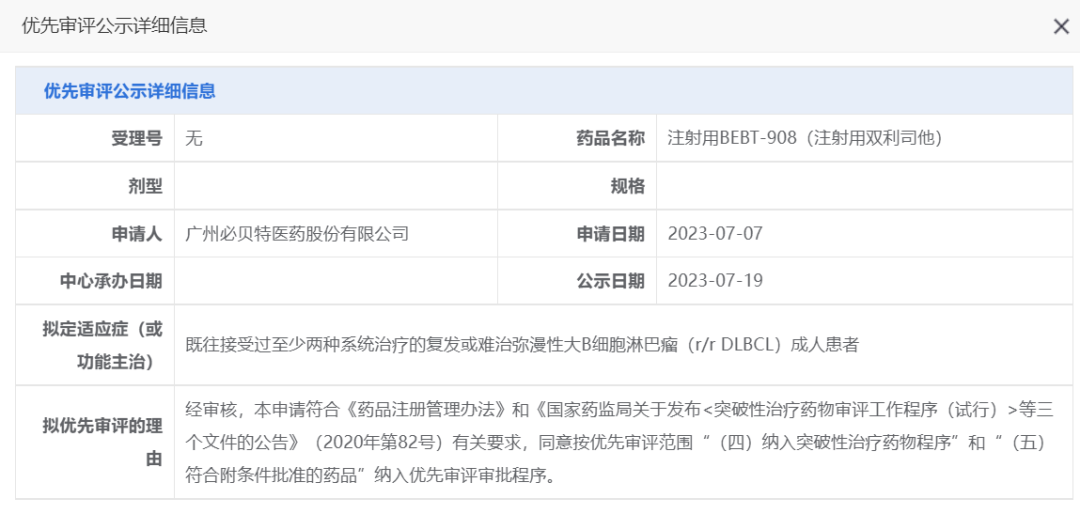
图片来源:CDE官网
DLBCL 是最常见的侵袭性 NHL 亚型,在中国DLBCL占所有NHL的45.8%,占所有淋巴瘤的40.1%。在国内,对r/rDLBCL的治疗仍然存在未满足的临床需求。
此外,BEBT-908 针对外周T细胞淋巴瘤、滤泡性淋巴瘤、慢性淋巴细胞白血病/小淋巴细胞淋巴瘤、淋巴浆细胞样淋巴瘤/华氏巨球蛋白血症等适应症均已开展临床试验。
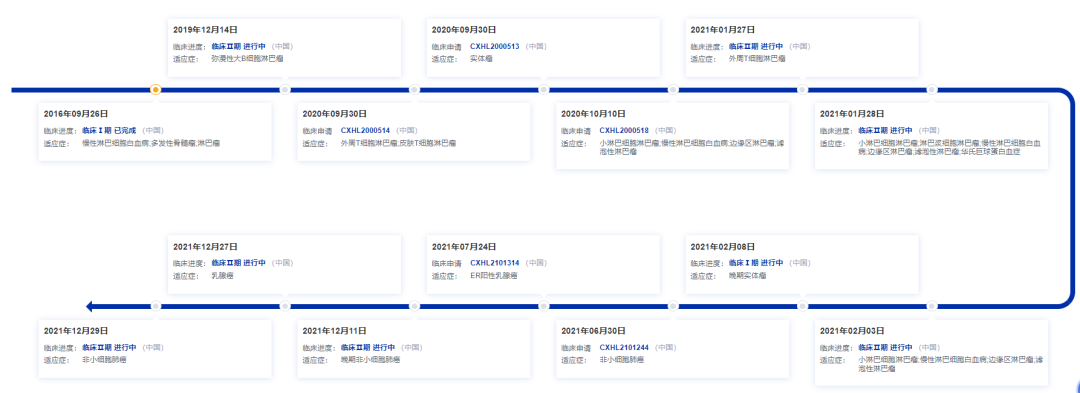
图片来源:药智数据企业版——全球药物分析系统数据库
小 结
DLBCL是成人淋巴瘤中最常见的一种类型,在亚洲国家发病率占非霍奇金淋巴瘤40%以上。尽管近年来随着治疗手段的进步,患者的生存率及缓解率有明显改善,但仍面临挑战。西达本胺片及BEBT-908有望对此类疾病的治疗起到一定帮助。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57