随着司美格鲁肽的火爆出圈,GLP-1R成为了药企争先研发的“明星靶点”。
近日,Nature、Cell两大顶级期刊双双发表减肥新机制研究结果,“GDF15”似乎也成了学术圈的心头爱。
企业不多、实力强劲
GDF15靶点在研/上市分析
目前,全球范围内尚未有针对GDF15靶点的新药获批上市,处于临床阶段的药物数量也较少。
经药智咨询分析统计,目前全球有10款GDF15靶点药物进入临床试验阶段,其中辉瑞、CatalYm GmbH及阿斯利康的3款已进入临床2期,其适应症均为肿瘤相关。
其余7款均处于临床1期,在这7款中有5款药物开展的适应症为肥胖,研究机构包括强生、诺和诺德及NGM Biopharmaceuticals Inc等公司。
表1 GDF15靶点全球在研情况
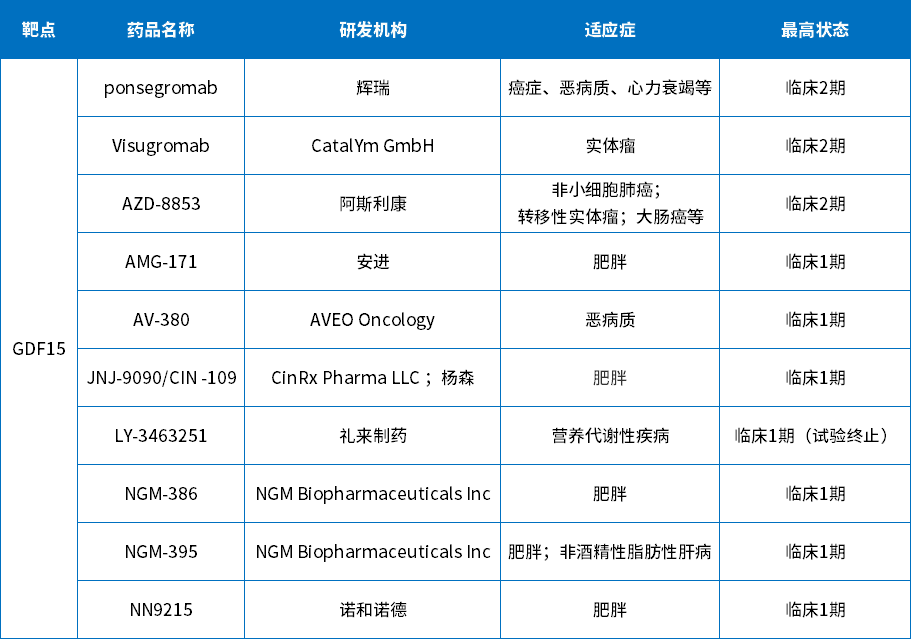
数据来源:药智数据,药智咨询整理
GDF15靶点是何方神圣?
GDF15(Growth differentiation factor 15,生长分化因子15)是一种内分泌激素,是TGF-β超家族成员,主要参与器官生长、分化、发育及细胞修复。GDF15在肝 脏和肾 脏中高度表达,并在线粒体毒素和内质网应激的所有细胞类型中被诱导,最初被确定为巨噬细胞和癌细胞分泌的可溶性因子,后来被证明可诱导恶病质并保护小鼠免受肥胖和胰岛素抵抗[1]。
大量研究表明,GDF15水平升高与心血管疾病如心肌肥大、心力衰竭、动脉粥样硬化、内皮功能障碍,以及肥胖症、糖尿病、癌症、恶液质等有关[2]。
2017年相关研究人员报道GDF15通过抑制食欲降低体重。
2019年加拿大Dr.Gregory Steinberg课题组和英国Dr.Stephen O’Rahilly课题组分别在Nature Metabolism和Nature上同时阐述了GDF15调节****通过抑制食欲达到减肥作用。
2020年Wang D.等人在Nature Reviews Endocrinology综述了GDF15的生物学作用,其可以降低体重、改善胰岛素抵抗和非酒精性脂肪肝(NAFLD)[3-5]。
GDF15的减肥机制
2023年6月28日,Nature杂志发表了一篇关于GDF15减肥机制的文章,该论文题目为:“GDF15 promotes weight loss by enhancing energy expenditure in muscle”,论文作者为麦克马斯特大学的博士后王冬冬及其研究团队。
这项研究发现了在节食过程中促进减肥、保持能量燃烧和避免体重反弹的一个关键机制:GDF15在抑制食欲的同时,通过增强肌肉能量消耗减轻了适应性产热效应(“适应性产热”又称“代谢适应性”,是指随着体重减轻,身体为了应对能量摄入的减少,其能量消耗会进入“节能模式”,新陈代谢速度减缓,体重下降速度也随之减慢),导致了与单纯热量限制相比更大的体重减轻和非酒精性脂肪肝的改善。
进一步的研究证实了GDF15的持续减重能力与肌肉有关。
通过刺激交感神经系统(SNS),GDF15上调了肌肉中的钙释放。肌肉细胞通过徒劳循环来消耗钙,并在这个过程中释放能量(让钙恢复控制这一过程需要更多的ATP,也即需要燃烧更多的卡路里),进而阻止了节食期间发生的新陈代谢减慢[1]。
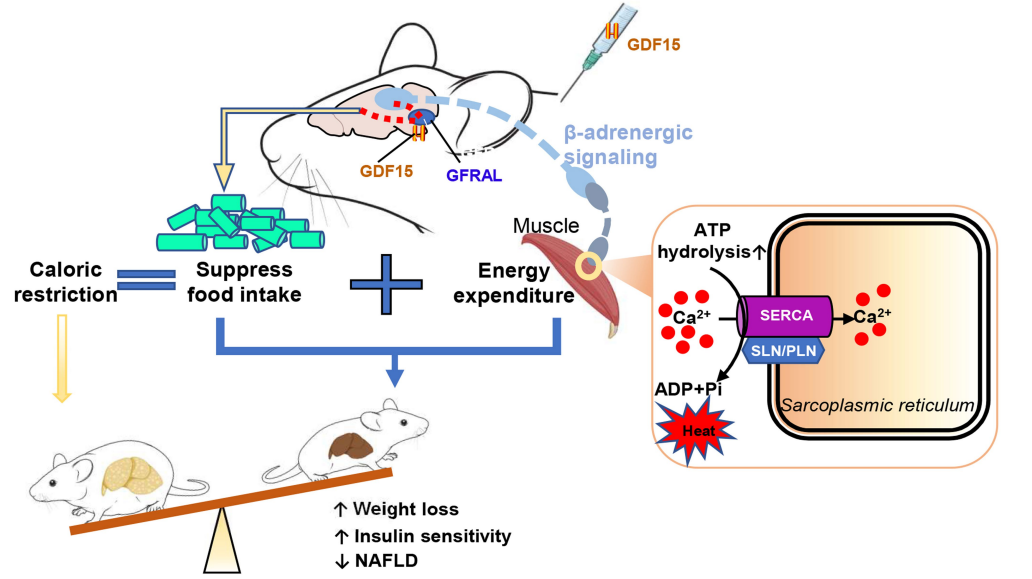
图1 连接GDF15与GFRAL和肾上腺素能受体的生物回路的机制图,以在热量限制期间维持肌肉的能量消耗
图片来源:参考文献
2023年7月10日,澳大利亚新南威尔士大学的研究人员在Cell子刊Cell Metabolism上发表了题为:“GDF15 enhances body weight and adiposity reduction in obese mice by leveraging the leptin pathway”的文章。
该文章揭示GDF15能通过瘦素通路增强对肥胖小鼠的体重和脂肪减少作用,后脑(hindbrain)中的瘦素信号通路增强了GDF15的代谢作用。GDF15通过胶质源性神经营养因子α样受体(GFRAL)在后脑极后区(AP)和孤束核(NTS)中调节其厌食作用,GDF15可能与其他在肥胖中升高的食欲调节因子相互作用,例如瘦素(leptin)。
瘦素是一种由脂肪组织分泌的激素,当动物体的体脂减少或饥饿时,血清中瘦素的含量会明显下降,从而激发觅食行为,同时降低自身能量消耗。而当体脂增加时,血清中瘦素含量会升高,进而抑制进食并且加速新陈代谢。
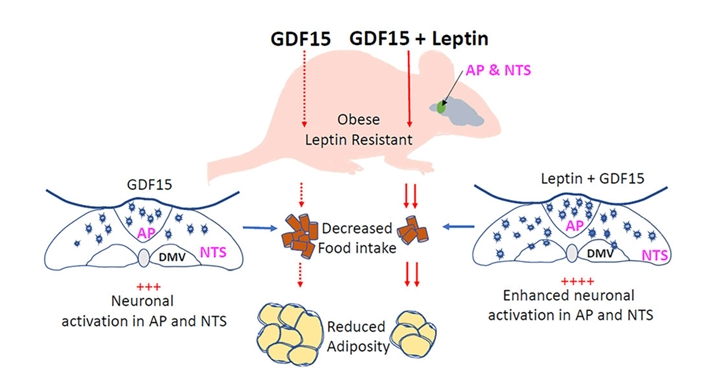
图2 GDF15与瘦素作用机制图
图片来源:参考文献
该研究进一步证明了GDF15与瘦素之间的这种相互作用是由于两条通路之间的突触连接,表达GFRAL和表达瘦素受体的神经元之间存在广泛连接,孤束核(NTS)中瘦素受体的敲低可以减少GDF15介导的极后区(AP)神经元的激活[6]。
国外顶级期刊频频发文,似乎是在提示我们:GDF15或将是下一个“GLP-1R”。
结 语
整体来看,进行GDF15靶点药物研发的企业不多,但竞争对手实力强劲,多为制药巨头。
值得一提的是,目前搜集到强生及北京质肽生物已有2款“GDF15”+“GLP-1R”双靶点药物在进行临床前研究(CIN-209、ZT007注射剂),若后续GDF15靶点药物对于肥胖患者的疗效显著,GDF15+GLP-1R双靶点药物或将是未来减肥药的研究方向。
参考文献
[1]Wang D,Townsend LK,DesOrmeaux GJ,et al.GDF15 promotes weight loss by enhancing energy expenditure in muscle.Nature.2023;10.1038/s41586-023-06249-4.
[2]https://www.163.com/dy/article/GOCVTJ850552DUJF.html.
[3]Day,E.A.et al.Metformin-induced increases in GDF15 are important for suppressing appetite and promoting weight loss.Nat Metab 1,1202-1208,doi:10.1038/s42255-019-0146-4(2019).
[4]Coll,A.P.et al.GDF15 mediates the effects of metformin on body weight and energy balance.Nature 578,444-448,doi:10.1038/s41586-019-1911-y(2020).
[5]Wang,D.et al.GDF15:emerging biology and therapeutic applications for obesity and cardiometabolic disease.Nat Rev Endocrinol 17,592-607,doi:10.1038/s41574-021-00529-7(2021).
[6]Samuel N.Breit,Rakesh Manandhar,Hong-Ping Zhang,Michelle Lee-Ng,David A.Brown,Vicky Wang-Wei Tsai.GDF15 enhances body weight and adiposity reduction in obese mice by leveraging the leptin pathway.Cell Metabolism.Issue&Volume:2023-07-10.



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57