10月2日,诺奖委员会宣布将2023年诺贝尔生理学或医学奖宣布授予德国生物技术公司BioNTech的Katalin Karikó博士和美国宾夕法尼亚大学教授Drew Weissman,以表彰他们在核苷碱基修饰方面的发现。这些发现使得高效率的新冠mRNA疫苗得以被快速研发,为无数人带来了保护,也改变了全球对抗新冠疫情的格局。
此前,该技术已获得过多项大奖,包括2022年美国科学突破奖(Breakthrough Prize)、2021年拉斯克基础医学研究奖(The Lasker Awards)、2023年盖尔德纳奖等。今年摘得诺贝尔生理学或医学奖,可谓是众望所归!
虽然新冠病毒感染疫情已迈向新阶段,但mRNA 药物应用的大门已开启,mRNA技术的应用和发展仍在继续。
揭开mRNA疫苗的神秘面纱
信使核糖核酸(messenger RNA,mRNA)疗法是基于体外转录(in vitro transcription,IVT)mRNA的一种新型有效的治疗手段。
新型病毒感染(COVID-19)疫情的突然爆发,极大地推动了mRNA技术在严重急性呼吸综合征冠状病毒2(SARS-CoV-2)疫苗研发领域的应用。与此同时,mRNA肿瘤疫苗也成为备受瞩目的研究热点领域。
通过优化和改进mRNA制备策略、mRNA疫苗递送系统、抗肿瘤免疫应答策略等,使mRNA肿瘤疫苗研发的关键技术取得了飞跃发展。
近年来,尽管肿瘤治疗取得了显著进展,但恶性肿瘤仍然是世界第二大致死原因。临床上常规的肿瘤治疗手段包括手术、放疗、化疗、靶向治疗、免疫治疗和综合治疗等。
肿瘤免疫治疗的目的是激活宿主的抗肿瘤免疫,改变抑制肿瘤的微环境,最终达到缩小肿瘤,提高患者总体生存率的目的。其中肿瘤疫苗是一种有潜力的抗肿瘤免疫治疗手段。
针对肿瘤相关抗原(tumor-associated antigen,TAA)或肿瘤特异性抗原(tumor-specific antigens,TSA)的疫苗可以特异性地攻击和摧毁高表达肿瘤抗原的恶性肿瘤细胞,并通过 免疫记忆而实现对肿瘤的持续杀伤作用。
因此,与其他免疫疗法相比,肿瘤疫苗提供了特异、安全和可耐受的治疗方法。
尽管研究者在开发肿瘤疫苗方面做出了相当大的努力,但由于肿瘤抗原的高度多样性和相对较低的免疫反应,几十年来将肿瘤疫苗转化为有效的临床治疗方法仍然具有挑战性。
迄今为止,美国FDA批准了三种治疗性癌症疫苗,分别为卡介苗(TheraCys®),一种牛分枝杆菌减毒活株,用于治疗非肌肉浸润性膀胱癌;Sipuleucel-T (Provenge®),一种用于治疗转移性去势抵抗性前列腺癌的DC疫苗;以及用于治疗晚期黑色素瘤的溶瘤性疱疹病毒疫苗(talimogene laherparepvec, T-VEC) (Imlygic®)和两种预防性癌症疫苗(HPV疫苗和乙型肝炎病毒疫苗)。
mRNA疫苗作为肿瘤疫苗的重要类型,能够编码TAA、TSA及其相关的细胞因子,同时激发体液和细胞介导的免疫反应,增加克服疫苗耐药性的可能性,从而达到加强患者抗肿瘤免疫的效果,成为一种具有良好前景的治疗方式。
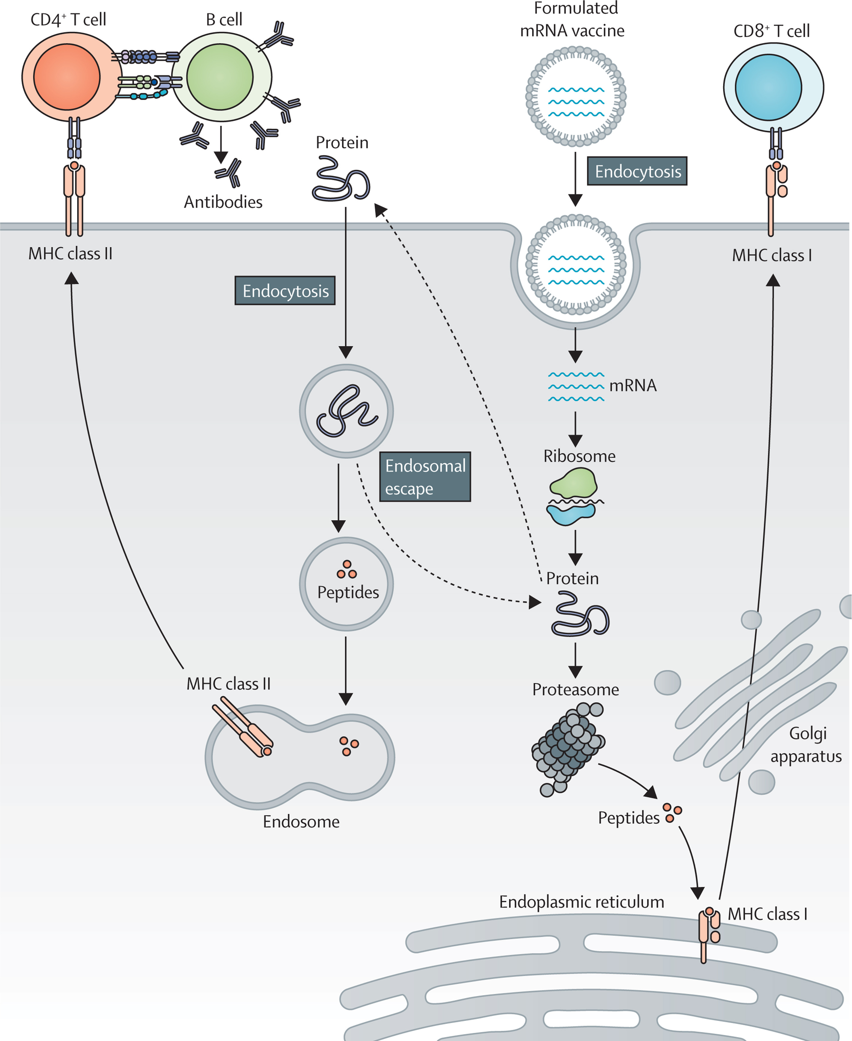
mRNA疫苗具有多种优势,如能够产生强有力的保护性免疫反应,mRNA的生产速度更快、更灵活、成本更低,可以用于精准和个性化的治疗。体外转录后再加帽加尾是mRNA肿瘤疫苗公认的生产方法,它类似于真核细胞胞浆中自然加工和成熟的mRNA。当接种疫苗部位的细胞吸收后,mRNA被运输到细胞质。接着,通过核糖体合成mRNA编码的蛋白质,然后进行翻译后修饰,产生正确折叠的功能蛋白质。mRNA疫苗可以使其编码的蛋白质或肽瞬时表达,持续几天或几周,使得mRNA更容易控制。
海外药企拔得头筹,国内药企奋起直追
目前全球已有多款mRNA肿瘤疫苗进入临床研究阶段。
企业上看,国内外药企均在积极布局。除了mRNA三大巨头BioNTech、Moderna、CureVac等国外药企,我国药企,如启辰生生物、莱美药业等也在积极布局mRNA肿瘤疫苗领域。
mRNA-4157/V940
今年2月,Moderna和默沙东合作开发mRNA癌症疫苗mRNA-4157/V940联合帕博利珠单抗组合疗法获美国FDA授予突破性疗法认定,用于高危黑色素瘤患者接受完全切除术后的辅助治疗。
mRNA-4157/V940是一种基于mRNA的新型研究性个性化癌症疫苗,所包含的编码由多达34种新抗原的单一合成mRNA分子组成。该疫苗是根据每位患者肿瘤独特的DNA序列突变特征设计制成,当疫苗被注入患者体内后,会促使患者体内产生特定的T细胞抗肿瘤反应。mRNA-4157/V940联合Keytruda治疗III/IV期黑色素瘤的2b期临床试验KEYNOTE-942/mRNA-4157-P201结果显示:与Keytruda单药治疗相比,mRNA-4157/V940联合Keytruda治疗组使患者的复发或死亡风险降低44%,符合试验的无复发生存期(RFS)的主要终点。

图片来源:默沙东官网
BNT111/BNT113/BNT122
BioNTech拥有超过30个产品管线,肿瘤相关的约15个,其正在开发针对直肠癌、黑色素瘤和其他癌症类型的治疗方法。
BNT111是基于BioNTech完全拥有的FixVac平台的开发的肿瘤疫苗,该平台利用mRNA编码的肿瘤相关抗原的固定组合,旨在触发针对癌症的强大而精确的免疫反应。已发表的BNT111治疗晚期黑色素瘤的I期临床试验结果显示:BNT111可诱导新颖的抗原特异性抗肿瘤免疫应答,并增强针对所编码的黑色素瘤相关抗原(NY-ESO-1、MAGE-A3、酪氨酸酶、TPTE)预先存在的免疫应答,这4种抗原在90%以上的皮肤黑色素瘤中表达,显示出了良好的安全性和初步抗肿瘤效果。2021年11月,BNT111被FDA授予快速通道资格。目前,BNT111已进入II期临床,联合Libtayo(cemiplimab)治疗抗PD-1疗法难治性/复发性不可切除III期或IV期黑色素瘤。
BNT-113是一款使用脂质体包裹的mRNA疫苗,编码HPV-16衍生的E6和E7修饰序列,针对HPV16+癌症。已公布的BNT113联合Keytruda一线治疗不可切除复发/转移性头颈部鳞状细胞癌的初步安全数据显示:截至2022年7月5日,在接受治疗的15例患者中,12例已完成安全磨合。安全磨合中的所有患者均有≥1次AE,最常见的是发热(8例)和寒战(6例)。
BNT122是利用BioNTech的iNeST技术平台研发的个体化新抗原mRNA疫苗,利用该平台设计的疫苗含有未经修饰的、优化后的mRNA,能够编码多达20种不同的特异性新抗原。2022 ASCO大会上公布的I期临床试验数据显示:BNT122联合PD-L1抑制剂atezolizumab和化疗在接受手术切除的胰 腺癌患者中展现出良好的有效性和安全性。
靶向Survivin DC细胞注射液
2023年1月,由启辰生生物研发的治疗脑胶质母细胞瘤的mRNA-DC疫苗—靶向Survivin DC细胞注射液获准进入临床试验,成为国内首 个获批开展临床试验的mRNA-DC肿瘤疫苗,也是全球首 个获批开展临床试验的靶向Survivin的mRNA-DC肿瘤治疗性疫苗产品。
靶向Survivin DC细胞注射液是将抗原mRNA负载的树突状细胞(DC),分别通过皮内注射和静脉回输的方式给予患者,诱导抗原特异的CD4+和CD8+T淋巴细胞,为原发性脑胶质母细胞瘤患者术后清除肿瘤残余细胞,防止复发,延长生存期,实现长期抗肿瘤效果提供全新的治疗手段。前期非临床研究和研究者发起的探索性临床试验数据已经表明,该mRNA-DC疫苗可诱导出抗Survivin特异性肿瘤免疫反应,安全性良好,有效性显著,试验患者的总生存期显著延长。
CUD002
2023年9月,莱美药业子公司四川康德赛的“CUD002注射液”临床试验申请获得临床试验默示许可,拟开展治疗难治性/耐药复发性卵巢癌的临床试验。CUD002是中国首 款基于肿瘤新生抗原的mRNA编辑DC肿瘤治疗性疫苗,根据患者独特的突变信息定制设计并制造,能激发患者自身免疫系统识别卵巢癌抗原,产生抗肿瘤免疫反应并杀伤肿瘤细胞。
mRNA癌症疫苗的挑战和趋势
遗传不稳定性会助力癌症的发展,并形成其异质性,导致肿瘤患者对治疗的不同敏感性。
随着对单个突变抗原认识的加深,测序技术的突破,以及大数据和机器学习的兴起,以经济和廉价的方式快速、准确地鉴定患者特定的突变已经实现。同时,通过优化mRNA序列和改善制备条件等策略的应用,突破了以往mRNAs不稳定和免疫刺激活性强的瓶颈,这些技术进步为以个性化mRNA疫苗为代表的精准医学的广泛实施奠定了坚实的基础。
然而,机遇总是伴随着挑战。
一方面,对新表位免疫原性的研究很有限,没有发现免疫原性新表位的一般规律。另一方面,在疫苗制备时,体外负载DC递送系统在早期肿瘤疫苗递送中起着重要作用,但目前还缺乏直接比较哪种递送工具在安全性和运输效率方面更具优势的研究。
目前,mRNA肿瘤疫苗的临床试验正在积极开展,总体处于研发的早期阶段。有报道结果的临床试验,特别是个性化的mRNA肿瘤疫苗试验仍然很少,而且治疗效果在不同的患者中表现出较大的差异。因此,需要更多更深入的研究,继续探索最合适的治疗人群、临床环境、给药途径、给药剂量和途径,以及联合治疗,才能实现肿瘤免疫治疗的又一次突破,造福于广大肿瘤患者。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57