尿路上皮癌是全球发病率排名第十三的常见癌症,高发年龄为50-70岁,男性尿路上皮癌的发病率为女性的3-4倍。随着ADC、「靶向+免疫」联合疗法等创新疗法取得一定成果,尿路上皮癌靶向治疗时代俨然开启。
临床需求庞大,一线化疗mOS仅14个月
根据弗若斯特沙利文数据,2020年全球尿路上皮癌病例51.6万人,预计到2025年将达到58.6万人,到2030年预计达到66.3万人。在中国,尿路上皮癌2020年新发病例约7.7万人,预计到2025年将达到9.1万人,到2030年将达到10.6万人。
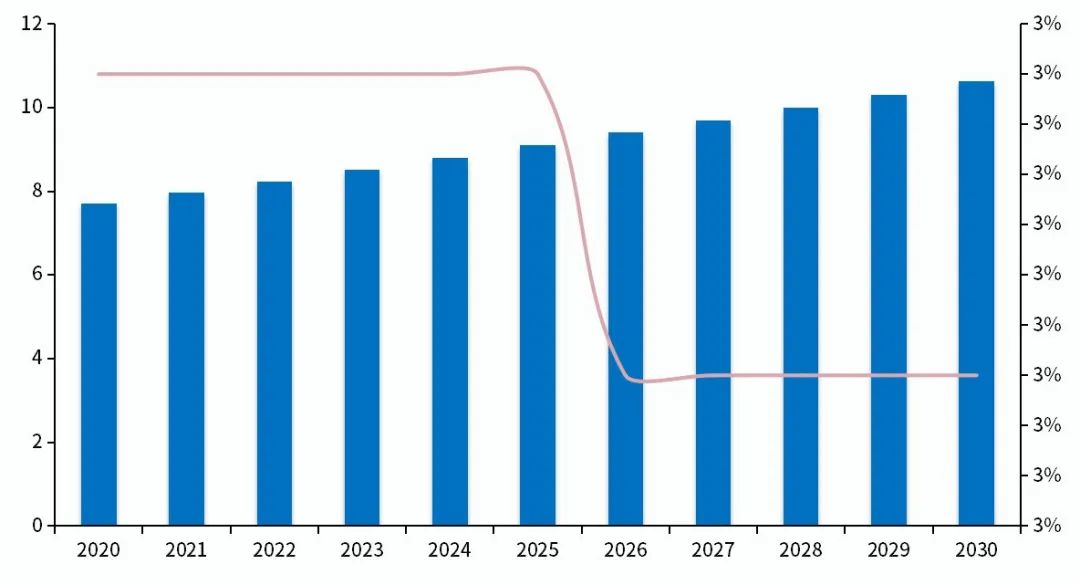
庞大的患者人群往往蕴含着巨大的市场机会。然而,尿路上皮癌目前的标准治疗方案是以吉西他滨联合顺铂为代表的化疗方案,中位总生存期仅14个月。而对于由于肾功能不全、表现不佳或其他重大合并症而无法接受顺铂治疗的患者,卡铂的中位总生存期仅9个月。因此,倘若免疫疗法在中位总生存期上能突破20个月,无疑将改写尿路上皮癌的治疗方案。
而Nectin-4便是这一适应症的破局者!
Nectin-4靶点:破局的关键
Nectin-4(Nectin cell adhersion molecule 4)是一种Ⅰ型膜蛋白,分子量为66kDa,在正常的胚胎和胎儿组织中含量很高,成年后下降,在健康组织中的分布有限。但Nectin-4可通过激活P13K/Akt通路促进肿瘤的增殖和迁移,与尿路上皮癌、乳腺癌、胰 腺 癌、三阴乳腺癌等的发生和发展息息相关,有研究表明,60%膀胱癌样本中可见中高水平Nectin-4蛋白表达。肿瘤组织和正常组织中表达水平的差异,使得Nectin-4成为ADC药物研发领域一个备受关注的靶点。
目前,全球仅一款Nectin-4 ADC获批上市,为Seattle Genetics/安斯泰来的Padcev,于2019年获FDA批准上市,并于2023年3月向CDE递交了上市申请。Nature预测Padcev的全球销售额有望在2026年达到35亿美元。除了MIBC外,Padcev正在开发NMIBC适应症,一旦能成功破局,空间更是有望打开天花板!
Nectin-4 ADC在研格局
国内处于临床阶段的Nect
in-4 ADC共5款,百奥泰、石药集团、迈威生物、科伦博泰的Nectin-4 ADC处于Ⅰ期临床。从临床的角度,Padcev先发优势明显,领先其他Nectin-4 ADC数个身位,但是Padcev存在皮肤毒 性的黑框警告,因此,谁能在安全性上更胜一筹,未来市场有望斩获更佳的市场份额。
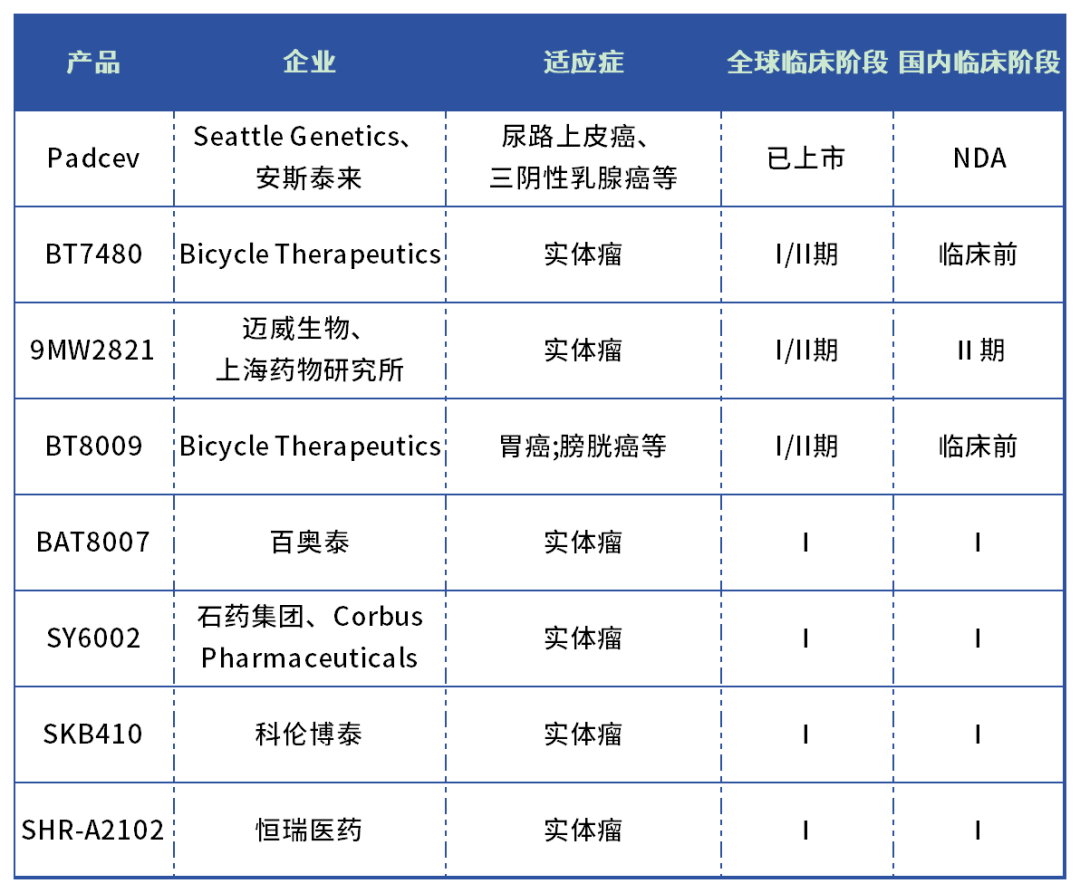
(1)Padcev(EV,Enfortumab Vedotin)是全球第一款及唯一一款获批上市的Nectin-4 ADC药物,2019年获FDA批准先前接受过含铂化疗和一种PD-(L)1抑制剂的局部晚期或转移性尿路上皮癌适应症,于2023年4月获FDA批准联合K药一线治疗mUC适应症。2023年上半年,Padcev销售额达2.8亿美元。
一线mUC适应症的获批大幅提升了Padcev的销售峰值预期。2023年4月,FDA批准Padcev联合K药一线治疗mUC适应症,Ⅲ期试验显示, EV联合帕博利珠单抗组和EV单药组的ORR为64.5% vs 45.2%,CR为10.5% vs 4.1%,mOS为22.3m vs 21.7m。这一适应症的获批验证了PD-1联合ADC的潜力,22.3个月的总生存期远优于化疗14个月的总生存期。此外,Padcev单药的数据亦展现出良好的治疗前景,单药21.7个月的总生存期疗效十分卓越。
但Padcev存在严重和致命的皮肤不良反应,包括史蒂文斯-约翰逊综合征(SJS)和中毒 性表皮坏死松解(TEN)。一旦发现SJS和TEN,须立即停止Padcev的使用并寻求特别的医护治疗。鉴于黑框警告是医生最为担心的副作用,这为后来者提供了弯道超车的思路。

(2)礼来瞄准了Padcev存在皮肤黑框警告的软肋,押注下一代Nectin-4 ADC药物。Emergence Therapeutics是一家专注于ADC药物开发的公司,其核心管线是一款Nectin-4 ADC药物(ETx-22)。2023年8月,礼来宣布已完成对Emergence Therapeutics的收购,根据Endpoints和多位分析师计算,礼来须支付约4.7亿美元,其中首付款1.35亿美元。
ETx-22是下一代Nectin-4 ADC,目前处于临床前阶段。通过优化,ETx-22具有更高的疗效和更低的毒 性,尤其是皮肤毒 性,而目前已获批上市的同靶点ADC药物Padcev带有严重皮肤毒 性的黑框警告。
临床前研究显示,ETx-22能与肿瘤细胞表达的Nectin-4选择性、高亲和力地稳定结合,并具有肿瘤特异性解偶联,避免了伤害正常细胞,从而降低毒 性,有望提供更高剂量并增加治疗的疗效。
期待看到ETx-22的临床数据,包括其疗效和安全性的潜力。
(3)9MW2821是全球第二个进入临床开发阶段的 Nectin-4 ADC 新药,由迈威生物研发,用于治疗实体瘤。目前正处于Ⅱ期临床多个队列扩展入组阶段,评价在尿路上皮癌、宫颈癌、前列腺癌、三阴性乳腺癌、非小细胞肺癌等实体瘤的抗肿瘤疗效。
2023年4月,迈威生物公布9MW2821于二线及以上实体瘤患者中的临床研究进展。初步数据显示,在Ⅱ期试验推荐剂量(RP2D)下,12例尿路上皮癌肿评受试者中,客观缓解率(ORR)达50%,疾病控制率(DCR)达100%;6例宫颈癌肿评受试者中,ORR达50%,DCR达100%。且在RP2D下同样体现了良好的安全性。
从RP2D的数据来看,9MW2821凭借50%的ORR具有超越Padcev成为BIC的潜力,作为国内临床进展最快的国产Nectin-4 ADC药物,9MW2821市场值得期待。
(4)BT8009是Bicycle Therapeutics 旗下一款Nectin-4 ADC药物,目前处于临床Ⅰ期。在Ⅰ/Ⅱ期研究中,共纳入21名末线UC患者,截至2023年3月31日,BT8009的ORR达43%,其中一名患者完全缓解。在5 mg/m2 QW RP2D的剂量,ORR达57%,CR达14%。在RP2D的剂量,未出现3级及以上的皮肤毒 性、眼毒 性及神经毒 性,展现出良好的安全性优势。
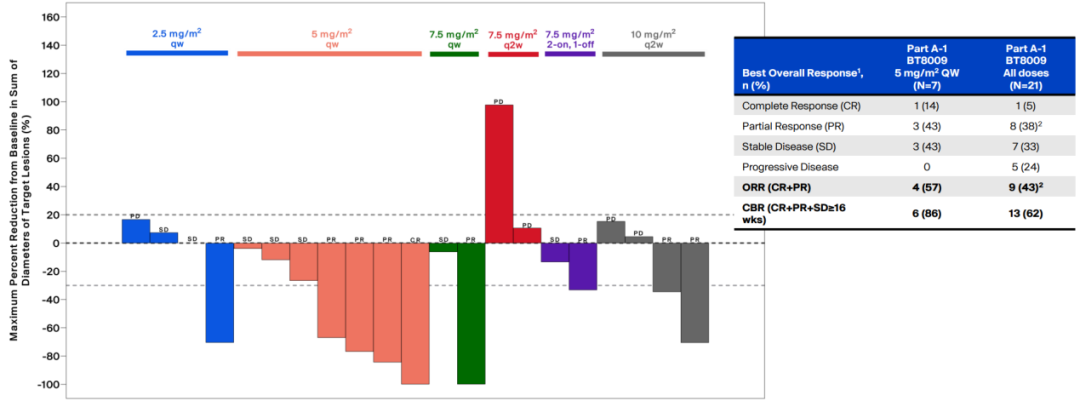
(5)SYS6002是石药集团旗下一款Nectin-4 ADC,采用酶催化定点抗体偶联技术,能将有效的有丝分裂及制剂MMAE针对性地导向Nectin-4表达的癌细胞,而其连接子的稳定性有助于将高浓度的MMAE送达肿瘤中,并同时通过减少不良的全身暴露量而将副作用减低。
SY6002于2022年10月获CDE批准临床。2023年2月,SY6002成功出海,公司与Corbus Pharmaceuticals就SY6002在美国、欧盟国家、英国、加拿大、澳大利亚、冰岛、列支敦士登、挪威及瑞士的开发及商业化订立独家授权协议。根据协议条款,石药巨石生物将收取750万美元的首付款,并有权收取最多1.30亿美元的潜在开发及监管里程碑付款以及最多5.55亿美元的潜在销售里程碑付款。
小 结
Nectin-4靶点已获验证。Padcev销售额逐步攀升,一线UC适应症的落地更是进一步拔高了药品的销售峰值。但Padcev存在严重的皮肤毒 性,FDA强调Padcev可引起严重和致命的皮肤不良反应,包括SJS)中毒 性表皮坏死松解症(TEN)。因此,企业正加速研发安全性更佳、疗效更好的Nectin-4 ADC药物。
放眼国内,迈威生物、百奥泰、石药集团、恒瑞医药等正在加速研发Nectin-4 ADC,其中迈威生物的9MW2821展现出卓越的疗效优势,ORR达50%,较Padcev疗效更加明显。礼来亦高度看好这一赛道,通过收购Emergence Therapeutics押注下一代Nectin-4 ADC药物,未来谁能脱颖而出,让我们拭目以待。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57