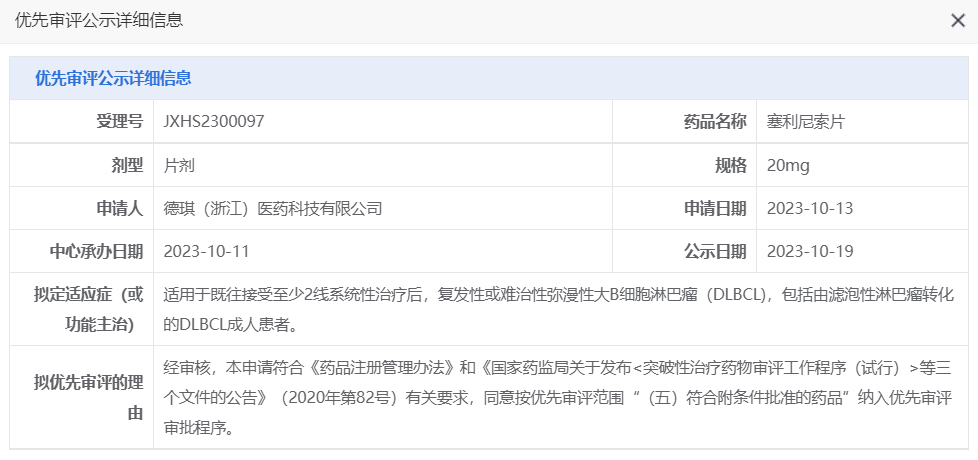
10月19日,CDE官网显示,德琪(浙江)医药科技有限公司「塞利尼索片」拟纳入优先审评,用于既往接受至少2线系统性治疗后,复发性或难治性弥漫性大B细胞淋巴瘤(DLBCL),包括由滤泡性淋巴瘤转化的DLBCL成人患者。
塞利尼索是全球批准的第一个选择性口服核输出蛋白(XPO1)抑制剂,通过抑制XPO1,可促使肿瘤抑制蛋白和其他生长调节蛋白的核内储留和活化,并下调细胞浆内多种致癌蛋白水平。
目前,塞利尼索已在国外获批三项适应症:
联合地塞米松用于治疗已接受至少四种既往治疗且对至少两种蛋白酶体抑制剂、两种免疫调节剂和一种抗CD38单克隆抗体药物难治的成人复发/难治性多发性骨髓瘤(R/R MM)(FDA 2019/07);
单药用于治疗既往接受过至少二线系统性治疗的成人复发/难治性弥漫性大B细胞淋巴瘤(R/R DLBCL)(非特指),适应症包括由滤泡淋巴瘤转化的DLBCL(FDA 2020/06);
联合硼替佐米和低剂量地塞米松,用于治疗既往接受过至少一线治疗的成人MM(FDA 2020/12)。
此外,塞利尼索还被开发用于治疗骨髓纤维化、复发/难治性非霍奇金淋巴瘤、复发/难治性T细胞淋巴瘤和NK细胞淋巴瘤、子宫内膜癌。其中骨髓纤维化适应症于今年7月被FDA授予快速通道资格认定。
弥漫性大B细胞淋巴瘤(DLBCL)方面,已公布的塞利尼索治疗复发难治性DLBCL(R/R DLBCL)的单臂多中心、开放性2b期临床研究SADAL结果显示:经塞利尼索单药治疗后,所有受试者总有效率(ORR)为28%,完全缓解(CR)率为12%。对86例R/R DLBCL受试者的肿瘤大小进行评估,56例(65%)患者经塞利尼索治疗后肿瘤体积缩小,其中33例(38%)患者肿瘤体积缩小>50%。中位随访11.1个月时,中位缓解持续时间(mDOR)为9.3个月。中位随访14.7个月时,中位总生存期(mOS)为9.1个月。
基于SADAL研究结果,FDA于2020年6月批准塞利尼索用于治疗既往接受过至少2线的R/R DLBCL(包括由滤泡性淋巴瘤[FL]转化而来)。
塞利尼索由Karyopharm Therapeutics研发,2018年德琪医药引进该药。2021年12月,该药在国内被NMPA批准,联合地塞米松用于治疗既往接受过治疗且对至少一种蛋白酶体抑制剂,一种免疫调节剂以及一种抗CD38单克隆抗体药物难治的R/R MM成人患者。为了扩大塞利尼索的覆盖范围,提高其可及性,2023年8月,德琪医药与翰森制药达成合作。此次塞利尼索针对R/R DLBCL的上市申请在国内纳入优先审评,将加速其获批治疗R/R DLBCL的上市进程。
关于R/R DLBCL及其治疗进展
弥漫性大B细胞淋巴瘤(DLBCL)是一种来源于成熟B细胞的非霍奇金淋巴瘤(NHL),是NHL最常见的类型。利妥昔单抗联合环磷酰胺、阿霉素、长春新碱和泼尼松(R-CHOP)方案是DLBCL的标准一线治疗方案,但仅50%-60%患者可以实现长期缓解。
挽救化疗后自体干细胞移植是目前治疗复发或难治性(R/R)DLBCL的标准疗法。但SCHOLAR-1研究显示,只有26%的患者对下一步挽救性治疗有反应,仅有少数病人能够符合自体移植条件,中位总生存期(OS)仅为6.3个月。整体来看,R/R DLBCL还存在很大未满足的市场需求。
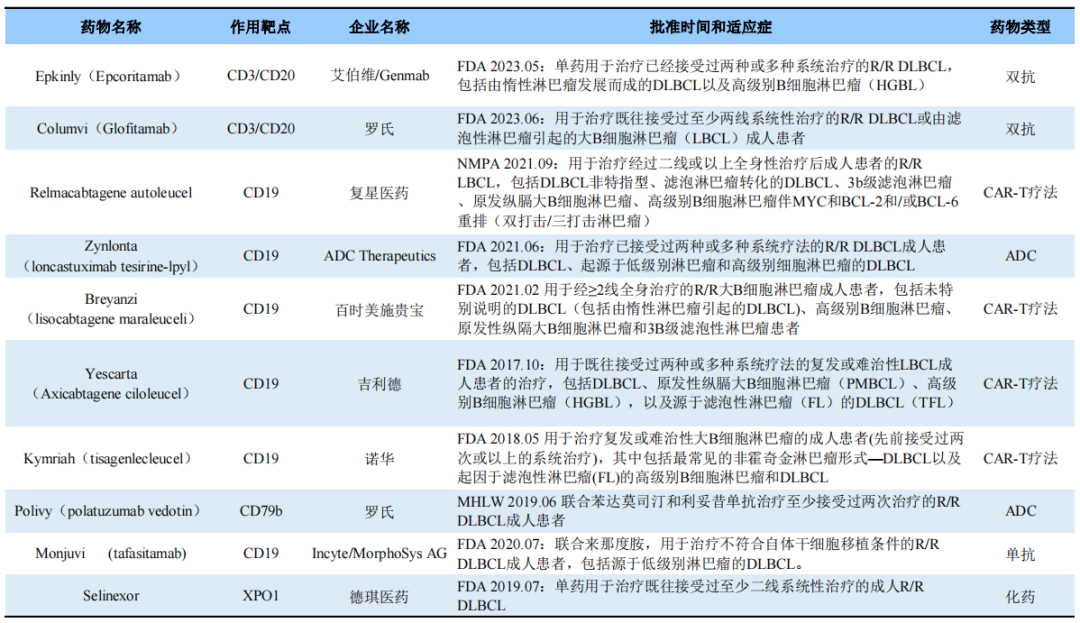
据不完全统计,目前全球监管机构已批准几款R/R DLBCL新疗法,详见下表。已获批的R/R DLBCL主要包括CD19靶向嵌合抗原受体T细胞免疫疗法(CAR-T疗法)和抗体偶联药物(ADC)、CD3/CD20靶向双抗,这些药物主要被批准用于DLBCL的三线及以上治疗。
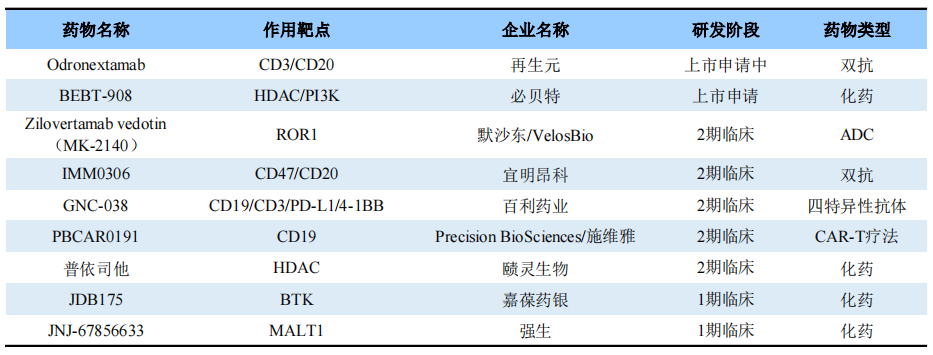
除了上述药物,目前全球还有多款药物被开发用于治疗R/R DLBCL,详见下表。这些药物中再生元的Odronextamab和必贝特的BEBT-908进展较快,目前已经申报上市。
Odronextamab
Odronextamab是再生元利用其专有的VelocImmune技术和Veloci-Bi双特异性平台开发的一款CD3/CD20靶向双抗,其用于治疗至少接受过两种系统治疗的R/R DLBCL和R/R FL的生物制品许可申请(BLA)正在美国接受优先审查,PDUFA日期为2024年3月31日。
Odronextamab的BLA是基于1期研究ELM-1和2期研究ELM-2的积极结果。已公布的ELM-1研究结果显示:接受80 mg或更高剂量Odronextamab治疗的既往未接受过CAR-T疗法治疗的DLBCL患者的ORR为53%,CR为53%。而接受80 mg或更高剂量Odronextamab治疗的既往接受过CAR-T疗法治疗的DLBCL患者的ORR为33%,CR率为27%。
而已公布的ELM-2研究数据显示:接受Odronextamab治疗后,在平均随访21个月时,既往未接受过CAR-T疗法治疗的复发/难治性DLBCL的ORR(肿瘤大幅缩小或消失的比例)为49%,CR(肿瘤完全消失的比例)为31%。平均缓解持续时间为18个月。
若顺利获批,Odronextamab将成为全球第一个同时获批治疗滤泡性淋巴瘤和DLBCL的双抗。
BEBT-908
BEBT-908是必贝特自主研发的一种靶向PI3K和HDAC的小分子双靶点抑制剂,对多种血液肿瘤和实体瘤均具有很强的抗肿瘤作用。已公布的BEBT-908治疗R/R DLBCL的2a期临床研究结果显示:BEBT-908在2期推荐剂量(22.5mg/m2)下的ORR达50.0%,且安全性良好。
2021年9月,BEBT-908被CDE纳入突破性治疗品种,用于治疗经过至少2种系统治疗后R/R DLBCL。今年7月,该药用于治疗既往接受过至少2种系统治疗的R/R DLBCL成人患者的上市申请被CDE纳入优先审评。
VLS-101
默沙东也积极布局DLBCL市场,通过收购VelosBio公司获得抗体偶联药物(ADC)MK-2140。该药由ROR1靶向单抗和甲基澳瑞他汀E(MMAE)偶联而成,在人类血液恶性肿瘤和实体瘤小鼠模型中显示出强大的抗肿瘤活性。
ESMO 2021上公布的VLS-101治疗淋巴系统恶性肿瘤患者的1期临床研究数据显示:5名DLBCL患者中,3名达到客观缓解(ORR为60%),其中1名部分缓解,2名完全缓解。
PBCAR0191
PBCAR0191是Precision BioSciences与施维雅合作开发的一款通用型同种异体CD19靶向CAR-T疗法。2022年6月,Precision BioSciences公布的最新临床试验数据显示:在接受过自体CAR-T疗法治疗后复发DLBCL患者中,PBCAR0191达到100%客观缓解率,73%完全缓解率,50%的患者缓解持续时间超过6个月。
BEBT-908是一种靶向PI3K和HDAC的小分子双靶点抑制剂,其治疗R/R DLBCL的2a期临床研究结果显示:BEBT-908在2期推荐剂量(22.5mg/m2)下的ORR达50.0%,且安全性良好。
总结
整体来看,近年来R/R DLBCL已取得不错进展,多款新疗法,如CD19靶向CAR-T疗法、ADC先后获批上市。此外,目前全球还有多款新药被开发用于治疗R/R DLBCL。整体来看,在研R/R DLBCL疗法药物靶点愈发丰富,涉及ROR1、HDAC、MALT1等。而且,除了化药、单抗、ADC、CAR-T疗法,四特异性抗体如GNC-038也被开发用于治疗R/R DLBCL。期待在药企的不懈努力下,R/R DLBCL早日迎来更多新疗法,满足该领域未被满足的巨大市场需求。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57