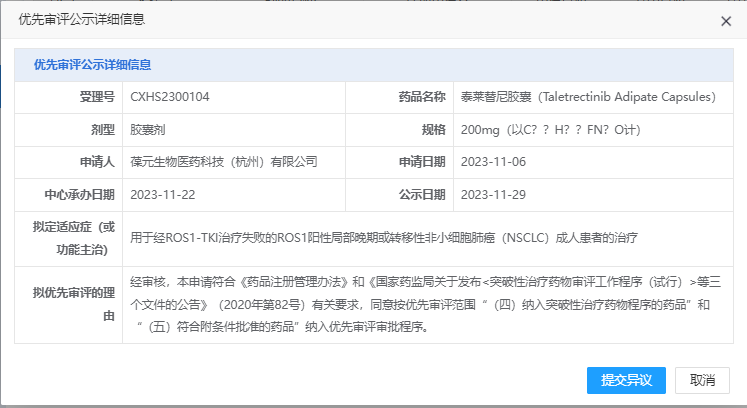
2023年11月29日 ,根据中国国家药监局药品审评中心(CDE)官网显示,信达生物和 葆元医药合作开发的泰莱替尼(Taletrectinib)胶囊拟被纳入优先 审评品种。泰莱替尼是新一代ROS1/NTRK抑制剂,用于经ROS1-TKI治 疗失败的ROS1阳性局部晚期或转移性非小细胞肺癌(NSCLC)成人患 者的治疗。11月22日泰莱替尼胶囊已提交上市申请,并获得CDE受理 。
交易历程
泰莱替尼最初由 由第一三共开发, 2018年12月葆元医药获得了该药的全球独家开发 、生产和商业化权益。
2021年6月,信达 生物与葆元医药达成协议,共同在大中华区(包括中国大陆、香港、 澳门及台湾)开发和商业化泰莱替尼。2023年10月,葆元医药将泰莱 替尼在日本的商业化权益授予Nippon Kayaku,获得4000万美元的预 付款,并有望在药物商业化后根据年净销售额获得潜在的监管和销售 里程碑付款以及特许权使用费。
临床疗效
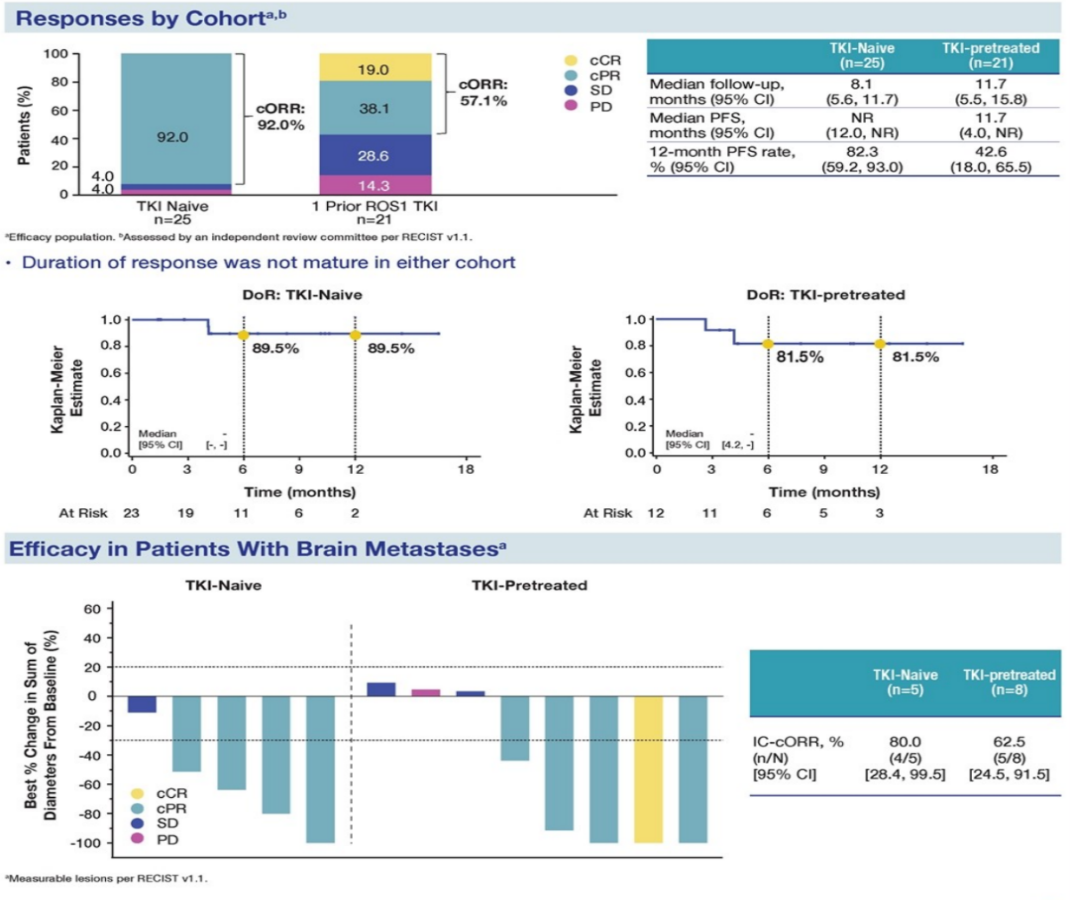
2023年ESMO大会 报道了Taletrectinib关键临床II期研究中分析结果。此次数据披露 了研究队列1(TKI初治)中25例患者、队列2(使用过1种ROS1-TKI) 中的21例患者,在队列1和队列2中,Taletrectinib治疗的cORR分别 为92.0%和57.1%,中位DoR均尚未达到,12个月DoR率分别高达89.5% 和81.5%,队列1中12个月PFS率为82.3%;队列2的中位PFS则为11.7个 月,12个月PFS率为42.6%。对基线有脑转移的患者,Taletrectinib 对脑转患者疗效显著在队列1和队列2中的颅内cORR也分别达到80.0% 和62.5%。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57