2023年9月14日,Madrigal Pharmaceuticals(新泰医药)宣布FDA已接受Resmetirom治疗NASH成人患者的新药申请,并授予优先审评资格。FDA预计于2024年3月14日前完成审评。Madrigal Pharmaceuticals已于7月完成向FDA滚动提交Resmetirom治疗NASH的新药申请。Resmetirom有望成为首 款获批上市的NASH治疗药物。
NASH药物有望成为医药投资的下一个风口。一方面,NASH患病人群庞大,预计到2025年全球NASH患者人群达4.1亿人,到2030年NASH患者达4.8亿人。国内2025年NASH患者预计达4600万人,到2030年达5550万人;另一方面,NASH领域尚无治疗药物获批上市,吉利德、辉瑞、诺华等MNC相继失败于NASH药物的研发。巨大的市场和未满足的临床需求,极易诞生下一个重磅炸 弹药物,鉴于此,NASH药物的研发万众期待。
放眼2023年,NASH领域先后经历了奥贝胆酸的上市受阻,以及Resmetirom成功NDA。2023年NASH领域还有哪些看点,值得关注,本文将抛砖引玉。
Resmetirom向FDA递交上市申请
Resmetirom(MGL-3196)是Madrigal Pharmaceuticals旗下一款甲状腺激素受体(THR)-β抑制剂,有望成为全球首 款获批上市的NASH药物。甲状腺激素通过激活肝细胞中的β受体,在肝功能中发挥核心作用,影响从血清胆固醇和甘油三酯水平,到肝脏中脂肪病理性积聚等一系列健康参数。
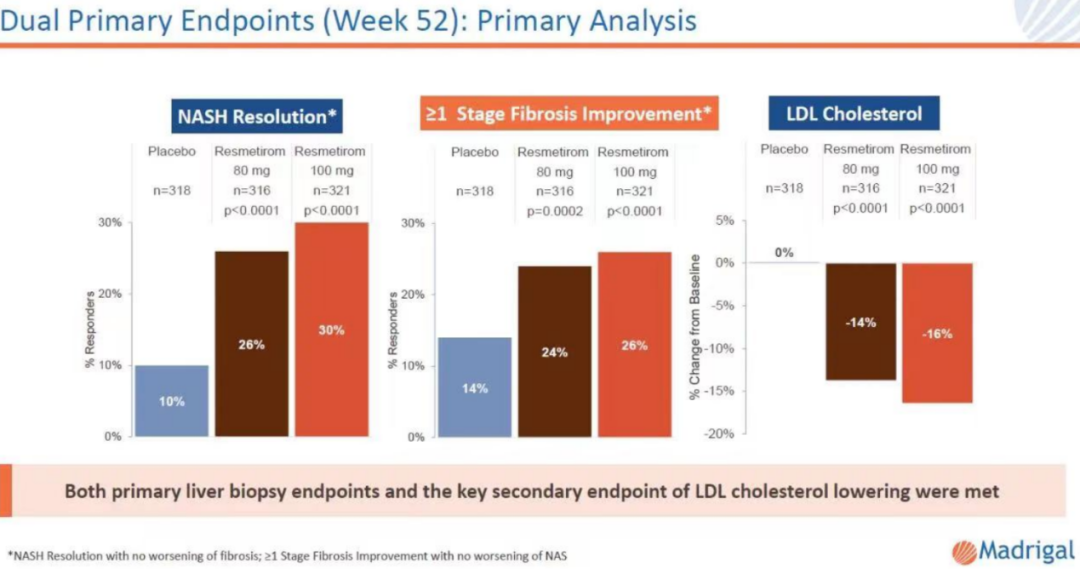
2022年12月,Madrigal Pharmaceutical宣布Resmetirom治疗Ⅲ期临床MAESTRO-NASH达到主要终点和关键次要临床。52周的肝活检数据表明,相比安慰剂,每日口服80mg或100mg的resmetirom治疗NASH和肝纤维化两个主要终点均达到,其中:
1)NASH方面,NAS评分改善≥2且纤维化无恶化的患者比例为26%(80mg)和30%(100mg),显著优于安慰剂组10%;
2)肝纤维化方面,评分改善≥1级且NAS无恶化的患者比例为24%(80mg)和26%(100mg),显著优于安慰剂组14%。同时实现多个次要终点,安全耐受性良好。
从疗效的角度,无论是对NASH抑或肝纤维化的改善,Resmetirom均较安慰剂取得了显著的治疗优势。叠加良好的安全性,Resmetirom有望成为全球首 款获批上市的NASH治疗药物。
奥贝胆酸二次上市失败
Intercept停止NASH领域投资
奥贝胆酸(OCA)一度被认为是NASH领域首 个诞生的药物,然而二次上市重蹈失败覆辙。奥贝胆酸是一种法尼酯X受体(FXR)激动剂,2016年5月首获FDA批准治疗原发?性胆汁性胆管炎。实际上,奥贝胆酸首 个NDA于2020年6月被FDA拒绝,与安慰剂相比,奥贝胆酸只有高剂量组达到改善一级纤维化患者比例这个终点,但高剂量组有51%患者出现皮肤瘙痒、9%患者因此退出试验。
Intercept没有放弃,2022年7月,Intercept公司公布了奥贝胆酸治疗NASH关键3期试验的新中期分析积极结果。这次新的中期分析总共包含了931位病患,ITT人群的中期分析结果显示,在随机分配每天服用1次25mg 奥贝胆酸的病患中,有22.4%达到试验主要终点,亦在第18个月时,其纤维化程度至少改善一个阶段且NASH情况没有恶化。与此同时,只有9.6%的安慰剂组病患达成这一指标(p<0.0001)。
尽管25mg组实现了统计学差异,但10mg奥贝胆酸组的数据与安慰剂组并没有统计学差异。且25mg组又一次错过了NASH情况改善且肝纤维化程度没有恶化的终点。此外,奥贝胆酸严重瘙痒的副作用依然明显,25mg组和10mg组以及安慰剂组瘙痒的发生率分别为55%、33%和24%,瘙痒的发生与药物剂量呈现相关性。鉴于此,在2023年5月19日,专家会认为25mg奥贝胆酸对肝纤维化2~3级NASH患者的风险大于益处。6月22日,Intercept宣布收到FDA的完整回应函,公司决定停止所有NASH领域所有投资。
2023年NASH领域潜力药物
除了Resmetirom外,2023年多款NASH药物值得期待,涉及的药物包括Efruxifermin和ASC40等。
(1)Efruxifermin(EFX)是Akero Therapeutics旗下一款Fc-FGF21融合蛋白。2022年9月13日,Akero Therapeutics宣布Efruxifermin的2b期研究(HARMONY)达到主要终点,
在50mg和28mg组中,分别有41%和39%的患者接受24周Efruxifermin治疗后,至少经历了1级肝纤维化的改善,同时没有NASH的恶化,而安慰剂组的仅有20%的受试者经历了肝纤维化的改善,具有显著性差异。试验同时达到了次要终点,76%和47%的受试者接受Efruxifermin治疗后,实现了NASH的改善,并且无纤维化的恶化,安慰剂组仅15%。同时,41%和29%接受50mg和28mg的受试者达到了两个指标的改善(即NASH缓解以及肝纤维化改善≥1级),安慰剂组仅5%。
总的来看,HARMONY研究结果是目前NASH治疗中疗效最强劲的,Efruxifermin有望成为NASH领域的BIC药物。Akero Therapeutics计划于2023Q4披露Efruxifermin在F4级纤维化中的Ⅱb期肝穿数据。
(2)ASC40是Sagimet Biosciences和歌礼制药旗下一款每日一次的口服小分子脂肪酸合成酶(FASN)抑制剂,FASN是非酒精性脂肪性肝炎患者中脂肪的新生通路中关键酶,FASN主要负责合成多余脂肪,并激活NASH患者的纤维化和炎症机制。
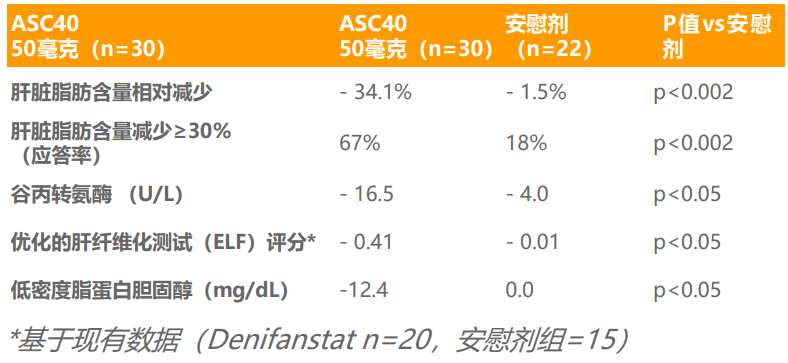
在2022AASLD上,Sagimet Bioscience宣布ASC40 (Denifanstat)治疗非酒精性脂肪性肝炎(NASH)患者2b期临床试验(FASCINATE-2)取得积极期中数据。数据显示,NASH各项关键标志物有统计学意义上的显著减少,包括肝脏脂肪含量、炎症和纤维化标志物,这进一步验证了早期研究中观察到的结果。
ASC40目前正有序开展在给药第52周进行的最终评估,全部患者的活检评估预计于2023年底完成。主要疗效终点包括NAFLD活动评分(NAS)的组织学(肝穿活检)改善且纤维化无恶化,或脂肪性肝炎缓解且纤维化无恶化;次要终点检测炎症、纤维化和肝损伤等生物标志物。
小 结
目前,FDA、EMA以及NMPA均未批准任何一款针对NASH的药物上市,NASH治疗仍然空白。此外,NASH患者人群庞大,作为一种慢性病,须长期甚至终生服药,市场空间巨大。鉴于Ⅲ期的优异数据,Resmetirom的NDA有望诞生首 款NASH药物。放眼2023年, Akero Therapeutics的Efruxifermin有望于四季度披露在F4级纤维化中的Ⅱb期肝穿数据,歌礼制药的ASC40将读出肝穿数据。NASH药物研发,虽道阻且长,但必定终闻花香。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57