今日(12月7日),CDE将和记黄埔医药(上海)有限公司(以下简称“和黄医药”)的醋酸索乐匹尼布片(HMPL-523)纳入拟优先审评品种,用于治疗既往接受过一线标准治疗(糖皮质激素、免疫球蛋白)无效或复发的成人原发慢性免疫性血小板减少症(ITP)。

有望成为全球第二款,
索乐匹尼布的可及性如何?
ITP是一种复杂的、多种机制共同参与的获得性自身免疫性疾病,全球首 款脾酪氨酸激酶(Syk)抑制剂Fostamatinib在2018年获FDA批准上市,用于治疗免疫性血小板减少症(ITP)患者。截至目前,尚无第二款Syk抑制剂获批上市。
Syk是Fc受体和B细胞受体信号传导通路的关键组成部分,可介导B细胞免疫受体的信号传导及其他细胞受体介导的免疫应答,靶向Syk的抑制剂能够干扰炎症和免疫疾病的发生和进展。索乐匹尼布是一款新型、高选择性的口服Syk抑制剂,拟用于治疗血液恶性肿瘤和自身免疫性疾病。
今年8月,和黄医药宣布,索乐匹尼布治疗成人ITP的中国关键性3期研究ESLIM-01达到持续应答率的主要终点以及所有的次要终点。此前,索乐匹尼布已被CDE纳入突破性治疗品种,本次申报上市并纳入拟优先审评品种便基于此。
据和黄医药此前公告显示,成人ITP发病率约为每年3.3名/10万人,患病率为9.5名/10万人,在中国约有11万原发免疫性血小板减少症患者,而中国之外的主要医药市场中约有14.5万名慢性免疫性血小板减少症患者。
在ITP之外,索乐匹尼布用于治疗温抗体型自身免疫性溶血性贫血和惰性非霍奇金淋巴瘤的研究也在进行中。
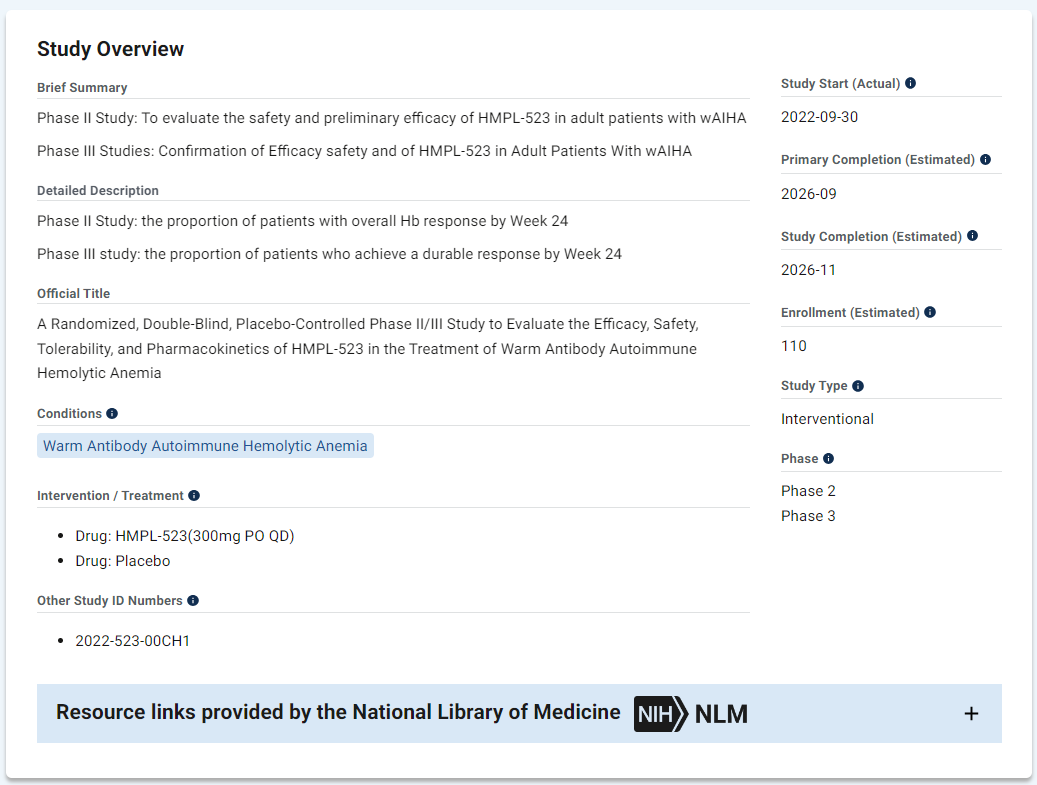
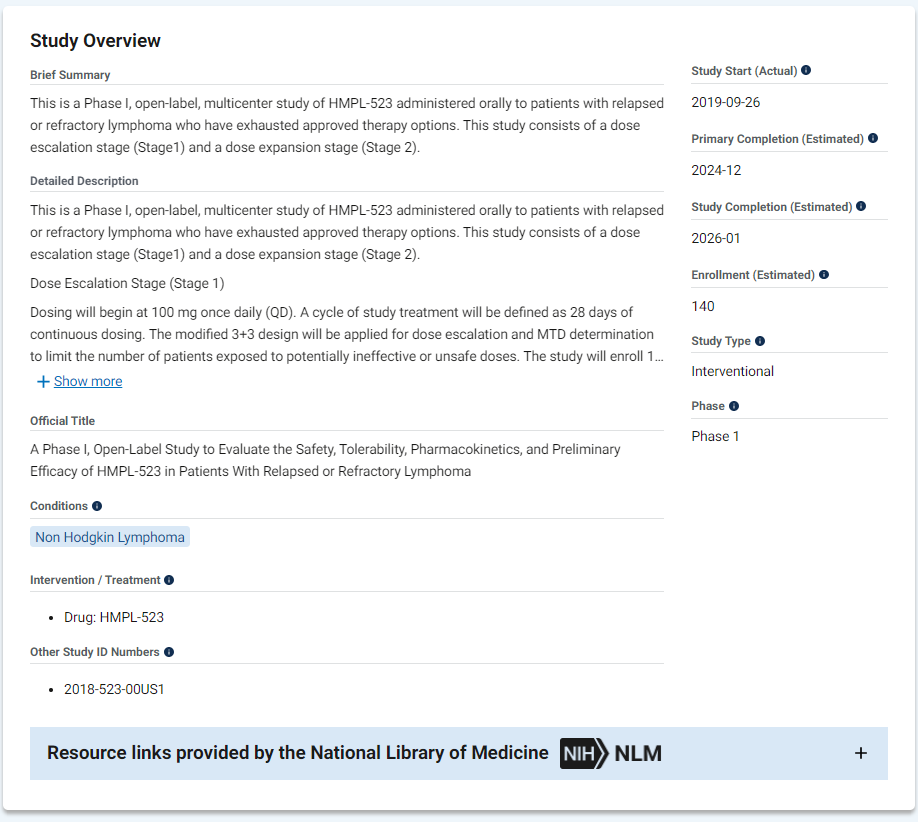
适应症在全球范围内的拓展有望为索乐匹尼布带来更大的可及性。
呋喹替尼开路,
下一位出海者是谁?
今年以来,和黄医药多个产品取得突破性进展。
11月,呋喹替尼成功出海。美国FDA提早了超过20天、通过优先审评通道批准呋喹替尼上市,该药物成为了美国首 个且唯一获批用于治疗经治转移性结直肠癌的针对3种VEGF(VEGFR1/2/3)受体激酶的高选择性抑制剂。此外,在获批后不到48小时,呋喹替尼便开出了首张处方。
“替尼三将”中,另外“两将”也在追击中。今年1月,赛沃替尼与奥西替尼的联合疗法已获美国FDA授予快速通道资格,此外还正开展肾癌的全球性临床试验。索凡替尼在中国开展了一系列临床试验的同时,也在日本开展了神经内分泌瘤的单药疗法桥接研究。
此前,和黄医药在年报中提到,将视中国3期研究的结果,决定是否在美国启动索乐匹尼布的1期免疫性血小板减少症临床试验。前文提到,索乐匹尼布取得了优秀的中国3期研究的结果。换言之,索乐匹尼布同样有望成为和黄医药继呋喹替尼后下一款出海药物。
小结
在优秀的临床结果加成下,索乐匹尼布有望将适应症可及性进一步扩大。同时,随着临床管线进度加速,和黄医药有望迎来下一款出海产品。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57