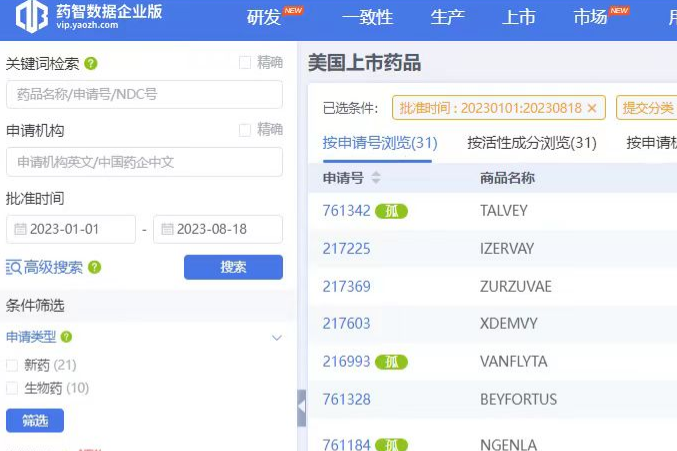
据药智数据统计,截至2023年8月18日,FDA已批准31款新分子实体,其中RSV疫苗、T1D细胞疗法药物Lantidra、血友病以及杜氏肌萎缩症基因疗法、产后抑郁症的口服药物等多款药物实现重大突破,均成为相应治疗领域全球首 款获批上市药物。
Zuranolone:
首 款治疗产后抑郁症的口服药物
2023年8月4日,FDA批准Zuranolone上市,该药物是首 个治疗成年人产后抑郁症的口服药物,Zuranolone为渤健和Sage Therapeutics的共同开发的一款GABAA受体调节剂。
临床数据显示,服用该药后3天便可起效,并可持续至45天。同安慰剂组相比,产后抑郁症患者服用50 mg规格Zuranolone第15天时,抑郁症状具有统计学和临床意义的改善。第15天,接受Zuranolone治疗的患者HAMD-17总分的最小二乘均值较基线的变化为-15.6,而接受安慰剂治疗的患者为-11.6,均值差异为-4分。
产后抑郁症是一种严重的抑郁发作,通常发生在分娩后,但也可能在妊娠后期开始,是一种严重的并且可能危及生命的疾病。因此Zuranolone的获批上市,对于孕期的女性都具有重要意义,很可能是其产后走出“鬼门关”的一味良药。
AREXVE:
首 款RSV疫苗
2023年5月3日,FDA批准葛兰素史克的AREXVE上市,是首 个呼吸道合胞病毒疫苗,主要用于预防60岁及以上的人群因呼吸道综合征病毒引起的下呼吸道疾病。
临床数据显示,AREXVY疫苗可降低RSV相关LRTD的发病风险82.6%,降低了严重RSV相关LRTD的发病风险94.1%。
RSV病毒传染性强,通常发病于秋冬季节。据统计,美国每年大约有6万-12万65岁以上人群因呼吸道合胞病毒感染而住院,同时导致6000-12000人因此死亡。
该疫苗在秋季到来之前获批上市,对于60岁以上人群来说无疑是一种福音。该疫苗是美国FDA批准的首 款RSV疫苗,也是全球首 个获得监管机构批准的RSV疫苗。
Beyfortus:
全球首 款针对婴幼儿以及儿童RSV疫苗
2023年7月17日,阿斯利康/赛诺菲共同研发的Beyfortus获批上市。与AREXVE类似,两者皆为RSV疫苗,但不同点是,Beyfortus是全球首 款针对婴幼儿以及儿童的RSV疫苗。
临床数据显示,Beyfortus可将早产儿出现MA RSV LRTI的风险降低70%,在足月儿或者晚产儿中可将MA RSV LRTI的风险降低75%。
新生儿在刚出生至两周岁前,较容易感染RSV病毒,Beyfortus的获批,将为无数家庭以及婴幼儿平添一道保障,对于家中有怀孕以及有婴幼儿的家庭具有重要的意义。
Lantidra:
全球首 款T1D细胞疗法
2023年6月28日,美国生物技术公司CellTrans开发的全球首 个T1D细胞疗法药物Lantidra获批上市,至此全球首 款针对糖尿病的细胞疗法诞生了。根据所公布的临床数据,其效果更是不俗。
临床数据显示,21名患者使用Lantidra后可1年及以上的时间摆脱外源胰岛素,11名患者使用Lantidra后可1-5年的时间内摆脱外源胰岛素,10名患者使用Lantidra后可5年以上的时间摆脱外源胰岛素,此外还有5名患者还需继续依赖外源胰岛素。
当前全球糖尿病患者超5亿人,我国更是有1.4亿人以上的糖尿病群体,其中90%为2型糖尿病患者,所以若能彻底消灭糖尿病,将很大程度上缓解我国医疗压力。
药物研发的终 极目标就是彻底消灭某种疾病,随着细胞疗法进军T1D领域,或许距离彻底治愈真的不远了。
Omisirge:
全球首 款现货型细胞疗法
2023年4月17日,以色列制药公司Gamida Cell开发的Omisirge获FDA批准上市,成为全球首 款现货型细胞疗法药物。
该药物为同种异体脐带血细胞疗法,可加速患者体内中性粒细胞的恢复,同时降低感染风险。该药物主要用于治疗成人和12岁及以上的儿童血液癌患者。
临床数据显示,在接受Omisirge的患者中,有87%的患者中性粒细胞恢复,恢复时间的中位数为12天。相比之下,在接受脐带血移植的患者中,有83%的患者中性粒细胞恢复,恢复时间的中位数为22天。此外,在移植后100天内,接受Omisirge治疗的患者中39%存在细菌或真菌感染,而接受脐带血移植组为60%。
Roctavian:
全球首 款A型血友病基因疗法药物
2023年6月29日,FDA批准了BioMarin Pharmaceutical公司的Roctavian上市,该药物为基于AAV病毒的的基因疗法药物,同时也为首 款获批FDA用于治疗成人A型血友病的基因疗法药物。
该药物的优势为患者只需接受一次治疗,即可持续表达凝血因子VIII,从而不再需要长期接受凝血因子注射。
临床数据显示,112名患者在接受Roctavian治疗之前,基线年化出血率(ABR)为5.4次出血/年,在接受Roctavian治疗后,基线ABR为2.6次出血/年(随访时间中位数为3年),患者的ABR减少了52%。
此外,相比于接受常规FVIII预防性治疗,接受Roctavian治疗可显著降低自发性出血和关节出血发生率。接受Roctavian治疗时自发性出血与关节出血的平均ABR分别为0.5次/年与0.6次/年,而接受常规FVIII预防性治疗自发性出血与关节出血的平均ABR分别为2.3次/年与3.1次/年。
最后,ISTH 上公布的3期GENEr8-1研究结果显示,与基线相比,研究受试者的治疗出血总体减少了82.9%,ROCTAVIAN使FVIII的使用量总体减少了 96.8%。
Elevidys:
全球首 款杜氏肌萎缩症基因疗法药物
2023年6月22日,Sarepta Therapeutics公司的Elevidys(SRP-9001)获得了FDA加速批准上市,Elevidys为全球首 款用于治疗4~5岁儿童杜氏肌营养不良症的基因治疗药物。
在SRP-9001-103的研究中,研究结果显示,经过52周的治疗后,NSAA评分可改善3.8分。
在SRP-9001-101的研究结果中显示,经过SRP-9001长期治疗,四年后SRP-9001治疗的参与者NSAA总分的平均差异为7.0分。
此外,根据SRP-9001-101、102和103的综合结果,与对照组相比,NSAA评分在52周时具有统计学意义。
小 结
研发新药的意义在于更好的治疗某种疾病,而上述7款药物都在各自的领域中取得了重大的突破,期待后续可以有更多的新药好药问世,造福全球患者。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57