近日,FDA同时批准两款基因疗法上市,分别为福泰制药/CRISPR共同研发的CRISPR/Cas9基因编辑疗法药物Casgevy以及蓝鸟生物研发的基因疗法药物Lyfgenia,更为有趣的是,两款药物适应症相同,皆具有治疗12岁及以上患有复发性血管闭塞现象的镰状细胞病的作用。FDA此番操作,成功将基因疗法推上风口浪尖。
Casgevy与Lyfgenia由于适应症相同,又恰好同日获批,其临床效果分别怎样?未来又会碰撞出什么样的火花?
正面“硬刚”,谁将是最后大赢家?
评判一款药物的好坏,自然是离不开有效性、价格以及副作用的严重程度等多维度数据。
Casgevy为全球首 款获批的CRISPR基因编辑药物,早于今年11月在英国药监局获批上市。
有效性方面,在为期24个月的随访期间至少连续12个月内,共有44名患者接受Casgevy治疗,其中31名患者时间治疗及随访达到要求,在这31名患者中,29 名患者在至少连续12个月的时间里未出现严重血管阻塞事件,有效性达93.5%。而接受Lyfgenia的32名患者中,在为期6-18个月的评估中,有30名患者未发生严重血管闭塞,占比达94%,此外28名患者未出现血管闭塞事件,占比88.2%。从有效性数据对比来看,两款药物打了个平分秋色。
价格方面,Casgevy定价为220万美元,折合人民币1570万元。而Lyfgenia定价为310万美元,折合人民币2220万元。所以价格方面无疑是Casgevy更具优势。而Casgevy能够定价较低,还是得益于研发成本较低。由于Casgevy是基于CRISPR/Cas9基因编辑技术,而Lyfgenia是基于慢病毒载体,所以Casgevy具有天然的成本优势,这也是Casgevy定价远低于Lyfgenia的底气所在。
安全性方面,这也是患者最为担心的一项,也是当今基因疗法药物急需改进的地方,毕竟基因疗法药物若是出现不可预知的严重副作用,那么无异于是在人体内埋藏了一颗“定时炸 弹”。
Casgevy最常见的副作用为血小板和白细胞水平低、口腔溃疡、恶心、肌肉骨骼疼痛、腹痛、呕吐、发热性 中性粒细胞减少症、头痛以及瘙痒等症状。
Lyfgenia常见的副作用与Casgevy相似,但Casgevy最大的优势就是并未被FDA黑框警告,而竞品Lyfgenia由于可能导致患者发生血液恶性肿瘤,所以被FDA黑框警告。安全性方面,Casgevy无疑是再下一城。
综上所述,效果方面两款药物平分秋色,而价格以及安全性方面无疑是Casgevy取得了胜利。而市场方面似乎也是给出了自己的答案,12月8日,蓝鸟生物直接暴跌40%,被迫停牌,在这一场博弈中,似乎资本也并不站在蓝鸟一方。
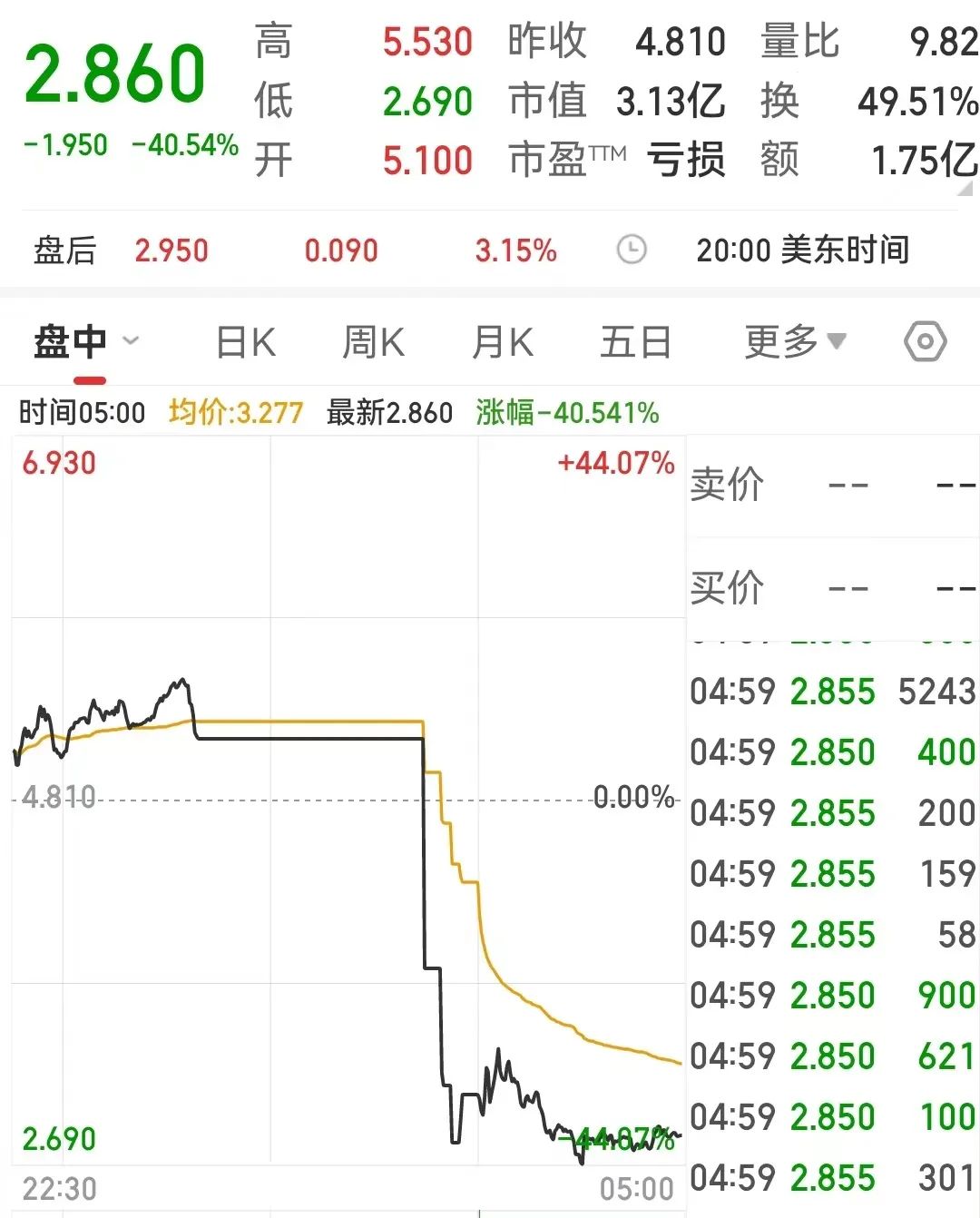
图1 蓝鸟生物股价
图片来源:同花顺
综合考虑,如果以上两款药物能够有一款大赢家,Casgevy无疑是更有胜算。然而基因疗法“一劳永逸”能否让患者买单?如若患者不买单,在这场没有硝烟的战争中,或许将不会存在赢家。
天价药,患者能否买单?
基因疗法药物虽说具有“一劳永逸”的可能性,然而高额的定价却让绝大部分的天价药“翻车”。
Hemgenix:由uniqure/CSLbehring共同研发,定价350万美元/剂,适应症为B型血友病。2023年前三季度,uniqure根据协议分得50万美元。
Skysona:由蓝鸟生物所研发,定价300万美元/剂,适应症为肾上腺脑白质营养不良。2023年前三季度营收仅为1086万美元,按售价来计算,大约只有3-4名患者接受该药物治疗。
Zynteglo:同为蓝鸟生物所研发,定价280万美元/剂,适应症为β-地中海贫血症。根据蓝鸟生物2023年Q3财报,Zynteglo的2023年前三季度仅867.8万美元。
Glybera:由uniqure所研发,为全球首 款AAV基因疗法药物,定价100万美元,适应症为脂蛋白脂肪酶缺乏症。自2012年欧洲上市后,仅有一位患者接受过治疗,于2017年无奈退市。
以上几款基因疗法药物,高额的定价,即使在经济发达的美国以及欧洲上市后依旧不被患者所接受。所以即使基因疗法药物具有“一劳永逸”可能,可在高额的定价背景下,依旧不被患者所买单。
但凡事皆有例外,基因疗法药物也有成功的案例。
Zolgensma:由诺华研发,定价212.5万美元/剂,适应症为脊髓性肌萎缩症。若是说以上几款药物为基因疗法药物失败方的代表,那么Zolgensma则是基因疗法药物胜利方的代表。Zolgensma在2019年销售额达3.61亿美元,2020年销售额9.2亿美元,2021年销售额达13.51亿美元,2022年销售额达13.7亿美元,2023年前三季度销售额达9.28亿美元。
Elevidys:由Sarepta 和罗氏共同开发,定价320万美元/剂,适应症为杜氏肌营养不良症。在仅销售两个月的时间里,Elevidys在2023年前三季度便斩获0.69亿美元的销售额。
以上两款基因疗法药物皆取得了不错的成绩,在同样高额定价的背景下,或许选择开发合适的适应症才是关键。
辉瑞54亿美元押注入局
纵然基因疗法研发成本高昂,市场接受度不理想。但也拦不住其他企业的布局热情,辉瑞就是其中一员。
就在Lyfgenia和Casgevy获批的后两日,美国血液学会(ASH)2023 年年会暨展览会上,辉瑞展示了其正在研究的镰状细胞病( SCD )治疗药物 GBT601的 II/III 期初步研究结果,研究结果显示该药物能显著提高血红蛋白水平。
GBT601 是镰状血红蛋白 (HbS) 的新一代聚合抑制剂。它通过提高 HbS 与氧的亲和力来防止血液中的红细胞镰状化。辉瑞将 GBT601 定位为其 Oxbryta 的后继药物,Oxbryta 是一种 HbS 聚合抑制剂,于 2019 年 11 月获得 FDA 批准用于 SCD。
在 ASH 大会上公布的数据来自 35 名患者,其中大多数患者已完成至少 12 周的治疗。17名受试者接受了100mg剂量的GBT601,每天两次负荷剂量,持续四天,之后每天给药一次。其余受试者则服用了 150 mg的 GBT601。
12 周后,接受 100 mg剂量治疗的受试者血红蛋白平均增加了 2.67 g/dL,而接受 150 mg剂量治疗的患者平均血红蛋白增加了 3.17 g/dL。研究人员还发现了溶血指标从基线下降的良好趋势。
研究人员指出,GBT601 的旋转细胞计数结果也显示“红细胞变形能力显着改善”。此外,他们报告说,使用 GBT601 时,脱氧过程中镰状细胞的中位点较基线在第 6 周和第 12 周有所下降,表明镰状细胞 Hb 的聚合可能被延迟。
GBT601 和 Oxbryta 最初由总部位于加利福尼亚州的 Global Blood Therapeutics 公司研发,辉瑞于 2022 年 8 月斥资 54 亿美元的价格收购了该公司,将两款药物收入囊中,正式入局基因疗法。
就当前的数据来看,GBT601研发进展良好,辉瑞54亿美元的押注还在燃烧着希望。另一方面,GBT601表现的积极数据,对于近期频陷困境的辉瑞而言也算是一剂安慰剂。
但GBT601离上市还有很长的路要走,是否会加入“百万天价药”俱乐部,现在讨论都还为时尚早。但是,GBT601为SCD 带来了新的治疗希望,后续表现值得我们期待。
小结
两款基因疗法药物的同时获批,似乎预示着“基因魔盒”即将全面开启,然而有关于基因疗法药物的两大世纪难题还需科学家们继续破解,即安全性问题以及高昂的成本,当这两大难题解决后,迎接基因疗法药物的将是光明的未来。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57