11月15日,国家药品监督管理局药品审评中心官网显示,阿斯利康首次提交AZD0486(TNB-486)临床申请。
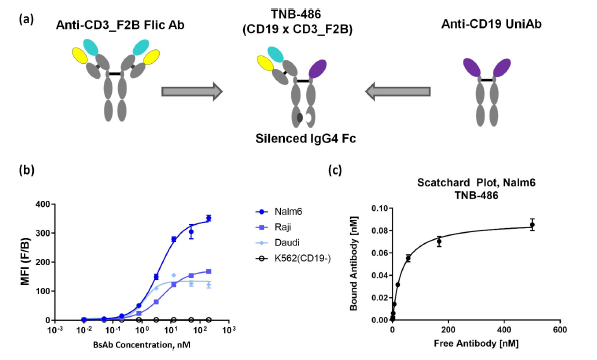
AZD0486是一款新型、全人源靶向CD19xCD3 IgG4的双抗,属于双特异性T细胞衔接器 (BiTE)。
临床前研究显示,TNB-486通过与CD19(B细胞上表达的抗原)和T细胞上的CD3受体结合,激活T细胞并将其募集到表达CD19的肿瘤中,引发免疫反应。
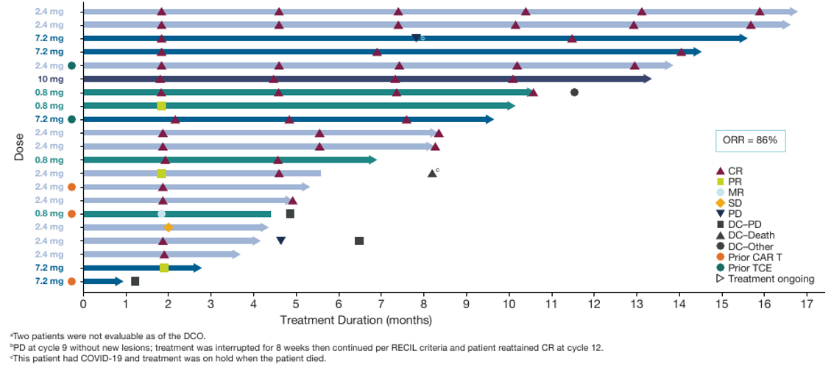
2023年美国血液学会(ASH)公布了AZD0486正在进行的I期FIH研究中实施双次剂量递增给药后更新的安全性数据,共纳入65例B-NHL患者,包括16例CAR-T细胞治疗失败和3例CD20单抗治疗失败的患者。
结果显示,中位随访5.72个月,整体患者客观缓解率(ORR)为86%,中位缓解持续时间(DOR)未达到,在2.4mg剂量组完全缓解(CR)率为91%(10/11);2.4mg或以上剂量的疗效可评估FL受试者,83%(14/17)实现了CR,客观缓解率(ORR)达88%。
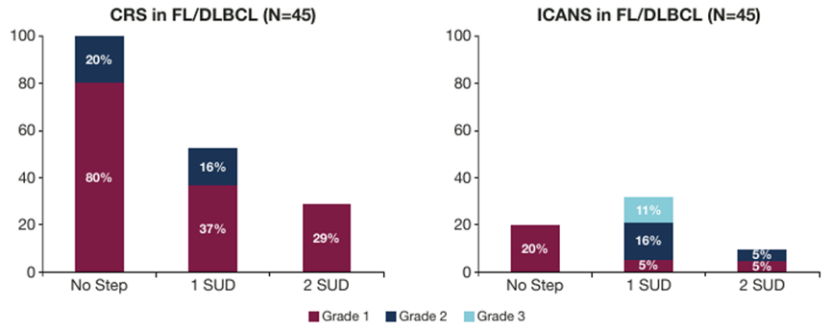
安全性方面,实施双次剂量方案后,未观察到≥3级CRS或ICANS,同时,对于DLBCL/HGBL及FL患者,相比于单次及固定剂量给药,双次剂量方案1-2级CRS发生率及1-2级ICANS发生率显著降低。
交易信息
2022年7月5日,阿斯利康宣布将以12.65亿美元的价格收购TeneoTwo公司,这份协议包括处于一期临床阶段的药物TNB-486,具有交易内容包括:阿斯利康将收购TeneoTwo的所有未偿股权,以换取交易完成时的1亿美元预付款。此外,根据协议条款,阿斯利康将向TeneoTwo的股东支付高达8.05亿美元的额外或有研发相关里程碑付款以及高达3.6亿美元的额外或有商业相关里程碑付款。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57