阿尔茨海默症患者的脑海中,仿佛有一块橡皮擦,擦去了记忆和时光。这是一件多么可怕的事情,意味着你的成就、你的经历、你的所爱,全部都离你而去,那么活着,也仅仅只是活着而已。多年来,全球药企投入了巨大的经费进行阿尔茨海默症药物的研发,但大部分以失败告终,前路茫茫似乎看不到希望。
所幸,我们生活在一个不断进取的时代,随着近期阿尔茨海默症新药在中国的获批,这一长久未曾进展的领域正在不断透进光来。
重磅新药
仑卡奈单抗(Lecanemab)的获批,似乎正在成为治疗阿尔兹海默症的一个里程碑。作为2003年来首获美国FDA完全批准的治疗阿尔兹海默症新药,仑卡奈单抗确实十分优秀。
2022年11月,仑卡奈单抗针对早期阿尔兹海默症的III期试验结果发表在国际权威医学期刊《新英格兰医学杂志》上。这项被称为Clarity AD研究的试验共在北美、欧洲、亚洲的235个研究点入组1795名患者,主要终点为治疗18个月后临床痴呆评分总和(CDR-SB)相较于基线的变化,该评分越高意味着患者临床功能越低。
试验结果显示,接受治疗18个月后,仑卡奈单抗组和安慰剂组的CDR-SB评分分别为1.21和1.66。相较安慰剂组,仑卡奈单抗组CDR-SB评分低0.45,评分增速降低了27%。此外,接受治疗6个月后,仑卡奈单抗组CDR-SB评分就开始出现显著性差异,且两组评分的绝 对差异随着时间的推移而扩大。
基于观察到的数据和外推至30个月的CDR-SB进行的斜率分析,接受仑卡奈单抗治疗25.5个月相当于安慰剂治疗18个月时的水平,这表明仑卡奈单抗可以延缓疾病进展达7.5个月。
仑卡奈单抗使患者CDR-SB的临床下降减少了27%
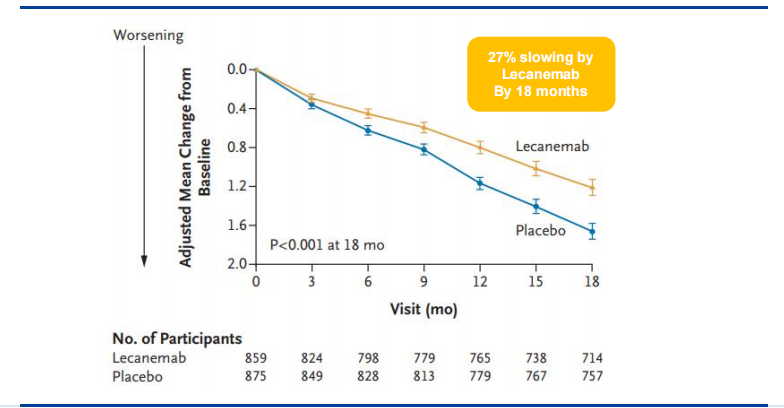
图片来源:华福证券研报
这项临床试验也成为仑卡奈单抗在此次中国获批的依据。
仑卡奈单抗成功上市,也为后来者在阿尔茨海默症治疗药物的研发注入了一剂强心剂。不过,也不能过于乐观,因为到目前为止,阿尔茨海默症的发病机制对人类来说,还是个迷。
未解之谜
1907年,德国医生Alois Alzheimer发表了一个病例,他持续跟踪一名女性患者的病程进展直至她在发病后四年半死亡,并在患者脑组织中发现大量神经炎性斑和神经原纤维缠结。1910年,德国著名精神病学家Emil Kraepelin首次将由此种病理改变引起的临床症状与体征命名为“阿尔茨海默症”。在中国,该疾病也被称为“老年痴呆”。
对于阿尔茨海默症的研究迄今已过百年,但依然未取得突破性进展。
阿尔茨海默症的发病机制复杂,至今仍未完全破译具体机制,通常认为是老化、遗传和环境多种因素的共同结果。患者中普遍存在神经元丢失、突触障碍、胞外淀粉样蛋白β(Aβ)沉积形成淀粉样斑块、异常磷酸化Tau蛋白形成胞内神经元纤维缠结。
目前致病机制主要存在三大主流假说:
Aβ类淀粉样蛋白级联假说
Aβ沉积形成淀粉样斑块是阿尔茨海默症的主要病理特征之一。Aβ由淀粉样前体蛋白(APP)经分泌酶降解生成,在淀粉样途径中,APP被BACE剪切产生sAPPβ蛋白,sAPPβ蛋白被γ-secretase继续剪切,生成包括Aβ1-42、Aβ1-40等Aβ多肽并释放到胞外,最终聚集形成淀粉样蛋白斑,导致阿尔茨海默症发生。渤健的Aducanumab、Lecanemab和礼来的Donanemab都是靶向Aβ淀粉样蛋白的阿尔茨海默症药物,为Aβ假说提供坚定支撑。
β类淀粉样蛋白的级联反应和主要治疗方法
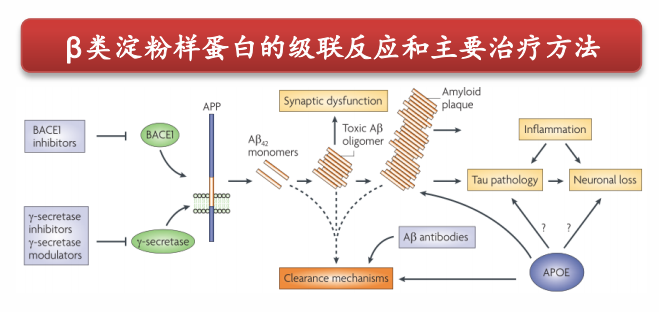
图片来源:西南证券研报
Tau蛋白异常磷酸化假说
病理状态下,胞内Tau蛋白过度或异常磷酸化使其丧失促微管组装的生物学活性,微管解聚、轴突运转出现障碍,进而引起神经细胞的凋亡,导致阿尔茨海默症发生。Tau蛋白的磷酸化与阿尔茨海默症患者病程中认知功能缺失密切相关。以Tau蛋白为靶点的阿尔茨海默症药物正在研发中,根据药渡数据,进入临床试验的有Tideglusib、Saracatinib、Nilotinib等小分子抑制剂。
Tau蛋白异常磷酸化路线和主要治疗方法
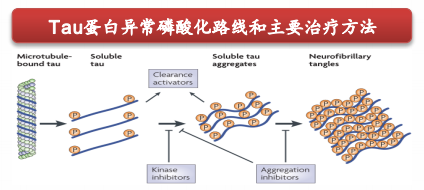
来源:西南证券研报
胆碱能假说
该假说认为阿尔茨海默症产生是由于患者脑内的神经递质存在缺陷,导致胆碱能神经元受到损伤。乙酰胆碱酯酶(AChE)和乙酰胆碱转移酶(ChAT)的活性下降是乙酰胆碱(Ach)浓度下降、胆碱能活性下降的主要原因。根据药渡数据,截至目前全球共有141种阿尔茨海默症治疗方法或药物研发管线,其中与神经递质调节以及突触功能改善上相关的药物管线有15个。
阿尔茨海默症胆碱能神经元的化学变化
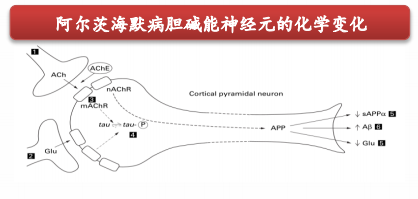
来源:西南证券研报
根据世界卫生组织《2023年世界社会报告》数据显示,2021年全球65岁以上老年人口数约为7.6亿,预计2050年全球老年人口数将增至16亿以上,人口老龄化背景下痴呆及轻度认知损害患者数将持续增加。截至2018年全球约3310万人患有阿尔茨海默症,2050年这一数字将增至2.42亿。
而在中国,据Frost&Sullivan数据,2020年中国阿尔茨海默症患者数为1250万人,预计将在2030年增至1950万人;1990年阿尔茨海默症的死亡顺位处于第10位,20年后已跃升至第5位。不论是年龄标化患病率,还是年龄标化死亡率均高于全球平均水平。
根据《中国阿尔茨海默症诊治指南》,胆碱酯酶抑制剂中的多奈哌齐、卡巴拉汀、加兰他敏是目前治疗轻中度阿尔茨海默症推荐用药,中重度患者则推荐使用谷氨酸受体拮抗剂中的美金刚。
但这些推荐用药疗效普遍不足,只能短期控制症状,难以针对明确病因机制入手延缓疾病进程。根据《阿尔茨海默病患者需求洞察报告》,在接受调查的1000名受访患者中(75.7%接受了药物治疗),其中有近半数接受药物治疗患者反馈了对现有药物治疗效果的不满意。
因此,市场急需治疗阿尔茨海默症新药。
但由于发病机制不明确,关于阿尔茨海默症的新药研发可谓屡战屡败。
根据美国药物生产与研发协会数据显示,全球累计在阿尔兹海默病上的研发投入超过6000亿美元,失败的临床药物超过300种,失败率超过99%。
2012年,强生/辉瑞的单抗药物Bapineuzumab在III期临床惨遭失败;2014年,罗氏的Gantenerumab的III期临床宣告失败;2016年,新加坡生物技术公司TauRx的LMTX宣布III期临床试验未能改善患者的认知功能宣告失败;2017年,默沙东宣布停止开发BACE抑制剂药物Verubecestat;2018年,强生宣布其终止了BACE抑制剂Atabecestat II/III期临床试验等。
直到2021年6月,美国FDA批准了Aducanumab的上市,才终结了2003年之后未有阿尔茨海默症治疗药物获批的尴尬处境。
但是,这款药物的上市却引起了很大的争议。
艰难前行
Aducanumab由渤健和卫材合作开发,是一种高亲和力、靶向-Aβ构象表位的全人IgG1单克隆抗体,可选择性与AD患者大脑中的淀粉样蛋白沉积结合,通过激活免疫系统清除大脑中沉积Aβ蛋白,进而延缓AD进程,有效支持了淀粉样蛋白假说。
然而,在2019年3月,两项临床试验ENGAGE和EMERGE在III期临床中展现相反结果:在EMERGE III期临床研究中,Aducanumab高剂量组可有效缓解患者认知下降,但在ENGAGE III期中,Aducanumab未能达到显著性差异。
不过经过曲折的探索和沟通之后,美国FDA最终还是于2021年6月附条件批准了Aducanumab上市。
上文所述的仑卡奈单抗可视为Aducanumab的升级版。
Aducanumab的临床数据

图片来源:中信建投证券
事实上,在Aducanumab与仑卡奈单抗之外,还有一款来自礼来的多奈单抗(Donanemab)更受瞩目。
John R.Sims团队在2023年阿尔茨海默病协会国际会议(AAIC)上宣布,Donanemab的III期临床试验TRAILBLAZER-ALZ 2取得成功,相关研究成功同步发表在顶级医学期刊《美国医学会杂志》(JAMA)上。
从主要研究终点来看,在低/中水平tau病理的早期阿尔茨海默症患者中,根据整合阿尔茨海默症量表(iADRS)评分,与安慰剂治疗相比,Donanemab治疗将患者疾病进展的风险降低了35.1%;在全部人群中,Donanemab治疗将患者疾病进展的风险降低了22.3%。此外,低/中水平tau病理的早期阿尔茨海默症患者中,47%的患者在接受Donanemab治疗1年后病情稳定,而接受安慰剂治疗的患者中只有29%病情稳定。
如果换算成更直观具体的数据的话,在76周时,接受Donanemab治疗的早期阿尔茨海默症患者的iADRS下降延迟了4.36个月,CDR-SB下降延迟了7.53个月。
Donanemab在2023年1月份因使用药物超12个月的患者数量不足而未获得美国FDA的加速批准,目前礼来已就Donanemab在中美都递交了上市申请,有望在2024年获批上市。
Donanemab与仑卡奈单抗的临床数据对比
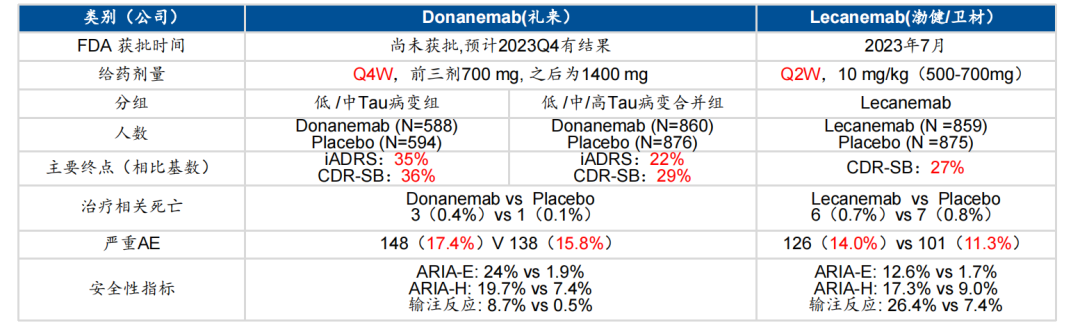
图片来源:华福证券研报
在小分子方面,Blarcamesine是“未来之星”。
Blarcamesine(ANAVEX2-73)是一款由Anavex Life Sciences开发的靶向Sigma-1的口服小分子激动剂,可有效改善神经元细胞内线粒体活化水平并改善神经炎症。
目前,Blarcamesine已完成针对阿尔茨海默症的IIa期和IIb/III期临床试验,针对帕金森病痴呆的II期概念验证研究,以及针对成年Rett综合征患者的II期和III期研究。
2023年12月欧洲EMA人用医药产品委员会(CHMP)宣布支持Blarcamesine在欧盟提交上市许可申请,因此,Blarcamesine有望成为新机制下的首 个治疗阿尔兹海默症的小分子药物。
Blarcamesine在阿尔兹海默病患者中的疗效

图片来源:中信建投证券研报
司美格鲁肽在降糖和减重领域大杀四方的时候,也不忘将触手伸向阿尔兹海默症领域。诺和诺和已开启两项全球多中心阿尔兹海默病临床,均预计纳入1840名患者,结果有望于2026年披露。
根据药渡数据统计,全球阿尔兹海默病在研新药超600款,除靶向Aβ与Tau的药物路线外,还有其他很多研发路线也在不断取得进展:Semorinemab是一种人源化的抗tau IgG4单克隆抗体,由基因泰克开发;Atuzaginstat是一款牙龈菌蛋白酶(gingipain)抑制剂,可以降低牙龈卟啉单胞菌毒性,降低细菌负荷,从而改善阿尔茨海默症进展;ATH-1017是一种小分子药物,旨在增强肝细胞 生长因子在其受体MET上的活性,由Athira Pharma开发;AGB101是一款低剂量的抗癫痫药物,使早期阿尔茨海默症患者海马回出现神经过度活跃的情况减弱,由AgeneBio开发等;Protollin是第一个被用于预防阿尔茨海默症的鼻腔疫苗等等。
国内方面,2019年11月,国家药监局有条件批准中国海洋大学、中科院上海药物所与上海绿谷研发的甘露特纳用于治疗轻度至中度阿尔茨海默症症;在研产品中,除了恒瑞医药的SHR-1707属于Aβ抑制剂外,多数国内药企研发目前主要聚焦抑制AChE和NMDA受体。
这里不得不提到通化金马的1.1类新药琥珀八氢氨吖啶片,该药物是一款AChE抑制剂。通化金马于2023年8月底召开了III期临床试验揭盲预备会,宣布正式完成盲态数据审核,通化金马的股价也由此开启了超过200%的涨幅。
国内治疗阿尔茨海默症的主要在研小分子药物研发进展
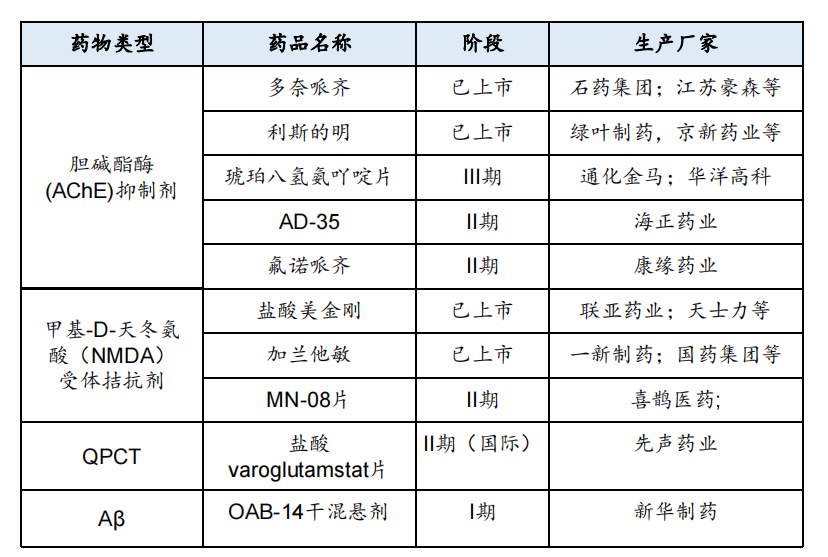
图片来源:华福证券研报
结语
尽管在研发方面,各种路线都在十分努力地证明自己,但从临床试验数据中我们也看到,这些都不是治疗阿尔兹海默症真正有效的药物。只因为发病机制没有搞清楚,目前所做的诸多努力仅仅只能够延缓阿尔兹海默症的进展,而不是彻底治愈。不过不必太过沮丧,在科学家的倾情努力下,曙光似乎就在眼前。后续发展如何,药渡还将持续关注。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57