2024年1月15日,据CDE官网公布,百吉生物第三条全球独家首 创产品管线BRL03注射液新药临床试验获批,用于治疗多种晚期实体瘤,包括肺癌和胃癌等。
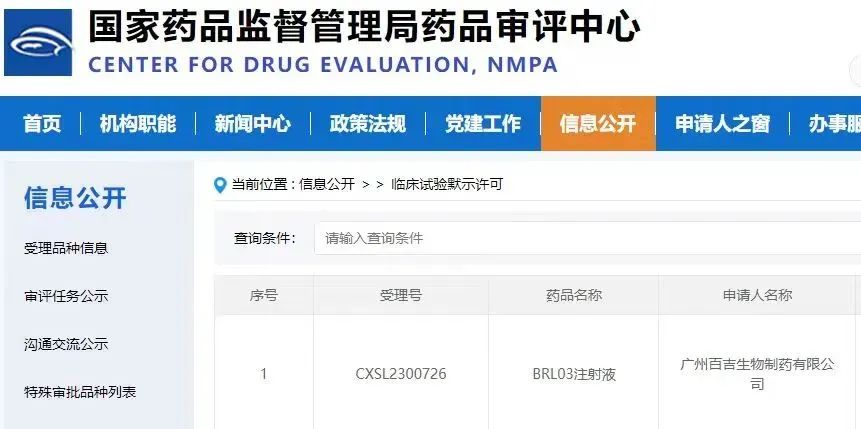
图片来源:CDE官网
去年9月9日,美国FDA批准了BRL03的I/II期临床试验申请,BRL03注射液的NMPA IND申请获得批准,标志着百吉生物已正式获得第7个全球首 创产品的IND临床批件。作为百吉生物自主研发的首 款进入临床的TCR-T产品,IIT研究显示BRL03注射液在实体瘤治疗中具有良好的安全性和初步疗效。
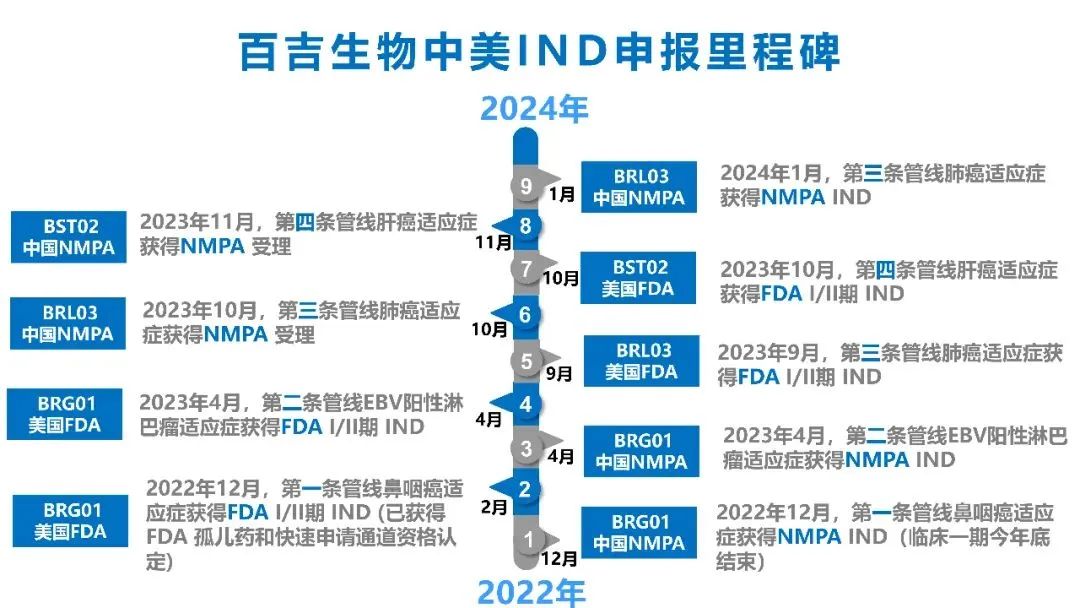
图片来源:百吉生物官微
此外,百吉生物的鼻咽癌适应症和EBV阳性淋巴瘤适应症两条管线已进入全球一期临床试验阶段,其中鼻咽癌适应症已完成一期临床入组。
百吉生物的自主创新技术平台IDENTIFIER®为抗原、抗体和TCR的发现和鉴定提供了强大的支持。
利用来自上千个体的TCR和肿瘤蛋白组数据库,百吉生物可以在两周内筛选和优化针对不同治疗需求的合适开发资产。通过该平台,百吉生物筛选出具有广泛受众群体,兼具高特异性和亲和力的、针对多种实体肿瘤的TCR。
此外,基于另一自研的MSE-T平台,BRL03还具有额外的功能模块组件,使T细胞在实体肿瘤微环境中不易耗竭,从而更持久地发挥抑瘤效力。
百吉生物将继续致力于满足患者未被满足的临床需求,为全球癌症患者提供最 佳的治疗选择。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57