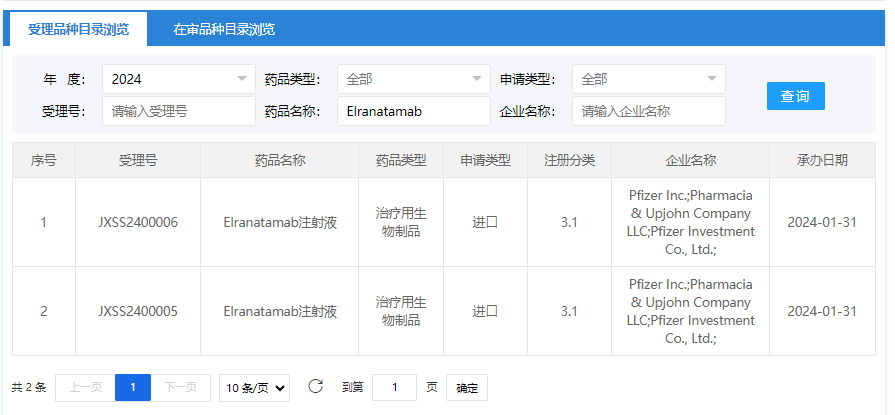
2024年1月31日,CDE网站显示,辉瑞的CD3/BCMA双抗Elranatamab(Elrexfio)在国内申报上市,用于治疗既往接受过治疗的复发或难治性多发性骨髓瘤(R/R MM)。
药渡数据检索可知,2023年8月Elranatamab获FDA加速批准上市,用于治疗既往接受过至少四线治疗的复发或难治性多发性骨髓瘤(R/R MM)成人患者。
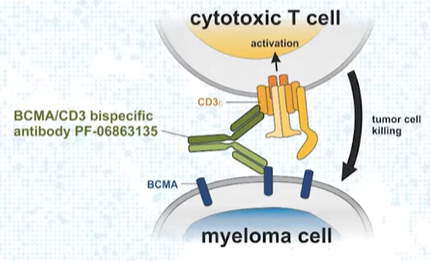
作用机制
Elranatamab是一种人源化双特异性抗体,通过同时靶向骨髓瘤细胞表面的BCMA和T细胞表面的CD3,直接激活T细胞诱导产生细胞毒作用杀伤骨髓瘤细胞。
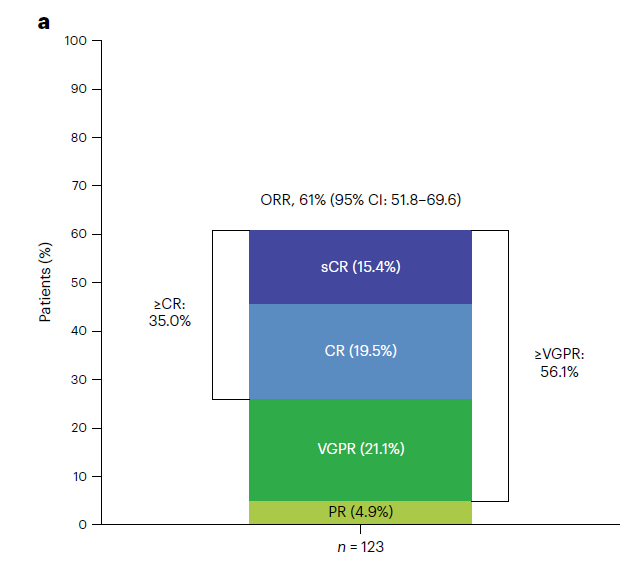
主要临床数据
MagnetisMM-3是一项正在进行的多中心、开放标签、单臂、2期临床研究,旨在评估Elranatamab在成人患者中的疗效和安全性。患者既往接受过至少一种蛋白酶体抑制剂、一种免疫调节剂和一种抗CD38抗体,经末线抗骨髓瘤方案后复发或难治的患者。其中队列A中的受试者既往不得接受过靶向BCMA治疗,而队列B的受试者为既往接受过BCMA治疗。其中MagnetisMM-3队列A的积极数据已在《Nature Medicine》发表。
临床结果表明队列A共入组123例患者中位随访14.7个月后达到主要终点,61.0%的患者经BICR证实达到客观缓解。35.0%的患者达到≥CR,56.1%的患者达到≥非常好的部分缓解 (VGPR)。
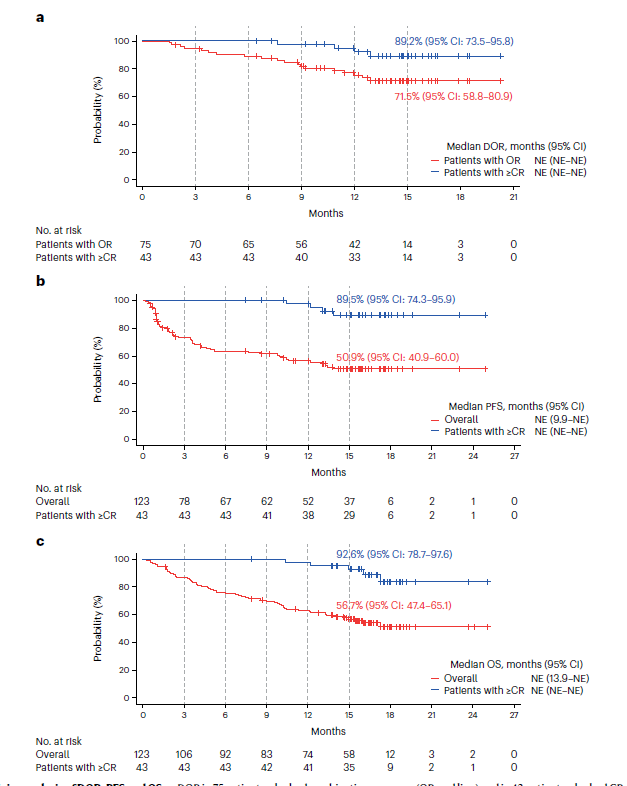
中位DOR暂未达到,56例(74.7%)患者在分析时删失。Kaplan-Meier分析显示,总体人群≥CR患者15个月DOR率为89.2%,整体患者为71.5%(下图 A)。中位 PFS 暂未达到,其中70例(56.9%)患者在数据截止时删失,15个月时PFS率为50.9%(下图B),15个月时中位OS率为56.7%(下图C)。对于≥CR的患者,15个月时PFS和OS率分别为89.5%和92.6%。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57