靶向蛋白降解(Targeted protein degradation, TPD)在过去二十年中作为一种主要的新型药物模式已被广泛用于多种蛋白,为癌症、炎症等疾病治疗提供了一种潜在的有前途的治疗策略。
其中,蛋白降解靶向嵌合体(Proteolysis targeting chimeras,PROTAC)作为一种有潜力的靶向蛋白降解技术,它是具有E3泛素连接酶招募者与感兴趣蛋白(POI)配体连接的异双功能小分子,通过诱导E3泛素连接酶与POI靠近实现靶蛋白降解。PROTAC分子具有高效、低耐药性等特点,同时能靶向“不可成药”蛋白,其应用前景十分广泛。
之后,受PROTAC的启发,去泛素化酶靶向嵌合体(deubiquitinase-targeting chimeras,DUBTACs)成功问世,用于靶向蛋白质稳定(targeted protein stabilization,TPS)。接下来,我们就来重点介绍一下靶向蛋白降解技术和靶向蛋白稳定技术(图1)。
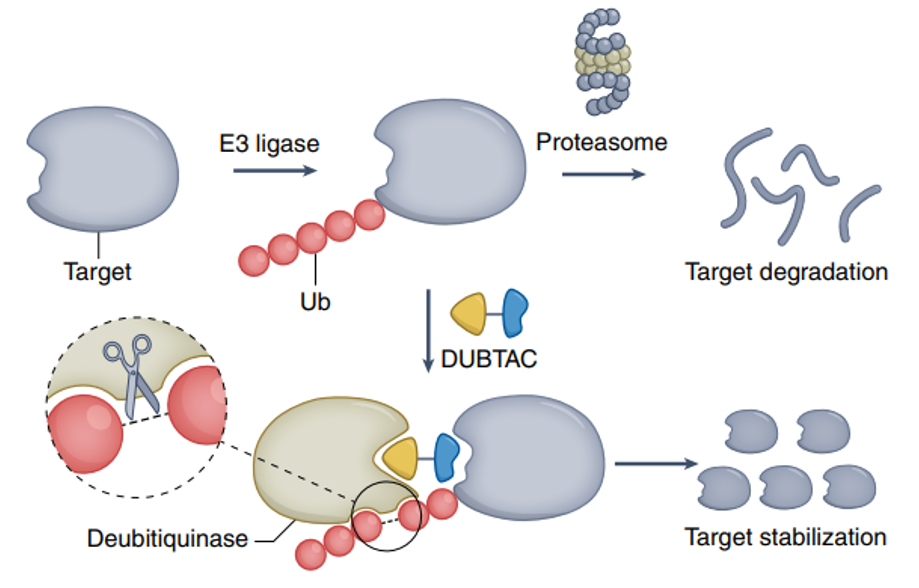
图1. 靶向蛋白降解技术和靶向蛋白稳定技术作用机制示意图
01
细胞内靶向蛋白降解(iTPD)
近年来,细胞内靶向蛋白降解(intracellular targeted protein degradation,iTPD)已成为小分子药物新的重要模式(图2)。在这里,构建了异双功能小分子,招募感兴趣的药物靶蛋白(POI)和E3连接酶,用于蛋白酶体降解。目前,已经开发出两类这样的分子。
PROTAC
蛋白质水解靶向嵌合体(Proteolysis-targeting chimeras, PROTACs)由Crews和Deshaies团队首 创,是由一个linker连接的大的特异性小分子;一部分与POI结合,另一部分与E3连接酶结合,使POI泛素化,被细胞质中的蛋白酶体降解。
分子胶
第二类被称为分子胶,是利用小分子化合物通过非共价作用与病理蛋白结合,形成大的稳定复合物,阻止病理蛋白的功能。在这种情况下,分子胶增强了E3连接酶和POI之间的相互作用,导致其泛素化和降解。相关文章回顾:继PROTAC之后的新型蛋白降解剂:分子胶。
由于PROTAC与E3连接酶和POI具有独立的结合位点,因此比分子胶更容易设计。然而,它们通常是大分子,开发起来很有挑战性,而基于lipinski五规则等指导原则,分子胶通常更小,更像药物。值得注意的是,雷帕霉素、FK506和环孢菌素等天然产物胶都是较大的分子,但仍可口服生物利用,它们代表了临床使用的分子胶的很大一部分。
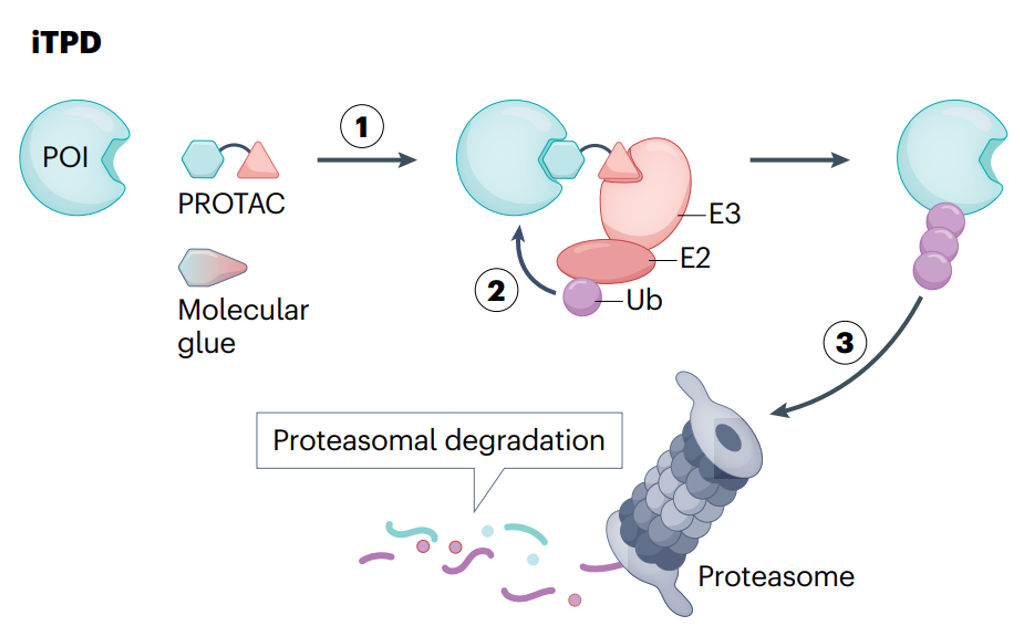
图2. 细胞内靶向蛋白降解(iTPD)示意图
与传统的基于“占位驱动”的小分子抑制剂相比,iTPD具有显著的优势。
首先,PROTACs发挥作用取决于靶蛋白和E3连接酶的空间邻近,属于“事件驱动”的作用模式。PROTAC具有催化特性,只需提供与靶蛋白的结合活性,无须直接占据靶蛋白的活性口袋、有助于攻克小分子难以成药的靶点。
其次,PROTAC发挥作用时直接将靶蛋白降解,克服了传统小分子药物容易导致的靶蛋白过表达及突变等耐药性问题。
第三,由于PROTAC的生效机制类似催化反应,因此只需要极低剂量即可发挥效用,较低的给药浓度使PROTAC药物的安全性较高。
目前,已有ARV-110、ARV-471、KT-474和DT2216等多个PROTAC分子进入临床试验阶段。与PROTAC相比,分子胶有更小的分子量(通常小于600Da)、更好的膜通透性和成药性,但分子胶并不等同于“去掉连接子的PROTAC”。分子胶通过诱导或稳定E3连接酶与靶蛋白之间的“蛋白-蛋白相互作用”(protein?protein interaction,PPI),介导靶蛋白泛素化和随后的蛋白酶体降解。
分子胶的发现多是偶然的,最 具代表性的是IKZF1/3降解剂沙利度胺、来那度胺和泊马度胺。在此基础上,研究人员通过合理的结构优化得到了CC-92480(IKZF1/3降解剂)和CC-90009(GSPT1降解剂)等进入临床试验阶段的分子胶(图3)。
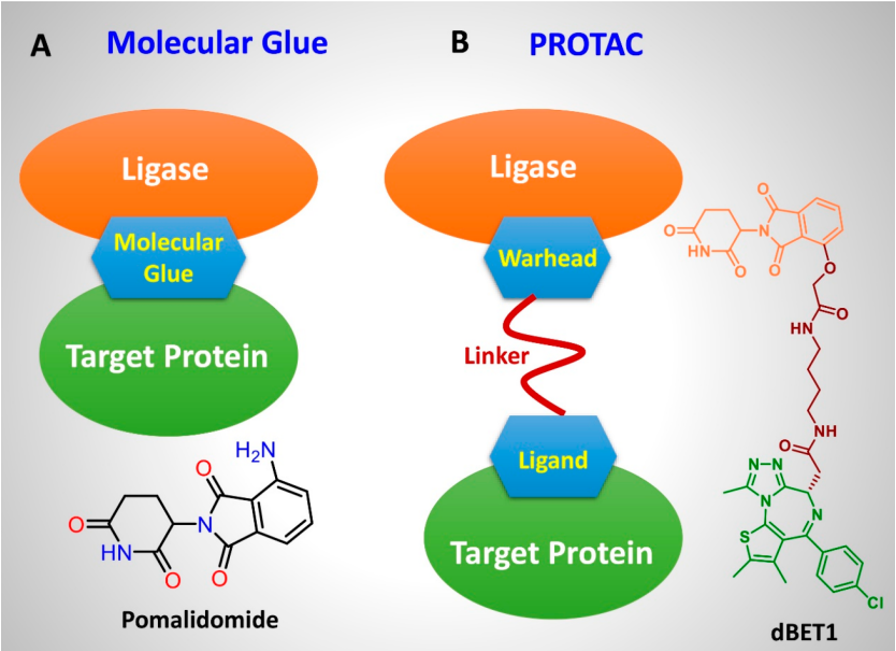
图3. 分子胶与PROTAC的作用方式及结构特点
02
细胞外靶向蛋白降解(eTPD)
细胞外蛋白质组由分泌蛋白和膜结合蛋白组成,涵盖了生长因子、细胞因子、激素、酶和受体等多种蛋白质,它们在细胞信号传导、免疫反应、组织修复和新陈代谢中扮演重要角色。由于许多疾病与细胞外蛋白的失调有关,因此,细胞外蛋白质被认为是药物研发中的一类重要治疗靶点。
近年来,细胞外靶向蛋白降解(extracellular targeted protein degradation,eTPD)技术的出现,为研究人员提供了一种全新的模式来调节细胞外蛋白质组。不同于传统基于“占位驱动”的药物,eTPD技术运用双特异性生物制剂或小分子招募细胞外蛋白,将细胞外蛋白质运送到溶酶体进行选择性降解,这种独特的作用方式拓展了可治疗的靶点范围,为治疗多种疾病开辟了新的可能性(图4)。
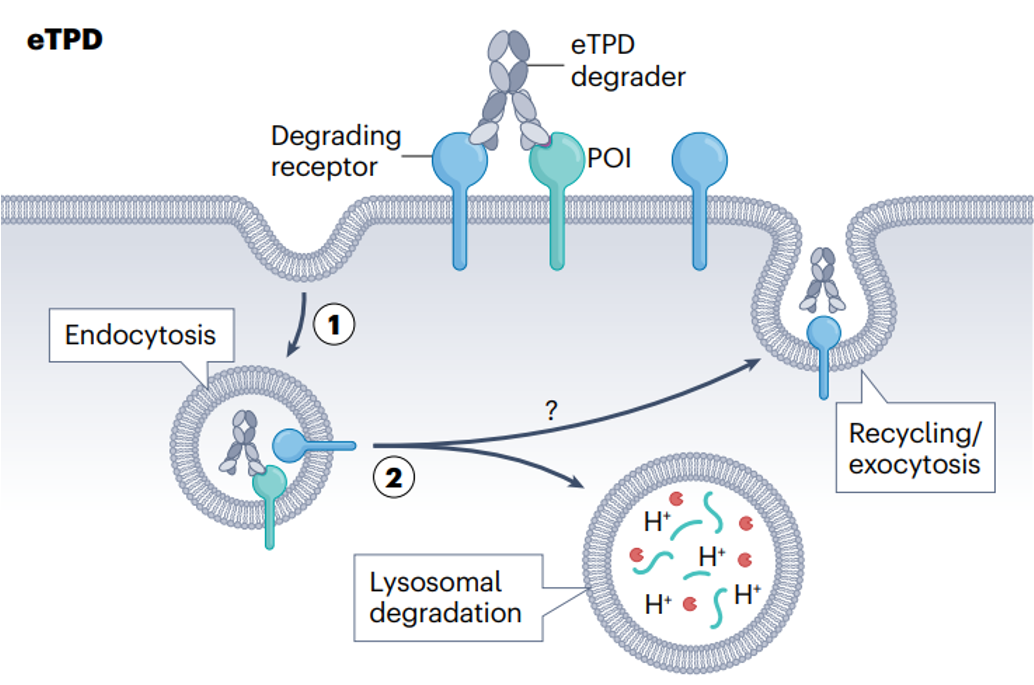
图4. 细胞外靶向蛋白降解(eTPD)示意图
目前,降解细胞外蛋白质主要有六种不同的方法策略,分别是降解可溶性POI的清除抗体eTPD、基于聚糖的循环受体eTPD、基于跨膜E3连接酶靶向膜蛋白的eTPD、基于细胞因子靶向膜蛋白的eTPD、基于整合素的eTPD、从内部降解膜蛋白的eTPD。
NO.1
降解可溶性POI的清除抗体eTPD
降解可溶性POI的清除抗体eTPD是“清除抗体”(sweeping antibodies)分子经过工程改造,增强了它们与Fc回收受体、新生儿Fc受体(FcRn)或FcγRIIb的结合能力。可以使工程化抗体通过FcRn,以pH可切换的方式将POI递送到酸性内体,酸性内体释放POI进行溶酶体降解。
Tocilizumab(Tcz)是一种被批准用于治疗类风湿性关节炎的人源化抗体。pH可切换的Tocilizumab于2020年被批准用于治疗视神经脊髓炎谱系障碍,这代表了eTPD中第一个被批准的抗体。
NO.2
基于聚糖的循环受体eTPD
基于聚糖靶向的再循环受体,如阳离子非依赖性甘露糖6-磷酸受体(CI-M6PR)可以促进膜和可溶性POI的溶酶体降解。其中,溶酶体靶向嵌合体(LYTAC)就是利用LYTAC–POI复合物与CI-M6PR结合后被内化,导致POI在溶酶体中降解。
NO.3
基于跨膜E3连接酶靶向膜蛋白的eTPD
基于跨膜E3连接酶靶向膜蛋白的eTPD是利用靶向含有跨膜结构域的E3连接酶家族成员和POI的双特异性抗体降解靶蛋白,被称为AbTACs或PROTAB。
NO.4
基于细胞因子靶向膜蛋白的eTPD
基于细胞因子靶向膜蛋白的eTPD,如细胞因子受体靶向嵌合体(KineTAC)也是一种双特异性抗体,KineTAC一端结合细胞因子或生长因子,而另一端结合POI。从而实现膜结合型和可溶性蛋白的降解。
NO.5
基于整合素的eTPD
利用整合素促进的溶酶体降解技术是使用双特异性抗体的一端结合整合素,而另一端结合POI,从而将POI引导至溶酶体进行降解,同时利用整合素的循环能力来增强目标定位和效率。
NO.6
从内部降解膜蛋白的eTPD
从内部降解膜蛋白的eTPD则涉及PROTACs技术,这类分子一部分用于结合受体酪氨酸激酶的细胞内激酶结构域,而另一部分与细胞质中的E3连接酶结合,通过泛素蛋白酶体途径进行降解。PROTACs技术为靶向细胞内蛋白质提供了一种高效的降解策略(图5)。
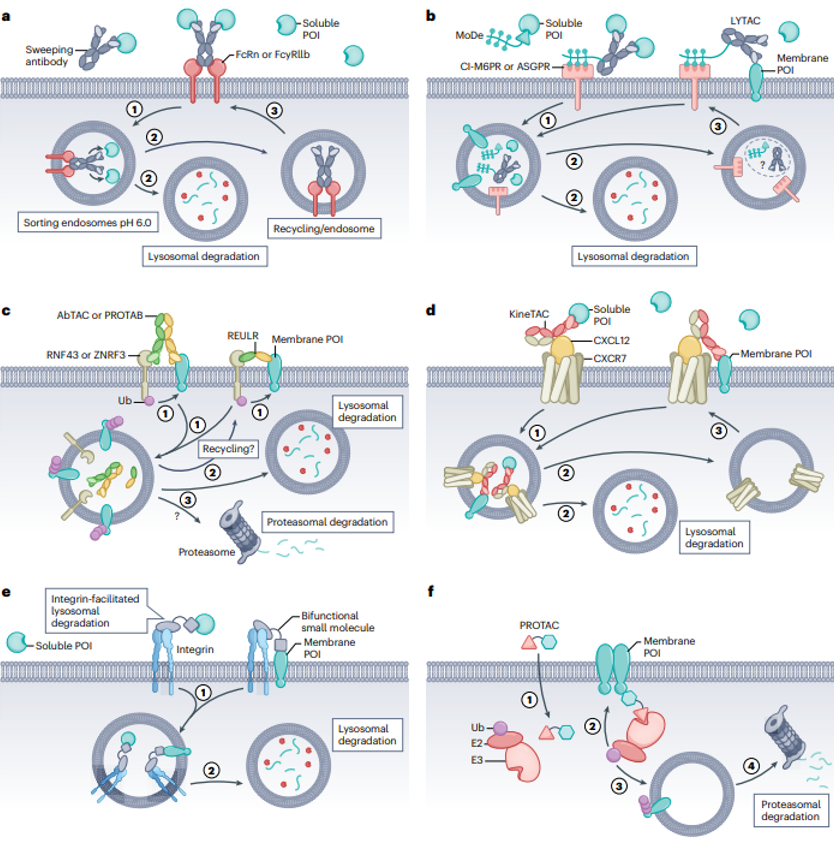
图5. 降解细胞外蛋白质的六种不同方法策略
03
靶向蛋白稳定(TPS)
2022年初,美国加州大学伯克利分校的Daniel Nomura教授团队与诺华生物医学研究所(NIBR)的研究人员合作,开发了一种新的治疗模式,它被称为去泛素化酶靶向嵌合体(Deubiquitinase Targeting Chimera ,DUBTACs)。
DUBTACs是一种异双功能小分子,由一个与蛋白质靶向配体和去泛素化酶招募者组成,DUBTACs发挥作用的大致过程为:DUBTACs一端结合靶蛋白(POI),一端结合去泛素化酶,诱导靶蛋白与去泛素化酶的靠近,从而去除泛素链,以阻止蛋白酶体介导的靶蛋白的降解,达到稳定以泛素依赖方式降解的特定蛋白质的水平(图6)。
在这项研究中,研究人员利用DUBTACs,提高了一种名为CFTR的氯离子通道蛋白突变体的稳定性。通常这种突变体的降解,会导致严重的囊性纤维化(CF)疾病。研究结果显示,靶向CFTR的DUBTACs,能够恢复从囊性纤维化患者体内获得的原代人类支气管上皮细胞的氯离子通道功能。研究结果同时显示,DUBTACs可以被用于治疗癌症。他们开发了一款能够稳定肿瘤抑制蛋白WEE1激酶的DUBTAC。WEE1激酶在很多肿瘤中被主动降解,从而促进癌细胞的增生,稳定癌细胞中WEE1激酶的水平可能终止肿瘤的生长。
不久后,美国哈佛医学院的魏文毅教授团队和西奈山伊坎医学院的金坚教授团队,使用EN523招募去泛化素酶OTUB1进一步开发了能够稳定抑癌蛋白的首 个TF-DUBTAC药物平台,旨在通过稳定抑癌转录因子(Transcription Factor,TF)实现对肿瘤的治疗。
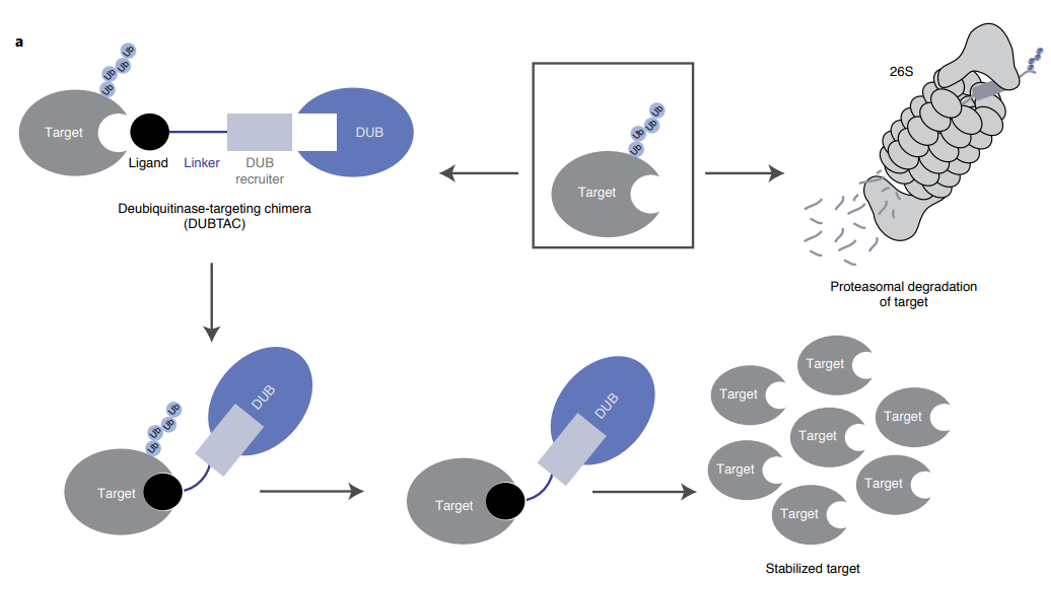
图6. DUBTACs作用示意图
总体来说,DUBTACs作为一种较新的疗法,进行的研究和开发还相对较少,但也已经在某些特定的案例中展现出了治疗潜力,TPD和TPS的兴起代表了药物发现领域的一次重大突破。鉴于其在癌症治疗、免疫调节、神经退行性疾病以及传染病等领域的应用潜力,TPD和TPS正显现出作为一种多功能性治疗策略的广泛意义。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57