2024年2月23日,从中国国家药监局(NMPA)官网公示武田公司的注射用替度格鲁肽(商品名瑞唯抒®)已正式获批上市,用于短肠综合征成人和1岁及以上儿童患者。
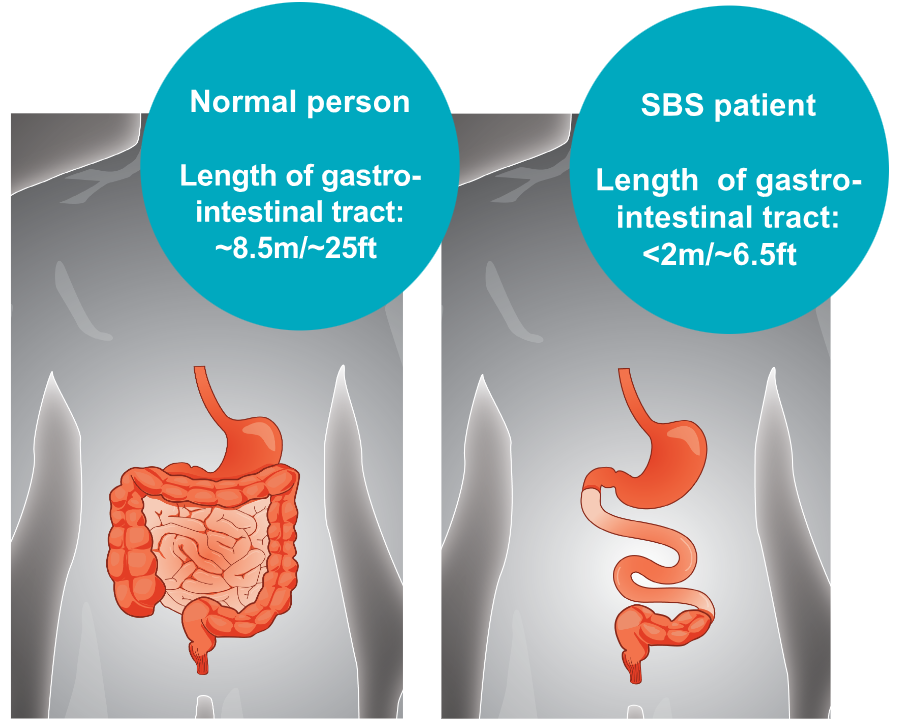
短肠综合征(Short bowel syndrome,简称SBS)是由于疾病和(或)手术切除导致的肠道长度严重缩短、肠道面积显著减少的一种临床综合征,主要症状是腹泻,其可导致脱水,营养不良和体重减轻。
临床疗效
本次获批是基于针对成人和儿童短肠综合征患者的全球及日本3期临床研究结果。
1)成人短肠综合征
患者关键3期研究STEPS研究(CL0600-020)共入组86例依赖肠外营养支持(PN)的患者,给药24周。研究结果表明,治疗24周后,63%的患者PN需求量下降≥20%,应答率相比安慰剂组(30%的患者)显著增高。另一项长期开放性扩展研究STEPS-2(CL0600-021)共纳入88例短肠综合征伴肠功能衰竭(SBS-IF)患者,研究结果显示:治疗30个月后,93%的患者PN需求量下降≥20%,33%的患者完全脱离PN。最常见不良反应是腹痛和腹胀、呼吸道感染、恶心等,多为轻度或中度。
2)儿童短肠综合征
患者关键3期研究(TED-C14-006),给药24周、纳入59名1至17岁依赖PN的儿童患者,主要终点分析数据显示:治疗24周后,69%的儿童患者PN需求量下降≥20%,12%的儿童患者完全脱离PN。安全性特征儿童与成人相似。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57