创新药“一哥”成绩单出炉,引得市场纷纷注目。
作为目前国内药企中,国际化最成功的Biotech,百济神州的打法战略有太多值得学习的地方。当然,这种打法战略不是人人都能学得来,也不是总那么成功。在过去的2023年,百济神州有悲有喜,遭遇了一些挫折,颇为惋惜,但喜事仍旧洋溢:泽布替尼成为中国制药史上第一个全球收入突破“十亿美元”的药物、替雷利珠单抗国际化战略为国内PD-1的出海提供了教科书般示范......
首破“十亿美元”
2月26日,百济神州公布2023业绩快报,全年总收入达24.59亿美元,同比增长74%;得益于对经营费用的严格管理,按美国公认会计原则(GAAP)计,2023年,经调整后经营亏损7.52亿美元,减少了47%。
其中,全年产品收入22亿美元,增长69.2%:百悦泽和百泽安全球销售额分别为13亿美元、5.37亿美元,安进公司授权产品全年销售额为1.88亿美元。
2023年百济神州营收数据
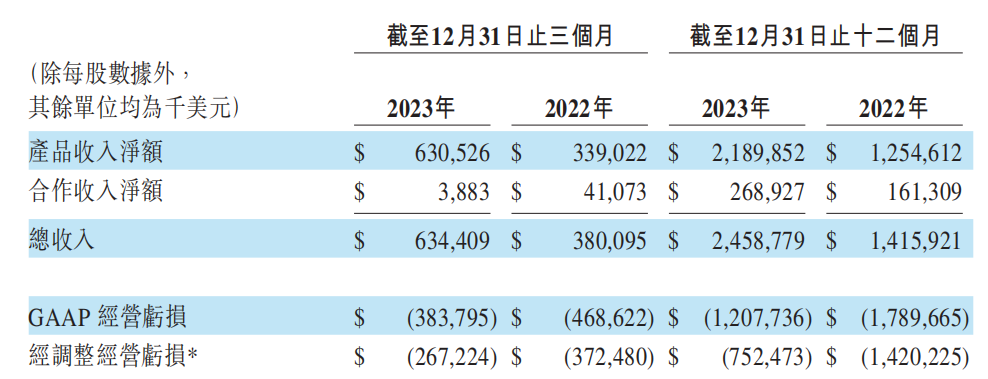
图片来源:业绩快报
单靠两个产品就能创下超百亿人民币营收,这商业化能力在国内无人能比。
2023年,BTK抑制剂百悦泽(泽布替尼)全球销售额总计91.38亿元,同比增长138.7%,在血液肿瘤领域进一步巩固领导地位。目前,百悦泽在中国获批的5项适应症已全部纳入国家医保目录。
在全球市场,百悦泽同样是大杀四方,目前已在包括美国、中国、欧盟、英国、加拿大、澳大利亚、韩国和瑞士在内的超过65个市场获批多项适应症。“头对头”硬刚伊布替尼的临床试验中,百悦泽在PFS和总缓解率(ORR)方面对比伊布替尼均展现了优效性,且心脏功能相关的不良事件发生率更低;在治疗R/R CLL/SLL成人患者中持续展示出PFS获益,且心血管事件发生率持续较低,中位随访39个月的积极数据已于2023年12月召开的ASH年会上进行展示。
2023年,百悦泽的进展包括获得美国FDA对更新说明书的批准,纳入在3期ALPINE试验中治疗R/R CLL/SLL成人患者取得的PFS优效性结果;获得欧盟委员会和加拿大卫生部批准,联合奥妥珠单抗用于治疗既往接受过至少两线系统性治疗的R/R FL成人患者;新增4个市场,获得治疗R/R和初治(TN)CLL适应症注册批准。
预计百悦泽将于2024年3月和6月分别获得美国FDA和中国国家药监局批准用于治疗既往接受过至少两线系统性治疗的R/R FL成人患者。

PD-1百泽安(替雷利珠单抗)虽然遭遇了一些挫折,但依然取得非常辉煌的成绩。2023年,百泽安的销售额总计38.06亿元,同比增长33.1%。
目前,百泽安已在中国已获批12项适应症,其中11项适应症已纳入国家医保目录,是目前国内适应症最广泛的PD-1;已在欧盟和英国取得批准用于二线治疗食管鳞状细胞癌(ESCC)成人患者。因受到一些挫折,百济神州已重获百泽安开发、生产和商业化的全球权利,目前正在接受美国和欧洲等10个国家和地区监管机构审评。
国家药监局正在审评百泽安用于局部晚期不可切除或转移性胃或胃食管结合部腺癌(GC/GEJC)患者一线治疗(预计将于2024年第二季度获批)、广泛期小细胞肺癌(ES-SCLC)患者一线治疗(预计将于2024年第三季度获批)以及用于可切除非小细胞肺癌(NSCLC)患者的围术期治疗的三项新增适应症上市许可申请。
在美国,FDA正在审评百泽安用于一线治疗ESCC患者的上市许可申请,根据
《处方药申报者付费法案》(PDUFA),预计FDA将于2024年7月对该项申请做出决定;正在审评百泽安用于二线治疗ESCC的新药上市许可申请,预计FDA将于2024年上半年批准此项申请。
在欧洲,欧洲药品管理局(EMA)正在审评百泽安联合化疗用于一线和单药用于二线治疗转移性NSCLC的三项新增适应症上市许可申请,预计EMA将于2024年上半年批准此申请;正在审评百泽安用于一线治疗ESCC成人患者的新增适应症上市许可申请。
在收入端不断攻城掠地的时候,作为国内最能烧钱的制药公司,百济神州的财务状况改善得如何?
进展喜人
根据业绩快报,2023年全年,按GAAP计算,百济神州净亏损较去年同期有所改善,主要由于经营亏损减少,并因BMS仲裁和解获得3.629亿美元的非经营收入。
但是研发费用依旧呈增长趋势,2023年全年,GAAP和经调整研发费用均同比增长,其中GAAP口径下研发费用支出17.79亿美元,增长8%。主要是由于对新技术平台和药物模式的投入,正在进行中的授权引入候选药物研发相关的预付款分别为3180万美元和4680万美元,上年同期分别为4870万美元和6870万美元。
2023年和2022年全年的经营费用分别汇总
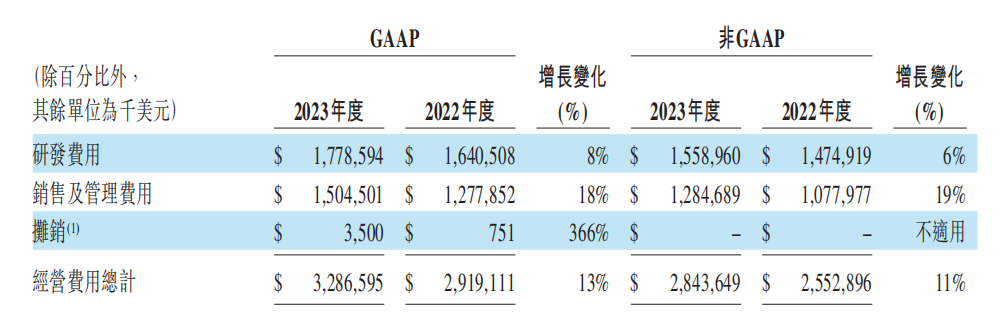
图片来源:业绩快报
后续管线中,百济神州在研药物管线超过50款,覆盖多种技术平台和药物模式,包括单抗、双抗/多抗、ADC、细胞治疗、mRNA等。2023年,百济神州共推动5款新分子实体进入临床,包括潜在“同类最 佳”BCL-2抑制剂、CDK4抑制剂。
BCL2抑制剂Sonrotoclax具备“同类最 佳”潜力,目前已启动了4项全球注册性试验。2023年的研发进展包括获得美国FDA“孤儿药”资格认定,用于治疗多发性骨髓瘤(MM)、华氏巨球蛋白血症(WM)、急性髓系白血病(AML)和套细胞淋巴瘤(MCL);在与百悦泽联合用于一线治疗CLL患者的全球关键性试验中,入组首例患者;与百悦泽联用,展示出良好的安全性和耐受性,且对治疗TN CLL有深度和持久的疗效;展示出令人鼓舞的数据,有望成为首 款在携带t(11,14)的MM适应症中获批的BCL-2抑制剂;在治疗R/R MZL中,展示出良好的单药活性等。
在火爆的ADC赛道方面,目前百济神州已布局了从Zymeworks引进的HER2双抗ADC ZW49,从映恩生物获得一款在研、临床前ADC药物B7H4-ADC的全球开发和商业化权利,还正在开发自有ADC技术,包括两款自研产品B7H3-ADC、CEA-ADC。目前B7H3-ADC、CEA-ADC、B7H4-ADC均在临床前阶段,即将进入临床开发阶段。
百济神州研发管线
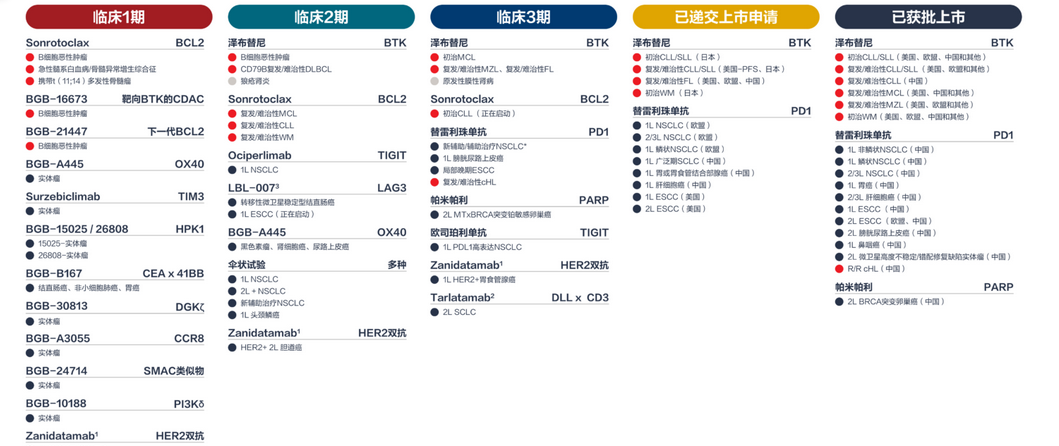
图片来源:官网
生产运营方面,百济神州的建设如火如荼。其中,位于美国新泽西州霍普韦尔西普林斯顿创新园区的旗舰级生物药生产基地和临床研发中心即将完工,预计将于2024年7月投入运营;位于中国苏州的新建小分子创新药物产业化基地已完工;位于中国广州的世界一流生物药生产基地总产能已达6.5万升,抗体偶联药物(ADC)生产设施和全新生物药临床生产大楼均已完工。
结语
肉眼可见,这艘巨轮正在以过去中国制药史上未曾出现过的模式和速度前进,但对这样的巨无霸的发展,市场也一直存在不同的声音,主要在其财务负担方面。2023年,百济神州拥有的现金及现金等价物为31.89亿美元,同比减少了13.51亿美元,如何平衡巨额研发费用和现金储备的天平,是百济需要解决的问题,希望百济早日破局,成功跻身MNC。后续发展如何,药渡还将持续关注。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57