2月27日,再鼎医药有限公司公布了2023年全年财务业绩。
财报显示,2023年再鼎医药全年产品收入为2.667亿美元, 2022年同期为2.127亿美元,同比增长25%, 按固定汇率计算同比增长31%。产品收入增加主要是由于销量增加、卫伟迦的上市以及COVID-19疫情负面影响的降低,但也部分被向经销商提供的销售返利增加和中国2023年下半年的医药政策环境调整的影响抵销。(由于有更多的产品被新纳入或成功续约NRDL,向经销商提供的销售返利由2022年的530万美元增至2023年的1,300万美元。)
此外,据财报显示,2023年再鼎医药亏损净额为3.346亿美元,每股普通股亏损为0.35美元(每份美国存托股份(ADS)亏损为3.46美元),2022年同期亏损净额为4.433亿美元,每股普通股亏损为0.46美元(每份ADS亏损为4.63美元)。亏损净额减少主要是由于产品收入增长速度高于经营费用的增长,利息收益的增加,以及汇兑损失的减少。
5大产品产业化
明星产品则乐销售1.688亿美元
据再鼎医药官网显示,再鼎医药目前已有5个产品实现商业化,50+项目临床试验进行中或计划中,涉及肿瘤学、传染病、神经科学、自身免疫失调4大治疗领域。
再鼎医药研发管线

图片来源:再鼎医药官网
则乐
2023年则乐销售收入为1.688亿美元,2022年同期为1.452亿美元,同比增长16%。
销售增长是由于卵巢癌一线维持治疗院内销售额的增加和治疗持续时间的延长,部分被NRDL续约相关的销售返利抵销。
在被纳入NRDL后的第三年,则乐继续保持中国卵巢癌领域PARP抑制剂院内销售领军者地位。
则乐用于成人铂敏感复发卵巢癌和一线卵巢癌维持治疗适应证成功续约NRDL,并于2024年1月1日生效。
卫伟迦®
2023年销售收入为1,000万美元, 2022年未产生收入。
2023年9月,卫伟迦于中国内地成功上市,用于治疗乙酰胆碱(AChR)抗体阳性的成人gMG患者。
据估算从上市到截至第四季度末已治疗近1,000名患者。
卫伟迦被纳入NRDL,用于治疗gMG,于2024年1月1日生效。
得益于医生和患者的积极反馈以及卫伟迦加速进院,更多患者的可及性得到提高。据估算仅2024年1月就有近1,000名患者接受卫伟迦治疗。
预计卫伟迦2024年销售收入将超过7,000万美元。
爱普盾®
2023年销售收入为4,700万美元,相较2022年同期的4,730万美元基本持平。
补充保险计划覆盖范围持续扩大,部分被医药政策环境调整抵销。
擎乐®
2023年销售收入为1,920万美元,2022年同期为1,500万美元,同比增长29%。
销售收入的增长得益于擎乐于2023年第一季度纳入NRDL,用于晚期胃肠道间质瘤(GIST)的四线治疗,部分被纳入NRDL相关的销售返利抵销。
纽再乐®
2023年销售收入为2,170万美元,2022年同期为520万美元,同比增长316%。
2023年第一季度,纽再乐(静脉注射剂型)用于治疗成人社区获得性细菌性肺炎(CABP)和急性细菌性皮肤和皮肤结构感染(ABSSSI)首次纳入NRDL,推动了销售收入的增长。
治疗上述适应证的纽再乐口服剂型已被纳入NRDL,自2024年1月1日起生效,预计这将进一步增加患者的可及性。
研发投入2.659亿美元
50+临床实验在研
此外,据再鼎医药财报显示,2023年再鼎医药的研发(R&D)开支为2.659亿美元,2022年同期为2.864亿美元。研发支出的降低主要原因为与许可及合作协议有关的预付款和里程碑付款减少,部分被研发人员工资和工资相关开支的增加抵销。
另外据再鼎医药官网显示,目前再鼎医药仍有50+临床实验在研。
再鼎医药正在进行的临床研究
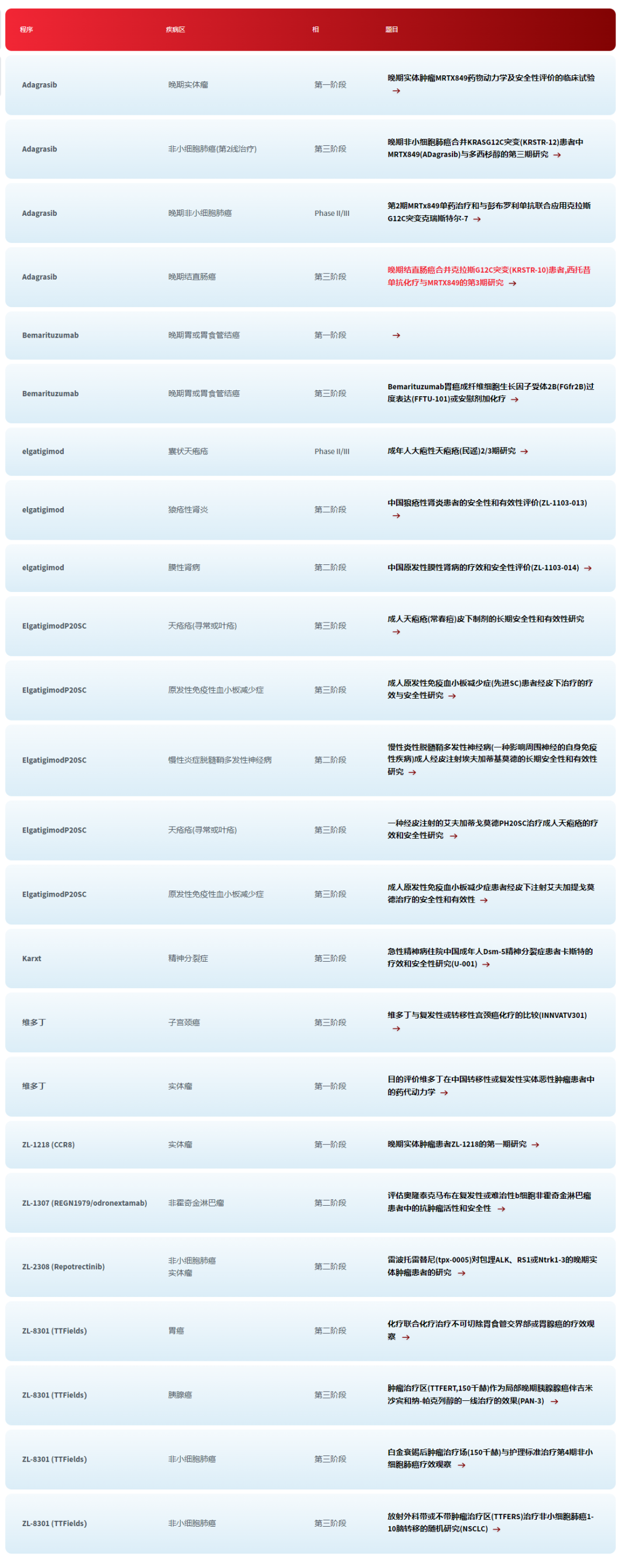
图片来源:再鼎医药官网
且据财报显示,2024年多项研究将取得里程碑进展。
肿瘤领域
肿瘤电场治疗
再鼎医药将向NMPA提交肿瘤电场治疗用于铂类化疗治疗中或治疗后出现进展的二线及以上NSCLC患者的MAA。
再鼎医药合作伙伴Novocure将于2024年第一季度公布非小细胞肺癌脑转移3期临床研究METIS的主要数据。再鼎医药正在大中华区参与这项研究。
Novocure将于2024年第四季度公布肿瘤电场治疗用于局部晚期胰腺癌的3期临床研究PANOVA-3的主要数据。再鼎医药正在大中华区参与这项研究。
瑞普替尼(ROS1/TRK)
瑞普替尼用于局部晚期或转移性ROS1阳性NSCLC的新药上市申请,有望于2024年获得NMPA批准。
Adagrasib(KRASG12C)
再鼎医药将向NMPA提交adagrasib用于二线及以上KRASG12C突变NSCLC的新药上市申请。
再鼎医药将于2024年下半年在大中华区参加全球3期研究KRYSTAL-7,评估adagrasib一线治疗肿瘤比例评分(TPS)≥50%的KRASG12C突变非小细胞肺癌
再鼎医药合作伙伴Mirati(BMS的子公司)将公布adagrasib用于二线及以上KRASG12C突变NSCLC的全球确证性3期临床研究KRYSTAL-12的临床数据更新。再鼎医药正在大中华区参与这项研究。
Mirati将公布adagrasib用于TPS<50%的一线KRASG12C突变NSCLC的全球2期研究KRYSTAL-17的临床数据更新。
Tisotumab Vedotin(组织因子 ADC)
再鼎医药将向NMPA提交用于二线及以上宫颈癌的NDA。
自身免疫疾病、感染性疾病
和中枢神经系统疾病领域
艾加莫德(FcRn)
艾加莫德皮下注射剂型用于gMG的sBLA有望获NMPA批准。
再鼎医药将于2024年上半年向NMPA提交艾加莫德皮下注射剂型用于CIDP的sBLA。
再鼎医药合作伙伴argenx将启动艾加莫德用于TED的注册临床研究。再鼎医药计划于2024年下半年在大中华区参与这一研究。
舒巴坦钠-度洛巴坦钠(SUL-DUR)
用于治疗由鲍曼不动杆菌-醋酸钙复合体敏感分离株引起感染的NDA有望获得NMPA批准。
呫诺美 林-曲司氯铵(KarXT)(M1/M4型毒蕈碱乙酰胆碱受体激动剂)
再鼎医药将于2024年第四季度在中国完成用于精神分裂症的桥接研究的患者入组。
再鼎医药将于年中在大中华区参与用于ADP的全球3期研究ADEPT-2和ADEPT-3。
再鼎医药合作伙伴Karuna将在2024年下半年公布评估用于治疗精神分裂症长期安全性的EMERGENT-4和EMERGENT-5研究的主要数据。
ZL-1102(IL-17 Humabody®)
再鼎医药将于年中启动针对轻中度慢性斑块状银屑病的全球2期研究。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57