Part 1
全球药物批准/研发动态
01
全球新药批准情况
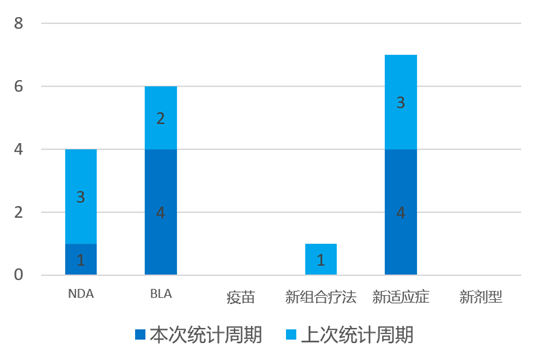
根据药渡数据统计分析,本次统计周期(2024.03.23-03.29)全球(不含中国)共有9个新药获批上市。其中,NDA批准1个,BLA批准4个,新适应症批准4个。本次批准新药数量与上个统计周期相同。
3月24日,亿帆医药宣布其子公司自主研发的创新生物药Ryzneuta® 获得欧盟委员会的批准,可在欧盟上市销售。该决定基于欧洲药品管理局(EMA)人用药品委员会(CHMP)的积极审查意见。至此,Ryzneuta®成为公司首 个在中国、美国和欧盟均已获批上市的创新生物药,也成为2024年度中国医药企业获得欧盟批准的首 个 创新药。此前,Ryzneuta®已于成功进入NCCN推荐指南和成功进入中国2023年版国家医保药品目录。
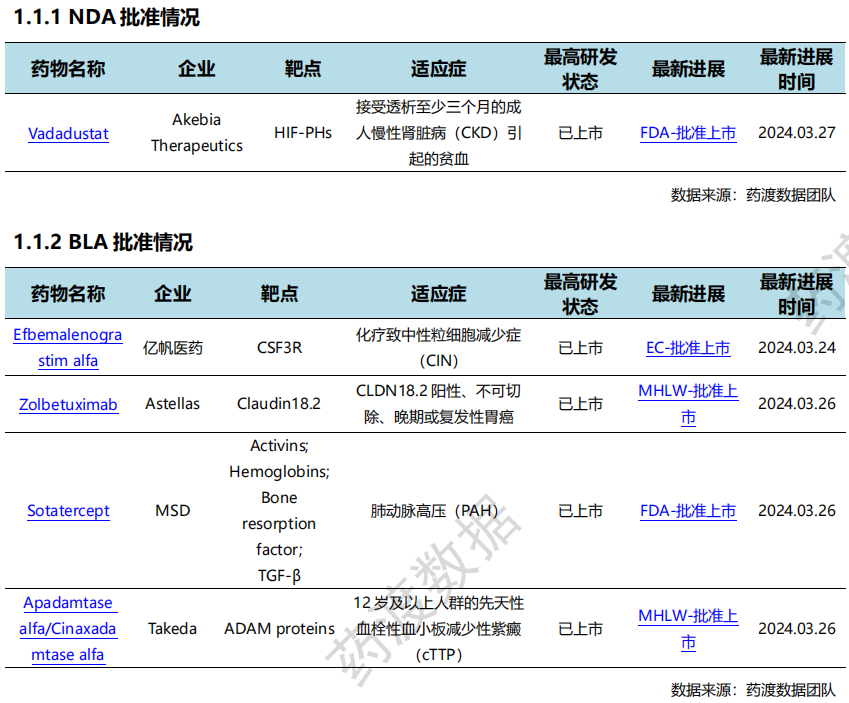
3月27日,FDA批准Akebia Therapeutics的Vafseo®(Vadadustat)片剂用于治疗已接受透析至少三个月的成人慢性肾病(CKD)引起的贫血。Vafseo® 片剂是一种每日一次的口服缺氧诱导因子脯氨酰羟化酶抑制剂,可激活对缺氧的生理反应,刺激促红细胞生成素的内源性产生,增加血红蛋白和红细胞的产生,以控制贫血。Vafseo®已获准在 37 个国家/地区使用。
全球(不含中国)新药批准情况(部分)
02
全球新药申报进展
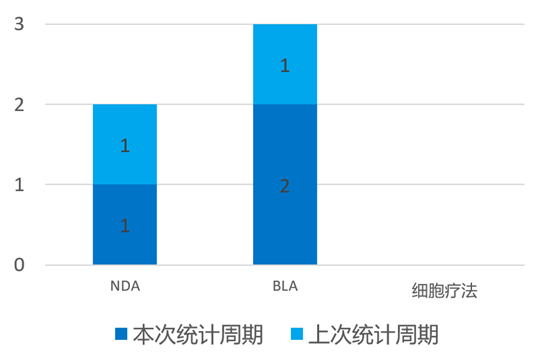
根据药渡数据统计分析,本次统计周期(2024.03.23-03.29)全球(不含中国)共有3个新药申报上市。其中,NDA申报进展1个,BLA申报进展2个。与上次统计周期相比,本次增加1个NDA/BLA申报。
3月25日,Astellas宣布CHMP通过了一项积极意见,建议批准XTANDI作为单一疗法或与雄激素剥夺疗法联合治疗,用于治疗不适合挽救性放疗的高危生化复发(BCR)非转移性激素敏感性前列腺癌(nmHSPC)成年男性。CHMP的积极意见是基于III期EMBARK试验的结果。
NDA/BLA申报情况
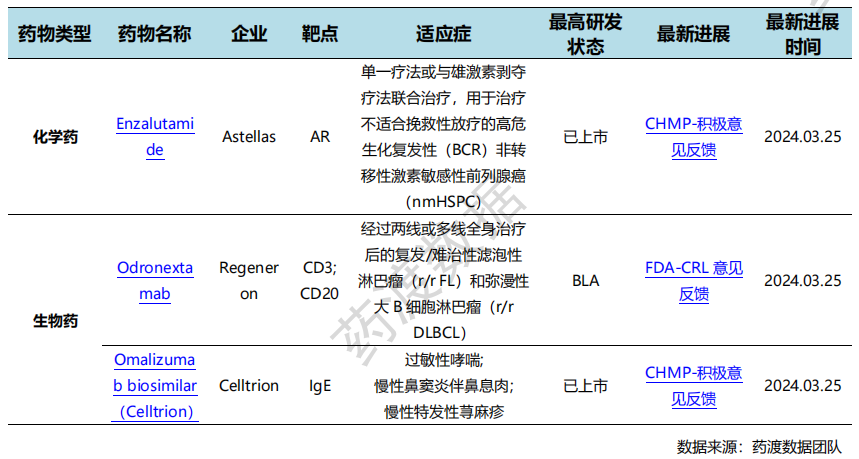
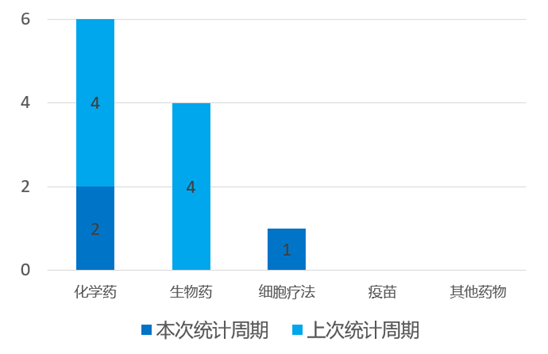
根据药渡数据统计分析,本次统计周期(2024.03.23-03.29)全球(不含中国)共有7个药物获监管机构特殊资格认定。其中,化学药4个,生物药3个。与上次统计周期相比,本次增加4个获监管机构特殊资格认定的药物。
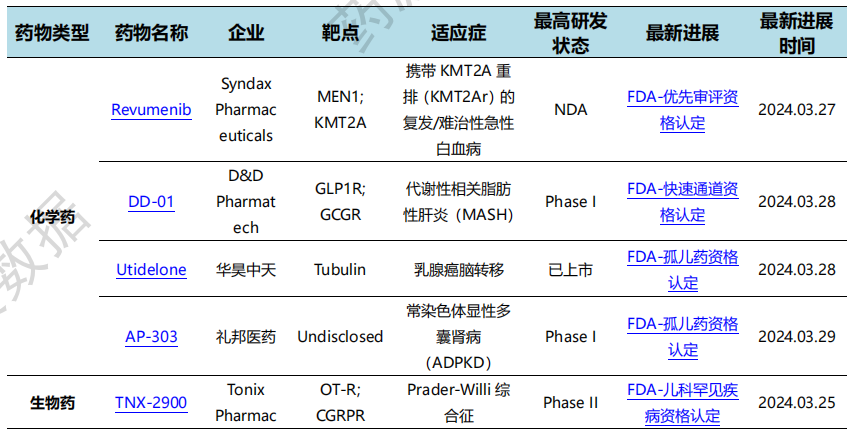
3月28日,华昊中天宣布优替德隆注射液获得FDA孤儿药认定,用于治疗乳腺癌脑转移。优替德隆独特的理化性质以及对P-糖蛋白介导的外排不敏感等优势,使其具备穿透血脑屏障的能力。该能力已通过动物脑组织分布实验、患者脑肿瘤囊液实验、以及两项针对乳腺癌脑转移的临床研究数据得到充分证实。一项优替德隆联合贝伐珠单抗和依托泊苷治疗HER2阴性乳腺癌脑转移患者II期临床共入组17例患者,中枢神经系统病灶客观缓解率(CNS-ORR)和中枢神经系统病灶临床获益率(CNS-CBR)分别达到73%和91%;另一项优替德隆联合贝伐珠单抗治疗HER2阴性乳腺癌脑转移II期临床共入组46例患者,中位无进展生存期为7.7个月,12个月总生存率达到74.4%。
特殊资格认定情况(部分)
03
全球新药研发进展
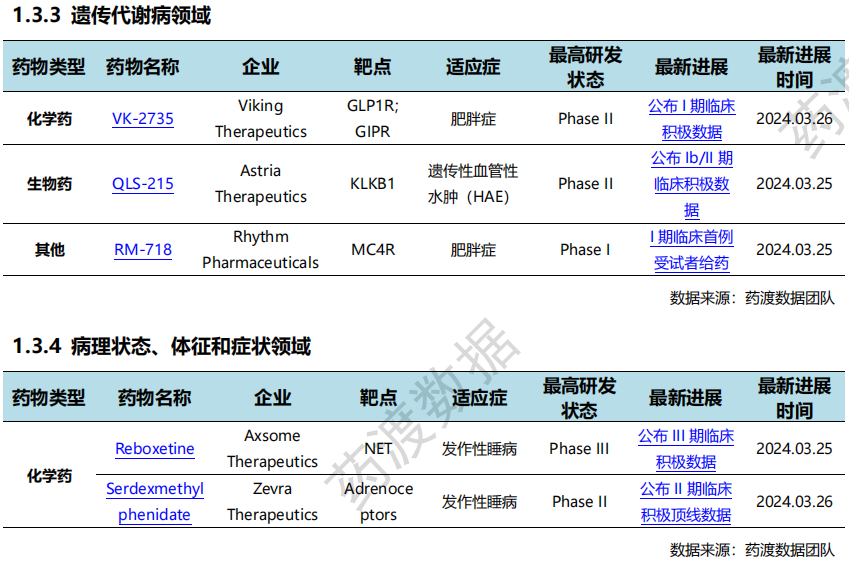
根据药渡数据统计分析,本次统计周期(2024.03.23-03.29)全球(不含中国)新药临床研发状态更新共计34条,涉及肿瘤、血液和淋巴疾病、遗传代谢病、精神疾病、免疫系统疾病以及眼部疾病等共计11个领域。
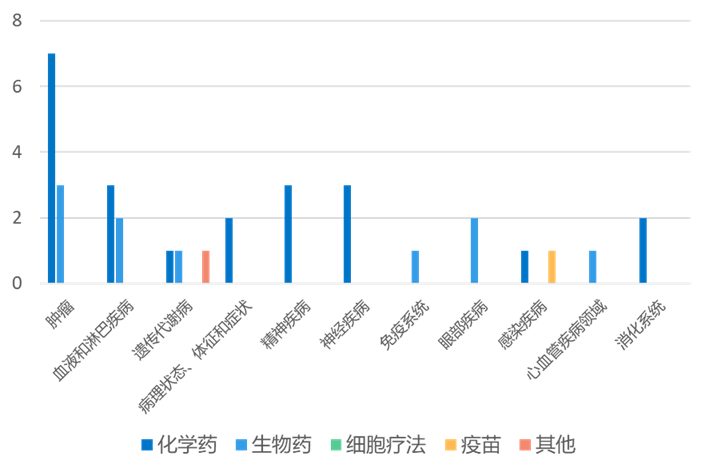
其中,肿瘤领域临床进展更新居各领域之首,涉及化学药7条,生物药3条。
3月25日,百奥泰生物宣布在研药品注射用BAT8006的II期临床试验申请(IND)已于近期获得FDA的许可,拟在铂耐药上皮性卵巢癌、输卵管癌或原发性腹膜癌患者中评估其疗效及安全性。BAT8006具有高效的抗肿瘤活性,毒素小分子有很强的细胞膜渗透能力,在ADC杀伤癌细胞后能进一步释放并杀死附近的癌细胞,产生旁观者效应,可望有效克服肿瘤细胞的异质性。同时,BAT8006表现出很好的稳定性,血浆中释放的毒素小分子极低,降低了脱靶毒性的风险。目前,BAT8006的I期临床试验已处于剂量扩展阶段,在多个肿瘤队列中进行剂量优化以及疗效探索。
3月26日,SELLAS宣布SLS009治疗无效或不再有效的复发/难治性(r/r)急性髓系白血病(AML)的IIa期研究获得积极的顶线数据。研究数据显示,在选定的最 佳剂量 30 mg BIW 下,缓解率为 50%,超过目标 20%,迄今为止,具有已确定生物标志物的患者的 100% 反应率。SLS009 在~70% 的患者中表现出强大的抗白血病活性,在所有剂量水平下都具有良好的安全性。
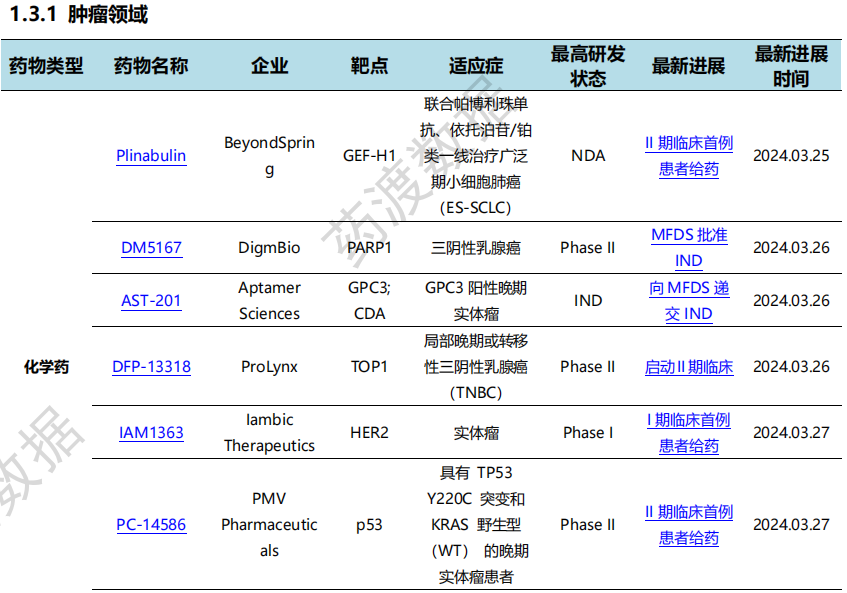
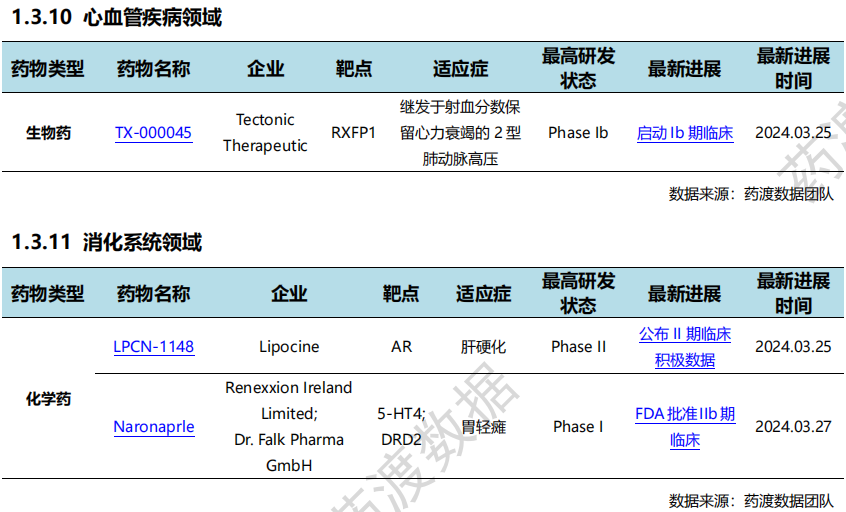
全球新药研发进展详情(部分)
04
全球医药交易事件
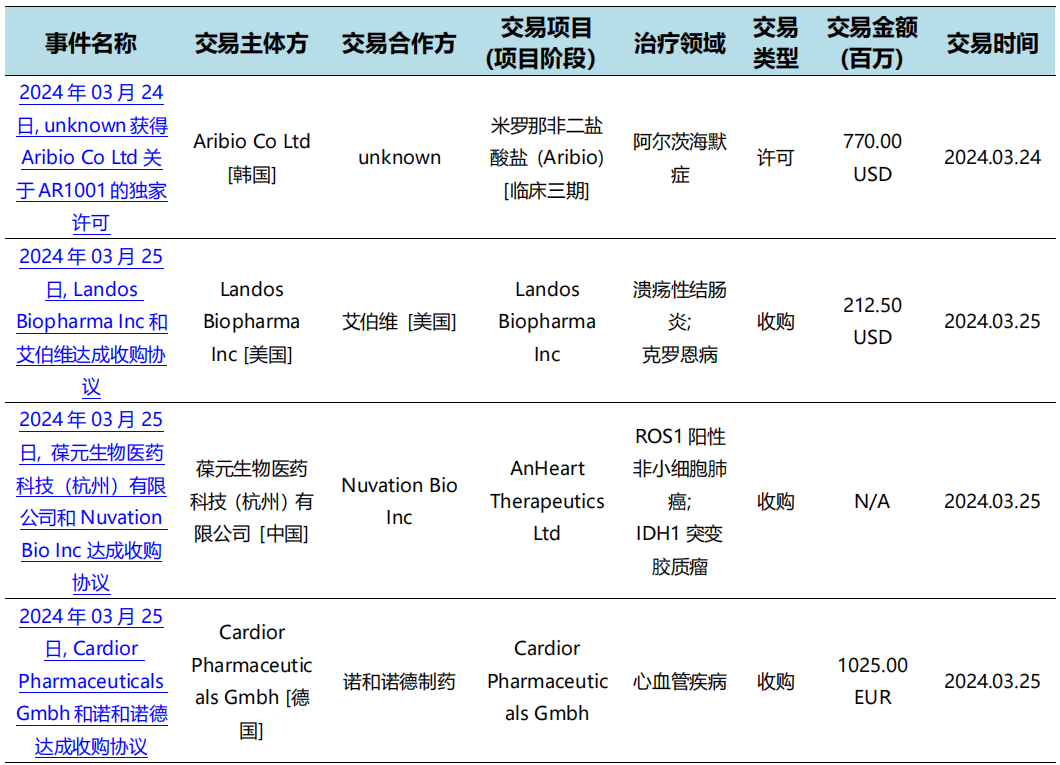
本次统计周期(2024.03.23-03.29)全球(含中国)医药交易时间共计34起,涉及药物权益转让、公司并购等多起交易事件。
全球医药交易时间汇总表(部分)
Part 2
国内药物批准/研发动态
01
国内新药批准情况
根据药渡数据统计分析,本次统计周期(2024.03.23-03.29)暂无相关药物获批。
02
国内新药临床默示许可进展
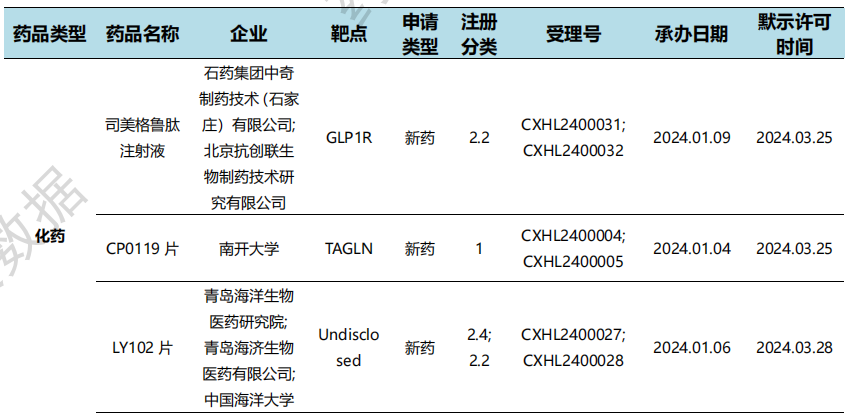
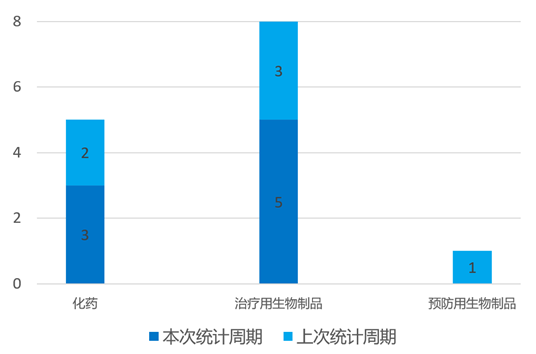
根据药渡数据统计分析,本次统计周期(2024.03.23-03.29)国内共有16个新药获临床默示许可,涉及22个受理号。其中,化学药7个,治疗用生物制品8个,预防用生物制品1个。与上个统计周期相比,本次减少63个临床默示许可获批受理号。
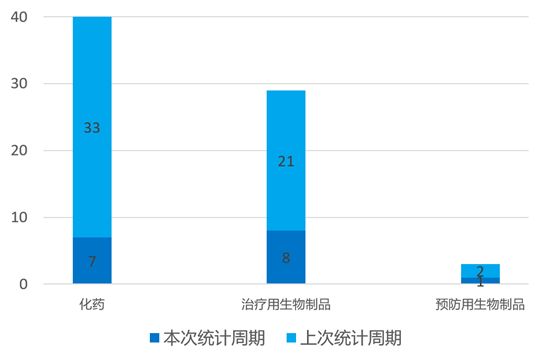
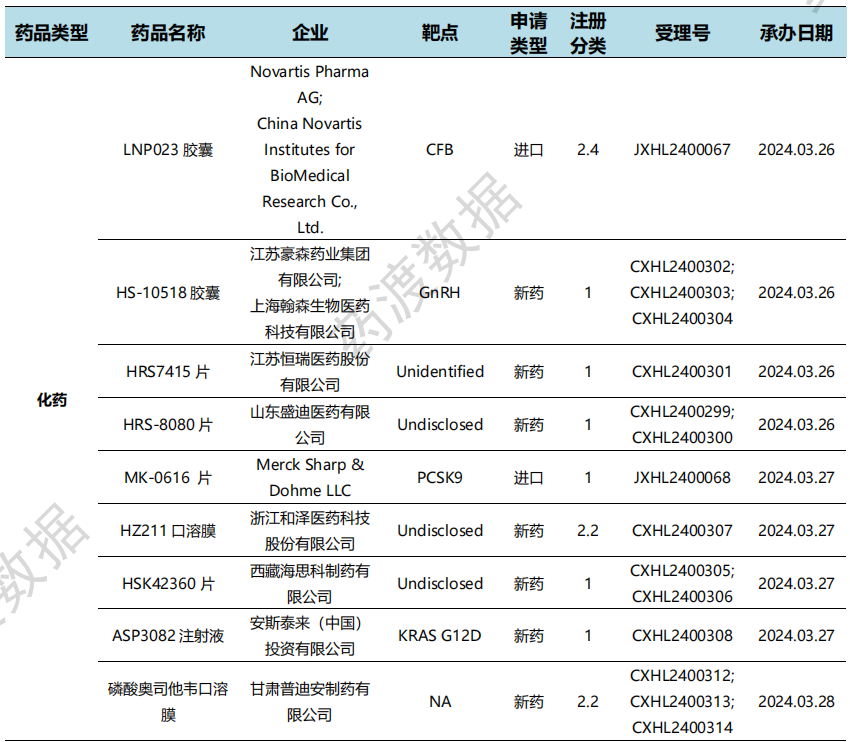
本周国内新药临床默示许可进展(部分)
03
国内新药申报进展
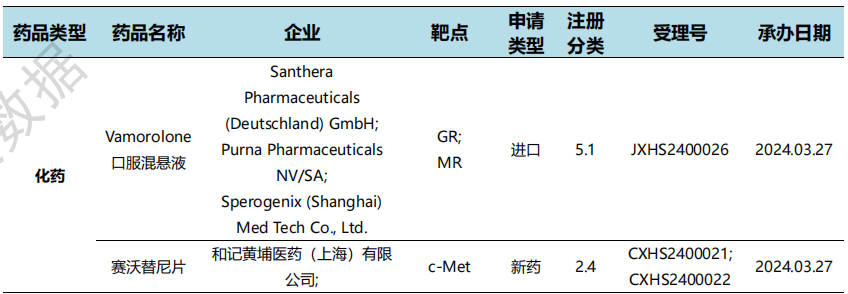
根据药渡数据统计分析,本次统计周期(2024.03.23-03.29)国内共有8个新药申报上市,涉及12个受理号。其中,化学药3个,治疗用生物制品5个。本次申报上市受理号数量与上个统计周期相同。
国内新药申报上市情况(部分)
根据药渡数据统计分析,本次统计周期(2024.03.23-03.29)国内共有27个新药申报临床,涉及41个受理号。其中,化学药16个,治疗用生物制品11个。与上个统计周期相比,本次增加10个临床申报受理号。
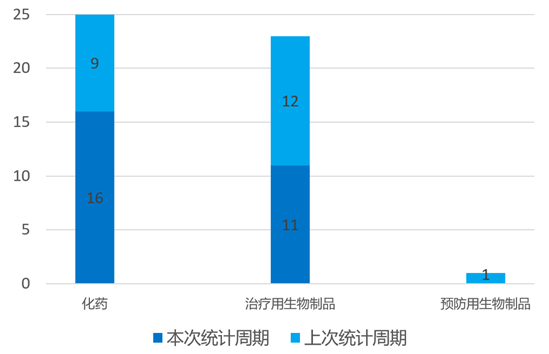
国内新药临床申报情况(部分)
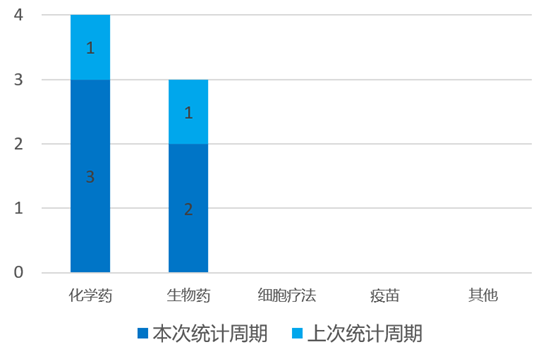
根据药渡数据统计分析,本次统计周期(2024.03.23-03.29)国内共有5个药物获NMPA特殊资格认定。其中,化学药3个,生物药2个。与上个统计周期相比,本次增加3个获监管机构特殊资格认定的药物。
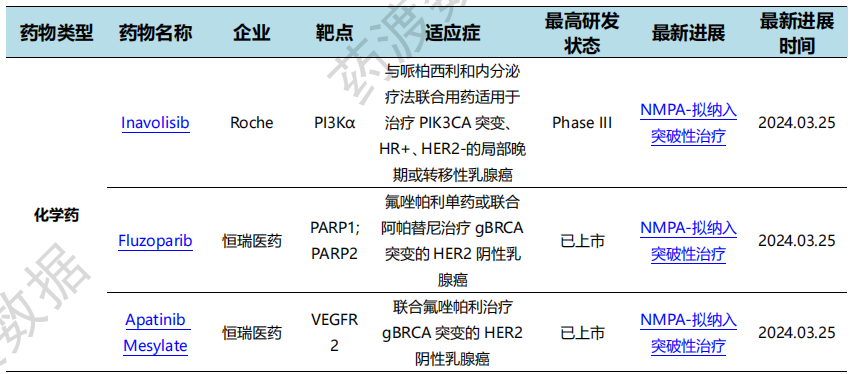
3月25日,CDE官网公示,恒瑞医药申报的氟唑帕利胶囊和甲磺酸阿帕替尼片拟纳入突破性治疗品种,适应症:氟唑帕利单药或联合阿帕替尼治疗gBRCA突变的HER2阴性乳腺癌。氟唑帕利是恒瑞医药研发的1类创新药,为一种新型口服PARP抑制剂。该药已经在中国获批用于胚系BRCA1/2(gBRCA1/2)突变的铂敏感复发性卵巢癌治疗,以及铂类敏感复发性卵巢癌维持治疗。
阿帕替尼是恒瑞医药研发一种高选择性的靶向血管内皮细胞生长因子受体2(VEGFR2)的抗血管生成药物,已经在中国获批单药治疗晚期胃腺癌或胃-食管结合部腺癌、晚期肝细胞癌,以及联合卡瑞利珠单抗治疗不可切除或转移性肝细胞癌。此外,它在卵巢癌和乳腺癌等多种实体肿瘤中均显示良好的活性和安全性。氟唑帕利单药或联合阿帕替尼的多个适应症开发已处在3期临床研究阶段。
NMPA特殊资格认定情况(部分)
04
国内新药研发进展
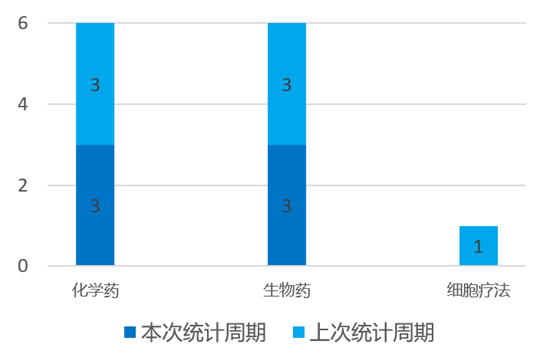
根据药渡数据统计分析,本次统计周期(2024.03.23-03.29)国内新药临床研发状态更新共计6条,涉及肿瘤和心血管疾病共计2个领域。其中,化学药3个,生物药3个。
3月27日,信达生物宣布IBI310(抗CTLA-4单抗)结肠癌新辅助III期临床研究(Neoshot)完成首例受试者给药。IBI310是信达生物自主研发的重组全人源抗细胞毒T淋巴细胞相关抗原4(CTLA-4)单克隆抗体注射液。IBI310能特异性结合CTLA-4,从而阻断CTLA-4介导的T细胞抑制,促进T细胞的激活和增殖,提高肿瘤免疫反应,达到抗肿瘤的效果。
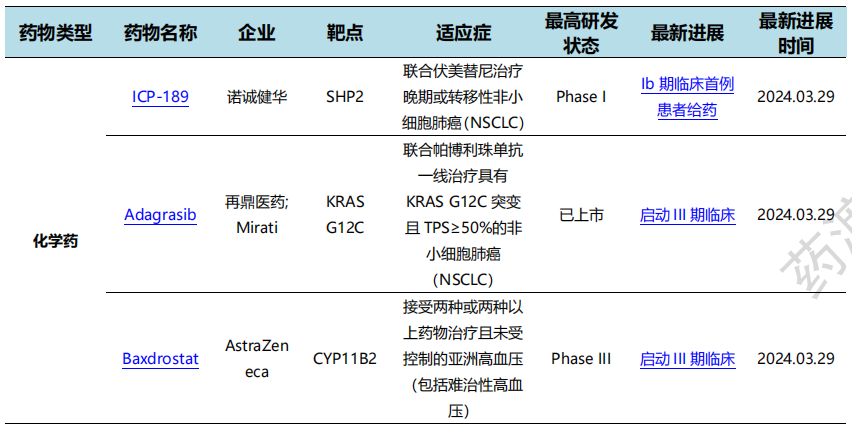
3月29日,诺诚健华宣布SHP2抑制剂ICP-189联合EGFR抑制剂伏美替尼临床研究完成首例患者给药。ICP-189是诺诚健华开发的一种高选择性的口服SHP2变构抑制剂,可用作单药疗法及/或和其他抗肿瘤药的联合疗法。ICP-189单药治疗已观察到初步疗效,在剂量爬坡研究中,剂量已增至120毫克,未观察到剂量限制性毒性(DLT),显示出良好的PK 和安全性。
国内新药研发进展情况(部分)
05
国内新药研发领域政策法规动态
国家药监局关于调整麻 醉药品和精神药品进出口准许证管理有关事宜的公告(2024年第33号)
为进一步提升“互联网+药品监管”应用水平,加强麻 醉药品和精神药品进出口准许证(以下简称准许证)管理,为企业提供更加高效便捷的政务服务,现将有关事宜公告如下:
一、自本公告发布之日起,申请人提交的准许证申报资料及补充资料,调整为电子形式提交,无须提交纸质申报资料。现有受理、审批和发证等工作程序不变。
二、申请人应当按照准许证申报资料要求(见附件)准备电子申报资料,通过国家药监局政务服务门户药品业务应用系统提出申请。
三、 取得准许证的申请人,应当将申报资料涉及的进口国主管部门出具的进口准许证原件、进出口单位资质证明文件公证或认证文本原件等保存至所取得准许证有效期满后两年备查。
四、自本公告发布之日起,准许证申请受理行政许可电子文书由药品业务应用系统推送,不再出具纸质文书。
五、自本公告发布之日起,国家药监局仅发放电子准许证,不再发放纸质证件。申请人可进入国家药监局政务服务门户“我的证照”栏目或登录“中国药监APP”,查看下载电子准许证。
06
国内新药研发领域热点新闻
利润暴涨5倍!三生国健重回巅峰
近日,三生国健发布最新年报,2023年,其总营收10.14亿元,同比增长22.84%;净利润2.95亿元,暴涨497.63%。在经历了三年的战略调整后,三生国健的发展终于又回到了正轨,不论是总营收还是净利润都回到了调整前的高度。此次王 者归来,三生国健进行了战略收缩,将主要精力全部放在了自免管线上。轻装简行下,三生国健显得更加稳健,布局也更加合理,兼顾了短中长期的发展平衡,一切都在向好的方向前进。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57