医麦客新闻 eMedClub News
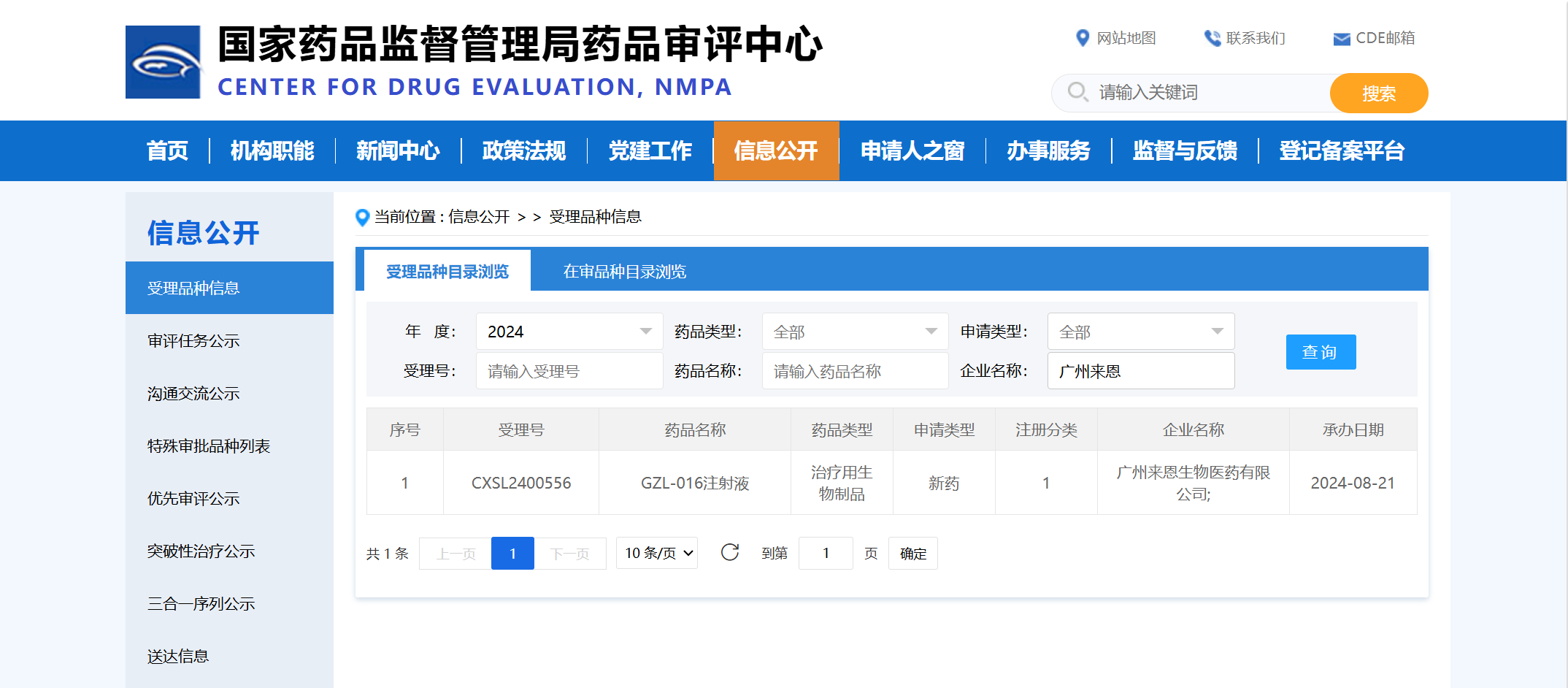
2024年8月21日,据CDE官网显示,广州来恩生物有限公司(以下简称“来恩生物”)的“GZL-016注射液”新药临床试验申请(IND)获受理。据来恩生物介绍,GZL-016注射液的适应症为乙肝病毒相关肝细胞癌。 来恩生物拥有First-in-Class、 全球首家针对乙肝病毒表面抗原的特异性T细胞受体的T细胞疗法(TCR-T)。
GZL-016注射液是一种自体T细胞疗法,通过mRNA编码表达靶向乙肝病毒表面抗原的TCR,赋予T细胞特异性识别并杀伤乙肝病毒相关肝细胞癌的能力。GZL-016注射液通过有效利用mRNA瞬时表达的特性,结合多次输注的方式,既能很好地控制安全性又能保证疗效,且患者在治疗前无需清淋,进一步提高了患者用药安全性和可及性。
2024年8月2日,全球 TCR-T细胞疗法Afami-cel(商品名:TECELRA®)在美国获批上市,用于治疗晚期滑膜肉瘤。这一重大里程碑不仅标着TCR-T这一新兴治疗技术从临床研发阶段正式步入商业化,同时也为TCR-T赛道注入了一针“强心剂”,极大地提振了TCR-T创新药企的信心,并促使TCR-T赛道的热度再次攀升。
Afami-cel的研发公司Adaptimmune对市场前景表示乐观,“预计每年销售峰值有望达到4亿美元,并且Afami-cel还具有多种适应症拓展的潜力,因此,我们有信心期待它更大的市场拓展的可能性。”
近两年,TCR疗法的市场热度已经初步显现。 2022年1月,全球 TCR蛋白疗法Kimmtrak成功获得FDA批准上市,治疗用于HLA-A*02:01阳性的无法手术切除或已发生转移的葡萄膜黑色素瘤成人患者。Kimmtrak是一种TCR/CD3双特异性融合蛋白,能有效连接肿瘤细胞与T细胞,从而激活T细胞的杀伤功能。
自上市以来,Kimmtrak的市场表现令人瞩目:上市第一年,其全球销售额就达到了1.411亿美元;2023年,全年净销售额更是攀升至2.387亿美元,同比增幅高达69%。
TCR-T疗法也吸引了众多知名跨国药企(MNC)强势布局。2022年11月,阿斯利康宣布以3.2亿美元收购专注于开发TCR-T疗法的公司Neogene Therapeutics。而作为拥有 上市CAR-T产品的公司,诺华在TCR-T细胞疗法领域的投入同样不容小觑,除了多轮投资专注于TCR-T疗法的TScan公司外,诺华还与TScan达成了数亿美元的合作,共同开发多个新靶点的TCR-T细胞疗法。百时美施贵宝(BMS)也在2023年7月向TCR-T疗法领域的Immatics公司追加投资了3500万美元,彰显了对该赛道前景的坚定信心。
国内TCR-T赛道近期也同样展现出蓬勃的发展态势,吸引了众多目光与投资。
2024年7月,香雪生命科学在研的TCR-T疗法(TAEST16001注射液)被国家药监局纳入突破性治疗品种名单,这显示了国家药监局对TCR-T疗法的高度认同与支持;8月,东北制药(SZ000597)宣布拟收购细胞治疗公司北京鼎成肽源70%的股权,这一动作无疑透露出国内老牌制药企业对TCR-T疗法的强烈看好,并正积极布局以抢占市场先机,同时也助力企业自身的创新转型。
结语
回到本次事件的主角,来恩生物GZL-016注射液新药临床试验申请(IND)获CDE受理,不仅是对公司科研实力的肯定,更是对人类健康事业的一大贡献。随着全球 TCR药物和TCR-T疗法的相继获批,TCR-T作为细胞与基因治疗(CGT)领域的热门方向,显示出巨大的市场潜力。展望未来,来恩生物将持续创新,引领全球mRNA编码TCR-T疗法的发展,为患者带来更多希望和福祉。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57