IL-15能够有效激活并扩增CD8+ T细胞和NK细胞,因而成为众多抗肿瘤免疫疗法中的明星分子。ALT-803作为一种IL-15超级激动剂,联合卡介苗于2024年4月获FDA批准上市,用于治疗对卡介苗不响应的非肌层浸润性膀胱癌。这一里程碑事件使IL-15成为历史上第三个用于癌症治疗的细胞因子,距第二个细胞因子IL-2在1992年获批已有32年。然而,与大多数细胞因子一样,IL-15仍然受到“cytokine sink”的影响,导致肿瘤部位的有效暴露量有限,从而面临严重的剂量相关性毒副作用问题。ALT-803的给药方式为膀胱内灌注,避免了静脉给药所带来的免疫相关不良反应,但至今尚无IL-15超级激动剂获得系统性给药的批准。
近日,上海交通大学药学院路慧丽团队在《Molecular Therapy》期刊上发表了题为“A tumor-conditional IL-15 safely synergizes with immunotherapy to enhance antitumor immune responses”的突破性研究成果,为IL-15在肿瘤免疫治疗中的应用开辟了新的可能性,展现了其安全性及在协同免疫疗法中增强抗肿瘤免疫反应的巨大潜力。

该团队巧妙地利用了Fc片段与IL-15Rα-sushi domain所形成的空间位阻,在不引入额外掩蔽基团的情况下成功实现了对IL-15活性的掩蔽。有趣的是,IL-15连接在Fc片段的N端时,Fc与sushi结构域无法形成有效的空间位阻来掩蔽IL-15的活性。通过优化Fc与ILR之间的可裂解连接子,该团队选择了最佳前药分子LIC19及其衍生分子LIC20(下文用pro-IL-15指代)进行活性评价。
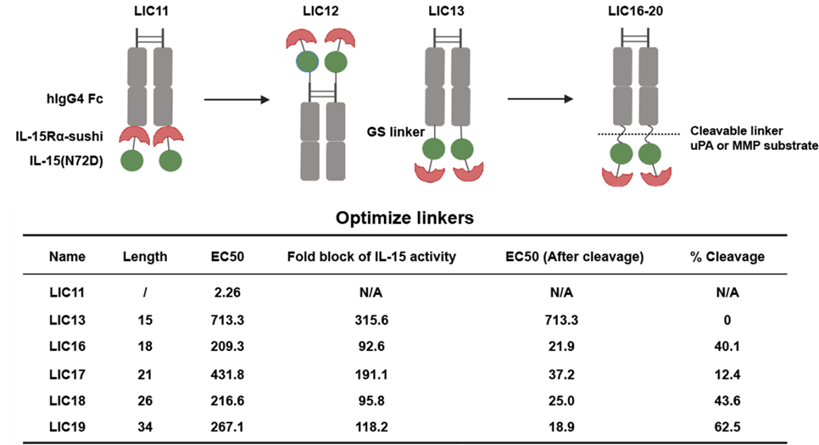
图1 肿瘤微环境响应型IL-15设计思路图
在对健康小鼠进行的系统性安全性评估中,结果显示,相较于未掩蔽的IL-15超级激动剂相,LIC19的剂量窗口至少增加了10倍。此外,LIC19在外周刺激活性方面显著降低,对外周CD8+ T和NK细胞的刺激活性也大幅减弱。进一步研究显示,Pro-IL-15与PD-L1抗体联合用药展现出显著的协同抗肿瘤疗效,诱导50%小鼠MC38肿瘤完全消退,并且治愈的小鼠产生了抗肿瘤免疫记忆。分析显示,虽然联合用药未能扩增终末耗竭CD8+ T细胞,但增强了其效应功能和杀伤功能,从而解释了其协同抗肿瘤作用的机制(图2)。
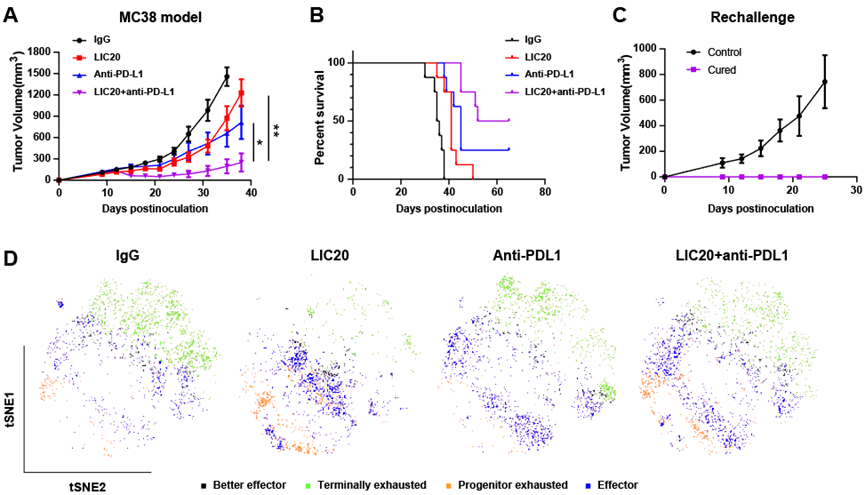
图2 Pro-IL-15协同anti-PD-L1抗肿瘤
该团队还研究了Pro-IL-15与过继性T细胞免疫疗法联合治疗实体瘤的潜力,结果显示,联合用药诱导所有小鼠的肿瘤完全消退。当再次荷瘤时,所有治愈小鼠均未长出肿瘤,表明联合用药诱导了持久的抗肿瘤免疫记忆反应,显示了其在预防肿瘤复发和转移方面的巨大潜力(图3)。
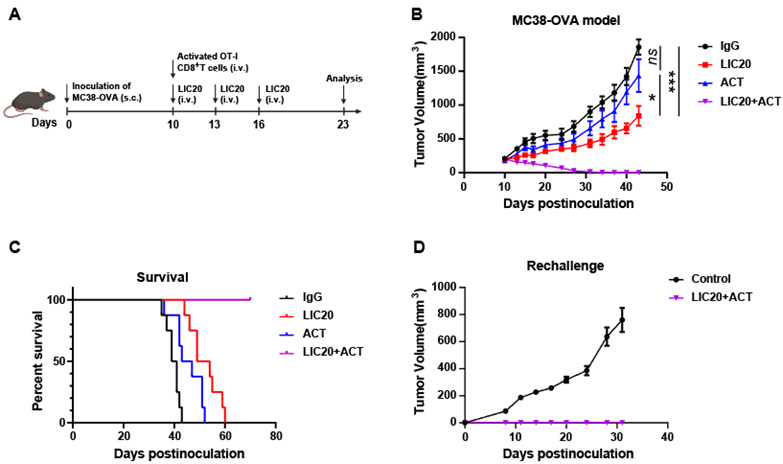
图3 Pro-IL-15联合ACT疗法清除实体瘤
除了与检查点抑制剂和过继性T细胞疗法展现出协同抗肿瘤作用外,Pro-IL-15与溶瘤病毒以及IL-12也显示出显著的协同抗肿瘤效果。无论与哪种疗法联用,Pro-IL-15均表现出良好的安全性,预示其广泛的临床应用前景。
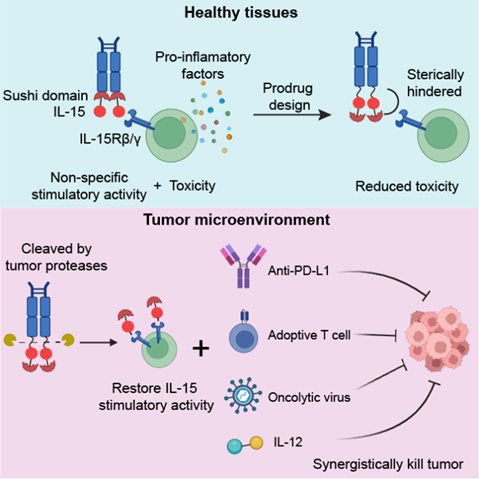
图4 Pro-IL-15的结构设计和作用机制。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57