CD8+ T 细胞的耗竭是抗肿瘤免疫的关键阻碍,当前研究集中于肿瘤微环境对 CD8+ T 细胞的调控,而忽视了 CD8+ T 细胞自身因素。不同肿瘤的微环境存在巨大差异, CD8+ T 细胞无一例外进入耗竭状态,这暗示除了外在环境因素,尚可能存在驱动 CD8+ T 细胞耗竭的内在因素。
因此,筛选在不同类型的肿瘤中普遍存在的 CD8+ T 细胞耗竭机制及潜在的驱动因素,可为同时靶向治疗不同肿瘤提供可能。
2025 年 1 月 13 日,清华大学江鹏、 武汉科技大学祝海川、北京大学李程、张泽民等人在 Nature 子刊 Nature Cancer 上发表了题为:ETV7 limits the antiviral and anti-tumor efficacy of CD8+ T cells by diverting their fate towards exhaustion 的研究论文。
研究团队从 21 种肿瘤病人中筛选到小鼠中缺失而人类具有的转录因子 ETV7,是驱动CD8+ T细胞命运向耗竭转化的核心,且广泛存在不同肿瘤中。临床前免疫治疗研究发现,靶向 ETV7 显著增强 CAR-T 细胞的抗实体瘤治疗效果。

为了筛选在临床病人中广泛存在的免疫逃逸的关键因素,研究团队使用 21 种肿瘤病人的单细胞转录组数据与 ATAC-seq 数据进行多组学分析,并通过功能性筛选,鉴定到 ETV7 是一个全新促进 CD8+ T 细胞终末分化的转录因子。进一步功能研究发现, ETV7 的表达通过促进 CD8+ T 细胞的耗竭,抑制其杀伤肿瘤和清除病毒的能力。
机制研究发现,在 CD8+ T 细胞分化过程中,ETV7 作为中心调控因子,逐渐增强与耗竭基因(CTLA4、TOX等七个基因)和记忆基因(TCF7等4个基因)的结合与转录调控,通过结合和调控多个经典T细胞耗竭相关基因(CTLA4、TOX等七个基因)和记忆基因(TCF7等4个基因),将 CD8+ T 细胞的命运从记忆转化为终末耗竭,说明 ETV7 可能是人 CD8+ T 细胞耗竭命运决定的中心调控因子(master regulator)。进一步将该研究应用于临床前实验中发现,在 CAR-T 治疗实体瘤模型中,敲低 ETV7 的表达能够显著抑制 CAR-T 细胞耗竭,增强 CAR-T 杀伤肿瘤的功能,为肿瘤免疫治疗提供了新的策略和筛选靶标。
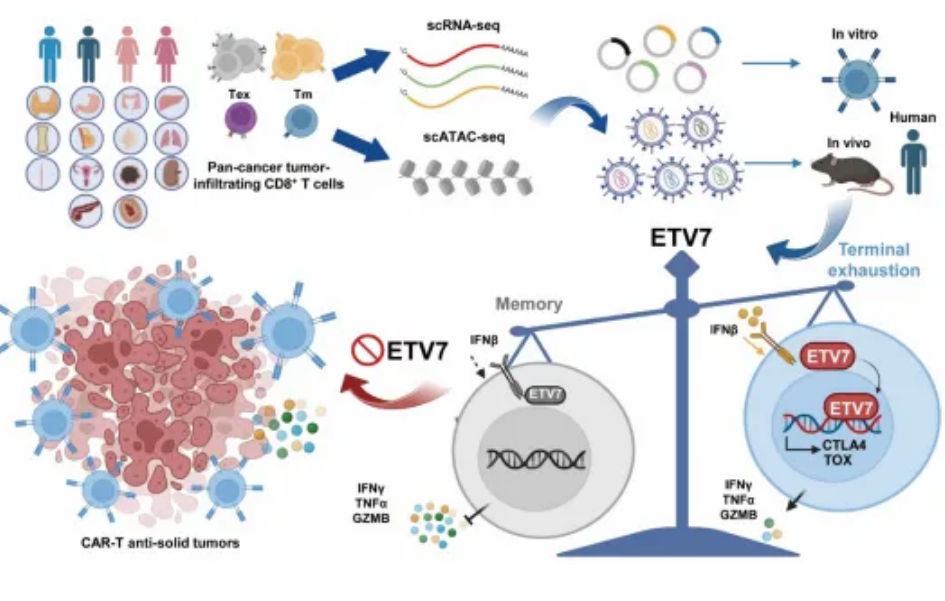 肿瘤病人单细胞多组学与筛选鉴定到 ETV7 是调控 CD8+ T 细胞命运的转录焦点,促进 CD8+ T 细胞的终末分化(耗竭)与功能缺失。靶向 ETV7 有效增强 CAR-T 杀伤实体瘤的效率。
肿瘤病人单细胞多组学与筛选鉴定到 ETV7 是调控 CD8+ T 细胞命运的转录焦点,促进 CD8+ T 细胞的终末分化(耗竭)与功能缺失。靶向 ETV7 有效增强 CAR-T 杀伤实体瘤的效率。
程洁(现为华中科技大学同济医学院独立PI)、清华大学2021级研究生肖一峰、北京大学彭婷、武汉科技大学张子健和华中科技大学秦铀为论文共同第一作者。江鹏、祝海川、李程、张泽民为论文共同通讯作者。
论文链接:
https://www.nature.com/articles/s43018-024-00892-0



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57